
- •Оглавление Введение…………………………………………………………………………3
- •Превращение микроорганизмами соединений углерода……………………..5
- •2) Образование щавелевой кислоты………………………………………….27
- •Заключение……………………………………………………………………...40
- •Введение
- •1)Гликолиз:
- •Анаэробное дыхание
- •2) Брожение
- •3) Аэробное дыхание
- •Суммарное уравнение цикла трикарбоновых кислот можно представить:
- •Энергетическая эффективность процесса полного окисления глюкозы
- •Рассмотрим 3 этапа энергетического выхода аэробного дыхания(рис.5):
- •Затем две молекулы nadн, образованные в результате этого окисления, поступают в дыхательную цепь:
- •2) Образование щавелевой кислоты
- •3) Образование лимонной кислоты
- •4) Образование глюконовой кислоты
- •5) Разложение клетчатки
- •6) Окисление углеводородов
- •7) Окисление жиров
- •8) Окисление высокомолекулярных кислот жирного ряда
- •Заключение
- •Список литературы
Суммарное уравнение цикла трикарбоновых кислот можно представить:
ацетил-КоА + 3 NAD++ FAD+ГДФ +Н3РО4 →2СО2+ 3NADН∙Н+ +ФАДН2+ГТФ
Цикл Кребса — это ключевой этап дыхания всех клеток, использующих кислород, центр пересечения множества метаболических путей в организме. Кроме значительной энергетической роли циклу отводится также и существенная пластическая функция, то есть это важный источник молекул-предшественников, из которых в ходе других биохимических превращений синтезируются такие важные для жизнедеятельности клетки соединения как аминокислоты,углеводы,жирныекислоты.
Но так как из цикла постоянно происходит постоянный отток для биосинтезов промежуточных метаболитов, приводящий к понижению уровня щавелево-уксусной кислоты, возникает необходимость в ее дополнительном синтезе. У некоторых микроорганизмов это обеспечивается с помощью последовательности из двух реакций, получивших название глиоксилатного шунта (рис.4).В первой из них изолимонная кислота под действием изоцитратлиазы расщепляется на янтарную и глиоксиловую кислоты. Во второй реакции, катализируемой малатсинтетазой, глиоксиловая кислота конденсируется с ацетил-КоА с образованием яблочной кислоты, превращающейся далее в щавелево-уксусную кислоту. В результате двух новых реакций происходит синтез С4-кислоты из двух С2-остатков. Глиоксилантный шунт не работает при выращивании на субстратах, катаболизирование которых приводит к образованию пировиноградной кислоты. Он включается при выращивании микроорганизмов на С2-соединениях.
Передача (водорода) электронов на кислород происходит не прямым путем, а в результате сложного многоступенчатого процесса дыхательной цепи. Далее рассмотрим состав и функционирование цепи транспорта электронов у аэробных микроорганизмов.
Строение дыхательной цепи аэробных микроорганизмов
В переносе электронов от субстратов к молекулярному кислороду принимают участие:
1)Пиридинзависимые дегидрогеназы, для которых коферментами служат либо NAD, либо NADF;
2)Флавинзависимые дегидрогеназы (флавиновые ферменты), у которых роль простетической группы играют FAD или FMN;
3)Цитохромы, содержащие в качестве простетической группы железопорфириновую кольцевую систему.
Среди компонентов дыхательной цепи обнаружены также убихинон (кофермент Q) и железосерные белки.
Общую схему переноса водорода (электронов) к молекулярному кислороду можно представить следующим способом:
Субстрат→ NAD∙H2→ Флавопротеин→ Кофермент Q→Цитохром b→
→ Цитохром с1 → Цитохром с → Цитохром аа3→ О2
Дыхательная цепь у прокариот находится в цитоплазматической мембране, а у эукариот – в мембране митохондрий. Дыхательная цепь построена таким образом, что одни ее компоненты переносят только атомы водорода, а а другие – только электроны. Причем переносчики атомов водорода и переносчики электронов последовательно чередуются в дыхательной цепи. Флавопротеины и хиноны осуществляют перенос атомов водорода, а FeS-белки и цитохромы – электронов.
Ф

В присутствии восстановленного субстрата (S-H2) – донора электронов и соответствуюзщей дегидрогеназы пиридиновое кольцо восстанавливается путем связывания в четвертом положении одного протона и двух электронов, а второй протон остается в среде:
Субстрат-Н2 +NAD+→Субстрат +NADH +H+
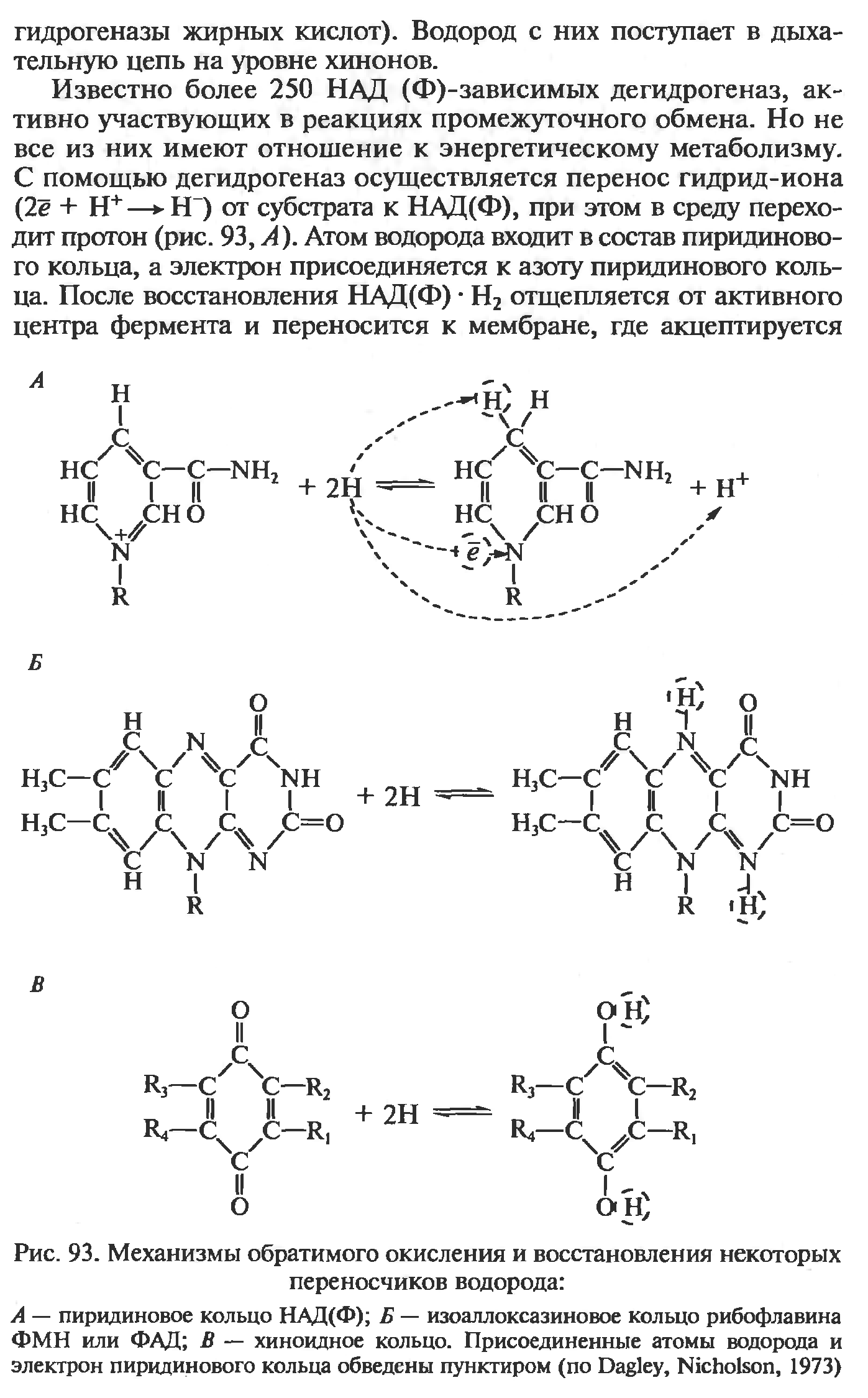
Следующим акцептором атомов водорода является группа флавиновых ферментов:
NADH+ H+ +FAD → FADH2+ NAD+
В некоторых случаях, например окисления сукцината, флавиновые ферменты могут играть роль первичных дегидрогеназ, т.е. прямо, без участия NAD и NADF-зависимых дегидрогеназ, принимать электроны и протоны при окислении субстратов.Такой фермент, в частности, сукцинатдегидрогеназа.
Восстановленная форма флавиновых ферментов передает атомы водорода (протоны и электроны) убихинону (коферменту Q):
Кофермент Q + FADH2→Кофермент Q∙Н2+ FAD
Кофермент Q - жирорастворимое соединение, которое служит «сборщиком» водорода, поставляемого различными коферментами и простетическими группами. Здесь атом водорода расщепляется на протон и электрон. Протон выделяется в среду, электрон передается на систему цитохромов, которые включаются в дыхательную цепь в определенной последовательности:
Цитохром b→ Цитохром с1 → Цитохром с → Цитохром аа3
Все цитохромы представляют собой гемопротеины. При этом в обратимой окислительно-восстановительной реакции участвует атом железа гемма, таким образом они переносят только электроны:
![]()
Каждый из этих цитохромов находясь в окисной Fe3+ форме, присоединяет один электрон и переходит в закисную Fe2+ форму.
Последним в ряду переносчиков электронов стоит цитохром аа3 (цитохромоксидаза), который является терминальным дыхательным ферментом, непосредственно взаимодействующим с кислородом. Восстановленная форма цитохрома Fe2+ вновь окисляется в Fe3+ форму молекулярным кислородом. Образовавшийся «активный» кислород присоединяет два протона из окружающей среды, в результате чего образуется молекула воды:
2H++О2-→Н2О
Во время прохождения электронов по цепи энергия освобождается отдельными небольшими порциями. Это осуществляется за счет разницы окислительно-восстановительных потенциалов. Для синтеза 1 АТФ достаточно 150-300 мВ. Такая разница достигается в электронно-транспортной цепи в трех определенных местах, называемых пунктами сопряжения, так как именно там находится АТФ-фаза.
