
- •060101 65 – Лечебное дело, 060103 65 – Педиатрия, 060105 65 – Стоматология, 060104 65 – Медико-профилактическое дело
- •Тема 1. Поверхностные явления 12
- •Предисловие
- •Введение
- •Тема 1. Поверхностные явления
- •1. Свободная поверхностная энергия, поверхностное натяжение
- •2. Смачивание, адгезия, когезия
- •3. Сорбция и ее виды
- •Абсорбция
- •Адсорбция на подвижной поверхности раздела фаз
- •Адсорбция пав в системе воздух-вода
- •Адсорбция на неподвижной поверхности раздела фаз
- •Молекулярная (неэлектролитов) адсорбция из растворов.
- •Адсорбция ионов из растворов
- •Ионообменная адсорбция
- •Основные физико-химические характеристики ионитов
- •4. Хроматография
- •5. Биологические поверхностно-активные вещества
- •6. Медико-биологическое значение адсорбции
- •Типы сорбентов, использующихся для удаления различных веществ
- •Основные области применения энтеросорбентов
- •Тема 2. Дисперсные системы
- •1. Классификация дисперсных систем
- •Свободно- и связнодисперсные системы
- •Лиофобные и лиофильные дисперсные системы
- •Классификация дс по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •2. Методы получения и очистки дисперсных систем
- •Методы очистки дисперсных систем
- •3. Лиофобные коллоидные растворы
- •Строение мицелл в лиофобных коллоидных растворах
- •Устойчивость лиофобных коллоидных растворов
- •Кинетика коагуляции
- •Механизм коагуляции
- •Пептизация или физико-химическое диспергирование
- •Коллоидная защита и флокуляция
- •4. Лиофильные коллоидные растворы
- •Истинный раствор ((;(( коллоидный раствор.
- •Зависимость области применения пав от значения глб
- •Свойства лиофильных коллоидных растворов пав и вмс
- •Ослабление высаливающего действия
- •Солюбилизация
- •5. Микрогетерогенные дисперсные системы
- •Аэрозоли и их свойства
- •Порошки и их свойства
- •Суспензии и их свойства
- •Эмульсии и их свойства
- •Пены и их свойства
- •Тема 3. Свойства вмс и их растворов
- •Классификация вмс
- •Полимерные полиэлектролиты и их свойства
- •Свойства растворов вмс, общие с истинными растворами:
- •Кислотно-основные свойства белков
- •Значения pI белков живого организма
- •Окислительно-восстановительные свойства белков
- •Комплексообразующие свойства белков
- •Поверхностные свойства белков
- •3. Набухание и растворение вмс
- •4. Вязкость растворов вмс
- •5. Осмотические свойства растворов вмс
- •6. Мембранное равновесие Доннана
- •7. Устойчивость и разрушение растворов вмс
- •8. Застудневание (желатинирование). Возникновение связнодисперсных систем и их свойства
- •Обучающие тесты
- •Обучающие задачи
- •Учебно-исследовательские лабораторные работы
- •Тема I. Поверхностные явления
- •Тема: Адсорбция уксусной кислоты на активированном угле. Качественные опыты по адсорбции и хроматографии
- •Тема: Определение обменной емкости ионита
- •Тема: Изотерма поверхностного натяжения и адсорбции изоамилового спирта на твердом адсорбенте
- •Учебно-исследовательская лабораторная работа № 4 Тема: Изучение адсорбции пав на твердом адсорбенте из водных растворов
- •Тема II. Дисперсные системы
- •Тема: Получение и свойства лиофобных коллоидных растворов
- •Конденсационный метод получения золей (химическая конденсация)
- •II. Дисперсионный метод получения золей.
- •Тема: Устойчивость и коагуляция лиофобных коллоидных растворов. Коллоидная защита
- •Тема: Получение и свойства эмульсий
- •Тема III. Растворы вмс
- •Учебно-исследовательская лабораторная работа №8
- •Тема: Вискозиметрическое определение молекулярной
- •Массы полимера
- •Тема: Набухание вмс
- •Тестовые задания, задачи, упражнения для самостоятельного решения
- •Тема 1. Поверхностные явления
- •Тема II. Дисперсные системы
- •Тема III. Растворы вмс
- •Тестовый контроль по теме: «Поверхностные явления».
- •Тестовый контроль по теме: «Лиофобные коллоидные растворы»
- •Тестовый контроль по теме: «Свойства вмс и их растворов».
- •Темы реферативных докладов для студентов лечебного, педиатрического, стоматологического и медико-профилактического факультетов
- •Список использованной литературы
- •Приложение
- •1. Основные единицы измерения физических величин
- •2. Основные физические постоянные
- •3. Метрическая система мер
- •4. Множители и приставки для образования десятичных кратных и дольных единиц и их обозначения
- •5. Плотность пав в жидком состоянии
- •6. Зависимость поверхностного натяжения воды от температуры
- •7. Поверхностное натяжение жидкостей при 293 k
- •Зависимость адсорбции газов на древесном угле от
- •9. Золотые числа
- •10. Критические концентрации мицеллообразования для некоторых мыл
- •11. Значения констант в уравнении Марка-Хаувинка и омм полимеров
Тема 2. Дисперсные системы
Цели изучения: получение представления о разнообразии дисперсных систем, их применении в медицине; природе коллоидного состояния; методах получения и очистки, свойствах коллоидных растворов; познание особенности лиофобных и лиофильных коллоидов, осознание их биологической роли; познание механизма коагуляции, принципа коллоидной защиты; формирование умения составлять формулы мицелл, пользоваться математическим аппаратом для расчетов порога коагуляции, защитного числа; выработка ценностного отношения к получаемым знаниям и умениям как профессионально значимым.
& Повторите и вспомните:
Гетерогенные системы.
Поверхностная энергия. Энергия Гиббса. Адсорбция. Ионная адсорбция. Правило Панета-Фаянса.
Способы выражения концентрации вещества в растворе.
Диффузия, осмос.
Оптические явления - дифракция, интерференция, светорассеивание (физика).
Электролиты сильные и слабые.
Реакция среды, рН.
Строение клеточных мембран (биология, гистология).
Учебно-целевые вопросы
Дисперсные системы. Классификация дисперсных систем.
Лиофобные коллоиды (золи). Строение мицеллы. Возникновение межфазного (jмф) и электрокинетического (x– (дзета) потенциалов.
Способы получения коллоидных растворов: диспергационные, конденсационные.
Методы очистки золей. Принцип АИП (аппарат «искусственная почка»).
Молекулярно-кинетические, оптические и электрокинетические свойства коллоидных систем.
Понятие о кинетической и агрегативной устойчивости золей. Коагуляция коллоидных систем и факторы, ее вызывающие. Суть теории Дерягина-Ландау-Фервея-Овербека (ДЛФО).
Механизм электролитной коагуляции. Нейтрализационная и концентрационная коагуляция.
Кинетика коагуляции. Коагуляция явная, скрытая, быстрая, медленная. Порог коагуляции. Правило Шульце-Гарди.
Коагуляция смесями электролитов. Гетерокоагуляция, пептизация. Биологическая роль.
Коллоидная защита, флокуляция, их биологическая роль.
Лиофильные коллоиды, получение, ККМ, свойства, биологическая роль.
Микрогетерогенные системы, краткая характеристика, применение в медицине.
Краткая теоретическая часть
Д исперсной
системой
называется
гетерогенная система, в которой дисперсная
фаза раздроблена и распределена в
дисперсионной среде (рис.14)
исперсной
системой
называется
гетерогенная система, в которой дисперсная
фаза раздроблена и распределена в
дисперсионной среде (рис.14)
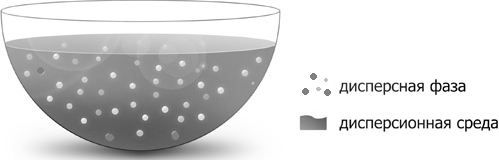
Рис. 14. Дисперсная система
1. Классификация дисперсных систем
В окружающей нас природе, как и в живом организме редко встречаются индивидуальные химические вещества. Чаще многообразие веществ, составляющих живую и неживую природу, представлено в виде растворов или в виде дисперсных систем.
Дисперсные системы в природе отличаются огромным разнообразием, поэтому невозможно составить для них единственную классификацию. Существуют общие признаки, которые характерны для всех дисперсных систем, и частные, распространяющиеся лишь на отдельные виды этих систем.
Классифицировать дисперсные системы можно на основе следующих общих признаков:
агрегатное состояние дисперсной фазы и дисперсионной среды;
размер и распределение частиц дисперсной фазы по размерам;
вид дисперсной фазы.
Дисперсность (степень дисперсности) D вещества обратно пропорциональна размеру частиц a (D ~ 1/a) и определяется удельной поверхностью Sуд, равной отношению общей площади поверхности частиц к единице объема (или иногда массы) дисперсной фазы Sуд = S/V.
Для пористых веществ (систем, тел), например адсорбентов и катализаторов, понятие дисперсности заменяется равнозначным понятием пористости, т. е. характеристикой размеров каналов пор, пронизывающих эти тела.
В химии высокомолекулярных соединений дисперсностью часто называют характеристику размеров линейных или разветвленных (цепочечных) полимерных молекул, определяемую молярной массой.
Классификация состояния вещества по степени его дисперсности приведена в табл. 3.
Таблица 3
Состояние вещества в зависимости от степени дисперсности
Состояние вещества |
Раздробленность вещества |
Размер частиц, нм |
Степень дисперсности D, см-1 |
Число атомов в одной частице (шт) |
Средство наблюдения |
Макроскопическое |
Грубодисперсная |
107–105 |
10–102 |
>1018 |
Невооруженный глаз |
Микроскопическое |
Тонкодисперсная |
105–102 |
102–105 |
>109 |
Оптические микроскопы |
Коллоидное или наноструктуриро-ванное |
Ультрадисперсная |
102–1 |
105–107 |
109–102 |
Ультрамикроскопы, РЭМ, ТЭМ, СЗМ |
Молекулярное, атомное и ионное |
Молекулярная, атомная и ионная |
100–10–1 |
>107 |
<102 |
Высокоразрешающие (<0,1 нм) РЭМ, ТЭМ, СЗМ |
(РЭМ и ТЭМ – сканирующие и просвечивающие электронные микроскопы; СЗМ – сканирующие зондовые микроскопы.)
Из таблицы видно, что коллоидное состояние является ультрадисперсным состоянием вещества, и, в соответствии с современными представлениями может быть названо наноструктурированным состоянием вещества, так как содержит структурные единицы (частицы, фазы, кристаллиты, зерна, нити, пленки, блоки, домены, пузырьки, поры) с размерами в диапазоне (1,0–100) нм.
Под коллоидами понимается не отдельный класс веществ, а особое состояние любого вещества, характеризующееся, прежде всего, определенными размерами его частиц, структур, слоев, физических и химических фаз.
 Вещества
и материалы в наноструктурированном
(коллоидном) состоянии с размерами фаз,
частиц, структур и слоев в диапазоне
(1,0 – 100) нм принято для краткости называть
наносистемами,
а сами частицы, структуры, слои (пленки)
и фазы - соответственно
Вещества
и материалы в наноструктурированном
(коллоидном) состоянии с размерами фаз,
частиц, структур и слоев в диапазоне
(1,0 – 100) нм принято для краткости называть
наносистемами,
а сами частицы, структуры, слои (пленки)
и фазы - соответственно
наночастицами, наноструктурами, нанослоями, (нанопленками) и нанофазами. Совокупности наночастиц, наноструктур, нанослоев, (нанопленок) и нанофаз часто называются нанообъектами.
Перевод вещества или материала в коллоидное состояние называется наноструктурированием, под которым следует понимать не только их получение в виде свободных наночастиц и свободных нанослоев, но создание на их поверхности наноструктур и нанослоев, а в их объеме физических или химических нанофаз, которые можно рассматривать как своеобразные наночастицы и нанослои, отделенные от остальной структуры поверхностями раздела.
Нанотехнологии – это способы контролируемого получения веществ, материалов и сред в коллоидном (ультрадисперсном с размерами дисперсных частиц, структур, слоев, физических или химических фаз в диапазоне (1,0 – 100) нм) состоянии, т.е. способы их контролируемого наноструктурирования, исследования и измерения их свойств и характеристик и использования их в различных отраслях науки, техники и промышленности.
Наноструктурированное состояние вещества может достигаться из верхнего (более крупного) макро- или микроскопического состояния вещества путем его диспергирования (диспергационными методами нанотехнологий) или подходом «сверху вниз» и из нижнего (более мелкого) молекулярного (атомного, ионного) состояния вещества путем его конденсации (конденсационными методами нанотехнологий) или подходом «снизу вверх».
По характеру взаимодействия частиц дисперсной фазы между собой дисперсные системы можно подразделить на два класса (табл. 4): свободнодисперсные, в которых частицы дисперсной фазы слабо связаны между собой и они могут свободно перемещаться друг относительно друга. Подобные системы характеризуются текучестью (золи, эмульсии). В связнодисперсных системах частицы дисперсной фазы соединены теми или иными связями. В итоге они образуют пространственные структуры – решетки, сетки и т.д. – и текучесть системы невелика (студни, гели).
Таблица 4
