- •Содержание
- •2 Лабораторные работы
- •2. 1 Титриметрический анализ, химическая посуда
- •Способы выражения концентрации растворов
- •Химическая посуда
- •Контрольные вопросы:
- •2. 2 Дисперсные системы и электрокинетические явления
- •Двойной электрический слой.
- •Электрокинетические явления.
- •Цель работы.
- •Приборы и реактивы
- •Выполнение работы.
- •Обработка результатов.
- •Контрольные вопросы.
- •2. 3 Коагуляция и седиментация.
- •Цель работы:
- •Приборы и реактивы
- •Выполнение работы.
- •Обработка результатов.
- •Контрольные вопросы.
- •2. 4 Определение критической концентрации мицеллообразования. Поверхностно-активные вещества, классификация.
- •Адсорбция на границе раздела фаз.
- •Мицеллообразование
- •Гидрофильно-липофильный баланс
- •Солюбилизация.
- •Методы определения ккм
- •Цель работы:
- •Приборы и реактивы:
- •Выполнение работы
- •Обработка результатов
- •Контрольные вопросы.
- •2. 5 Расчет параметров кристаллической решетки сдг
- •Цель работы:
- •Выполнение работы
- •Обработка результатов
- •Контрольные вопросы.
- •3 Примеры решения задач по теме «Неорганические мицеллы»
- •3.1 Задачи на выпадение осадка (Произведение растворимости)
- •3.2 Задачи на определение формулы мицеллы
- •3.3 Задачи для самостоятельного решения:
- •4 Темы для самостоятельного изучения
- •4.1 Адсорбция.
- •Уравнение изотермы адсорбции Ленгмюра (Лэнгмюра)
- •Уравнение изотермы адсорбции Фрейндлиха
- •Теория полимолекулярной адсорбции Поляни (1915)
- •Уравнение изотермы адсорбции бэт
- •Контрольные вопросы.
- •4.1 Анализ твердой поверхности на содержание кислотно-основных центров
- •Контрольные вопросы:
- •4.3 Жидкие кристаллы
- •Контрольные вопросы:
- •5 Вопросы к аттестационному тестир
- •5.1 По предмету «Физикохимия наночастиц и наноматериалов»
- •5.2 По предмету «Физикохимия наноструктурированных материалов»
- •Приложение Лабораторный журнал
Гидрофильно-липофильный баланс
Кроме поверхностной активности, непосредственно определяющей адсорбционную способность ПАВ, другой важной количественной характеристикой коллоидных ПАВ является гидрофильно-липофильный баланс (ГЛБ). Соотношение между гидрофильными свойствами полярной группы и липофильными (липос – жир) свойствами углеводородного радикала, зависящими от его размера, характеризуется числами ГЛБ. Числа ГЛБ определяются путем сравнения способности различных ПАВ к мицеллообразованию, стабилизации эмульсий и др.
Физический смысл эмпирических чисел ГЛБ состоит в том, что они определяют отношение работы адсорбции молекул ПАВ на границе раздела из фазы «масло» к работе адсорбции на той же границе из фазы «вода».
Таким образом, числа ГЛБ линейно связаны с поверхностной активностью. Именно эти параметры должны быть критериями оценки ПАВ. Однако на практике обычно качество ПАВ оценивают по числам ГЛБ. Так, для получения устойчивых прямых эмульсий (масло в воде) используют ПАВ с числами ГЛБ от 10 до 16 (в зависимости от природы масла), для получения обратных эмульсий (вода в масле) – от 3 до 5; при ГЛБ 7-8 наблюдается переход эмульсий от прямых к обратным; числа ГЛБ составляют для смачивателей 7-9, моющих средств 13-15, солюбилизаторов в водных растворах – 15-16.
Солюбилизация.
Явление растворения веществ в мицеллах ПАВ называется солюбилизацией. В водных мицеллярных системах солюбилизируются вещества, нерастворимые в воде, например, бензол, органические красители, жиры. Это обусловлено тем, что ядро мицеллы проявляет свойства неполярной жидкости. В органических мицеллярных растворах, в которых внутренняя часть мицелл состоит из полярных групп, солюбилизируются полярные молекулы воды, причем количество связанной воды может быть значительным. Явление солюбилизации подтвердило представление о жидкой природе углеводородного ядра мицеллы ПАВ в водном растворе.
Вещество, солюбилизированное раствором ПАВ, называют солюбилизатом, а ПАВ – солюбилизатором.
Методы определения ккм
Один из методов расчета ККМ основан на определении поверхностного натяжения (см. выше), по методике отрыва кольца (самостоятельно).
По широте применения и точности среди прочих методов определения ККМ особенно выделяется кондуктометрический метод, основанный на измерении электропроводности водных растворов ПАВ.
На кривой концентрационной зависимости эквивалентной электропроводности (λ) водных растворов ПАВ в связи с изменением строения растворов по мере увеличения концентрации четко фиксируются три области (рис. 7а): постепенное линейное снижение электропроводности до ККМ, затем выше ККМ более резкое падение ее до минимума и последующее возрастание электропроводности (на рисунке не изображено).
Коллоидные
ионогенные ПАВ в отношении электропроводности
в разбавленных растворах ведут себя
как обычные электролиты, подчиняясь
уравнению Онзагера (до ККМ):
![]() ,
где λ – эквивалентная проводимость,
,
где λ – эквивалентная проводимость,
![]() –
эквивалентная электропроводность при
бесконечном разбавлении, А – константа,
зависящая от температуры, вязкости и
диэлектрической проницаемости среды.
Понижение эквивалентной электропроводности
до ККМ связано с усилением межионного
взаимодействия.
–
эквивалентная электропроводность при
бесконечном разбавлении, А – константа,
зависящая от температуры, вязкости и
диэлектрической проницаемости среды.
Понижение эквивалентной электропроводности
до ККМ связано с усилением межионного
взаимодействия.
Крутой излом связан с тем, что мицеллы ПАВ хотя и переносят ток, но менее подвижны в электрическом поле. Электропроводность мицеллярных растворов уменьшается вследствии электростатического связывания части противоионов. При этой концентрации начинается формирование ионных мицелл, сопровождающееся образованием облаков из противоионов, связанных с мицеллами. Подвижность поверхностно-активных ионов, общее число и заряд проводящих частиц в системе при этом падают, и электропроводность понижается при возрастании концентрации резче, чем до ККМ. Последующее возрастание электропроводности после минимума на кривой (c) для коллоидных электролитов объясняется освобождением части противоионов в результате перекрывания ионных атмосфер при сближении мицелл и увеличения их размеров с ростом концентрации ПАВ.
|
|
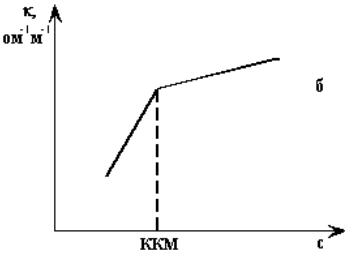
Рис. 8 Зависимость электропроводности от концентрации |
|
Графическая обработка результатов измерений электропроводности водных растворов мыл показывает, что точка излома (ККМ) особенно резко выражена на графике зависимости удельной электропроводности от концентрации. Излом связан с уменьшением электропроводности в связи с образованием мицелл. Начало мицеллообразования вызывает резкий излом кривых (рис. 8б).