
- •По курсу общей физики молекулярная физика термодинамика
- •Введение
- •1. Статистический и термодинамический методы исследования вещества.
- •Тема 1. Основы молекулярно-кинетической теории газов
- •2. Идеальный газ. Параметры состояния идеального газа.
- •3. Основное уравнение кинетической теории газов.
- •4. Средняя кинетическая энергия поступательного движения молекул. Температура. Закон Дальтона.
- •5. Газовые законы. Уравнение Менделеева-Клапейрона.
- •6. Распределение скоростей молекул по Максвеллу.
- •7. Идеальный газ в силовом поле. Барометрическая формула. Закон распределения Больцмана.
- •8. Распределение энергии по степеням свободы.
- •Решение задач по теме 1. Примеры решения задач.
- •Задачи для самостоятельного решения.
- •Тема 2. Явления переноса в газах
- •9. Понятия о явлениях переноса. Средняя длина свободного пробега, эффективный диаметр молекул.
- •10. Диффузия.
- •11. Вязкость (внутреннее трение). Теплопрводность.
- •Тема 3.Основы термодинамики
- •12. Основные термодинамические понятия. Внутренняя энергия термодинамической системы.
- •13. Первое начало термодинамики. Работа, совершаемая газом при изменениях объема.
- •14. Теплоемкость газов. Уравнение Майера. Теплоемкость идеального двухатомного газа.
- •15. Первое начало термодинамики в изопроцессах.
- •16. Адиабатный процесс.
- •17. Круговой процесс. Тепловая машина.
- •18. Второе начало термодинамики. Обратимые и необратимые процессы.
- •19. Цикл Карно.
- •20. Энтропия. Приведенная теплота.
- •21. Изменение энтропии при некоторых процессах.
- •Решение задач по теме 3.
- •Задачи для самостоятельного решения.
- •Тема 4. Реальные газы и жидкости
- •22. Реальные газы. Уравнение Ван-дер-Ваальса.
- •23. Внутренняя энергия реального газа.
- •24. Свойства жидкого состояния вещества.
- •25. Поверхностный слой. Поверхностная энергия. Поверхностное натяжение.
- •26. Явления на границе жидкости и твердого тела.
- •27. Давление под искривленной поверхностью жидкости. Капиллярность.
- •28. Равновесие фаз. Фазовые переходы. Диаграмма состояния.
- •Решение задач по теме 4.
- •Задачи.
- •Ответы.
- •Оглавление.
15. Первое начало термодинамики в изопроцессах.
Для
равновесных изопроцессов в газах
уравнение первого начала термодинамики
(dQ
= dU
+ dА)
имеет вид:
![]() .
.
·
Первое начало термодинамики при
изохорическом процессе (V=const):
![]()
При
этом работа не совершается:
![]()
·
Первое начало термодинамики при
изобарическом процессе (p=const):
![]() .
.
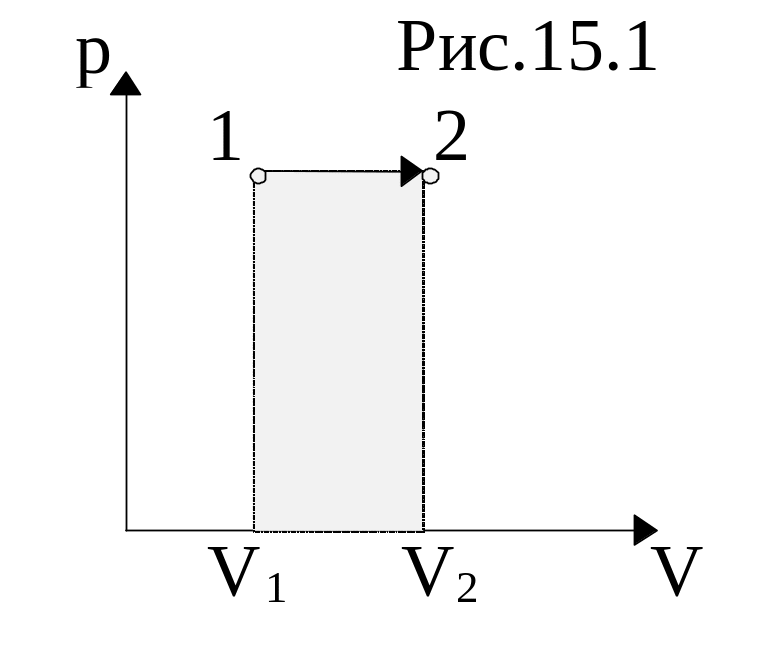
График изобарического процесса представлена на рис.15.1. Работа изобарного расширения равна площади фигуры, заштрихованной на рис. и имеет значение
![]() .
.
Здесь же мы сможем вывести уравнение Майера и сформулировать физический смысл универсальной газовой постоянной.
![]() .
.
Для
изобарического процесса (с учетом
уравнения Менделеева-Клапейрона)
![]() .
Поэтому
.
Поэтому
![]() ,
или
,
или
![]() (уравнение
Майера)
(уравнение
Майера)
Универсальная газовая постоянная численно равна работе, которую необходимо совершить, чтобы нагреть 1 моль вещества на 1 К при постоянном давлении.
·
Первое начало термодинамики при
изотермическом процессе (Т=const):
![]() – теплота, сообщаемая системе при
изотермическом процессе, идет на работу
против внешних сил.
– теплота, сообщаемая системе при
изотермическом процессе, идет на работу
против внешних сил.
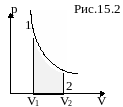
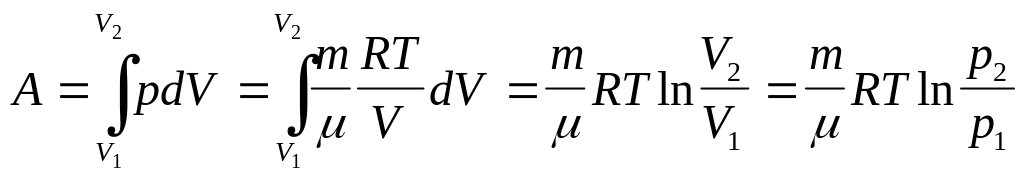 Итак,
работа при изотермическом процессе:
Итак,
работа при изотермическом процессе:
 .
.
Изменение внутренней энергии dU=0, теплоемкость системы равна бесконечности.
Если газ изотермически расширяется (V2>V1), то к нему подводится тепло и он совершает положительную работу, которая измеряется площадью, заштрихованной на рисунке фигуры. Если же газ изотермически сжимается (V2<V1), то он совершает отрицательную работу (то есть над ним совершают работу внешние силы).
16. Адиабатный процесс.
Адиабатным называется процесс, протекающий без теплообмена с внешней средой: dQ=0, Q=0
Чтобы процесс был адиабатным, необходимо, чтобы система была отделена от окружающих тел теплонепроницаемой перегородкой, либо процесс должен быть очень быстро протекающим, причем настолько быстро, чтобы не успел установиться теплообмен.
Из первого закона термодинамики: dA=-dU, то есть работа при адиабатическом процессе совершается за счет убыли внутренней энергии.
Для получения уравнений адиабатного процесса рассмотрим один моль газа, для которого: dA=pdV, dU=CVdT. pdV =CVdT
Учтем,
что p=RT/V
(из уравнения Менделеева-Клапейрона
для 1 моля газа), тогда
![]() ,
или
,
или
![]()
Из уравнения Майера: R=Cp – CV,
тогда
![]() где
где
![]() .
.
![]()
Пусть произошел адиабатный процесс из состояния с параметрами (V1,T1) в состояние с (V2,T2).
Проведем интегрирование с соответствующими пределами::
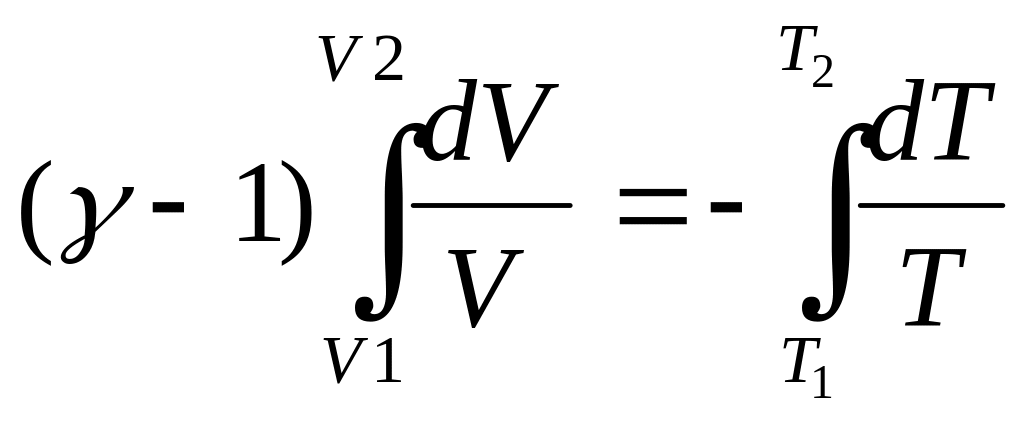 ,
,
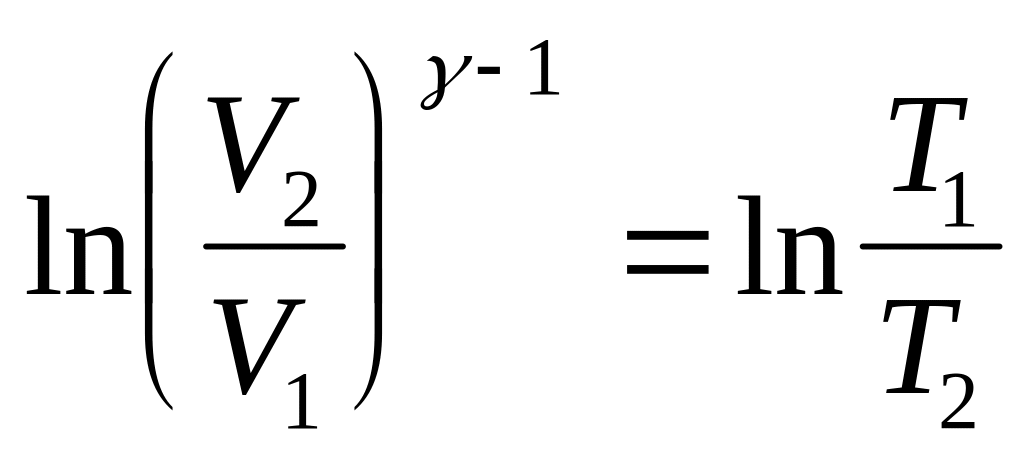 ,
,
![]() .
.
Итак, для адиабатного процесса уравнение состояния:
![]() (1)
(1)
Из уравнения Менделеева-Клапейрона: T=pV/R.
![]() ;
т.е.
;
т.е.
![]() (2)
(2)
Из уравнения Менделеева-Клапейрона: V=RT/p.
![]() ;
;
![]() (3)
(3)
Уравнения (1), (2) и (3) – уравнения адиабатного процесса, названы уравнениями Пуассона.
Работа адиабатического расширения:
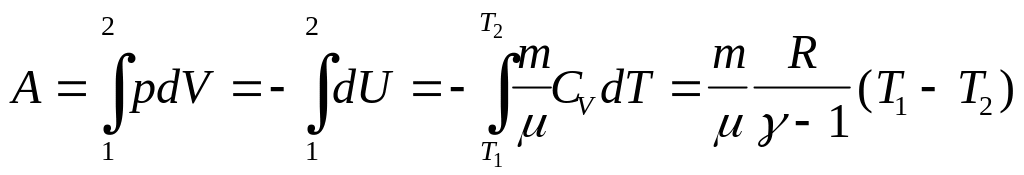
Здесь
мы учли полученное нами из уравнения
Майера соотношение:
![]() откуда
откуда
![]() .
Итак, работа по расширению при адиабатном
процессе:
.
Итак, работа по расширению при адиабатном
процессе:
![]() .
.
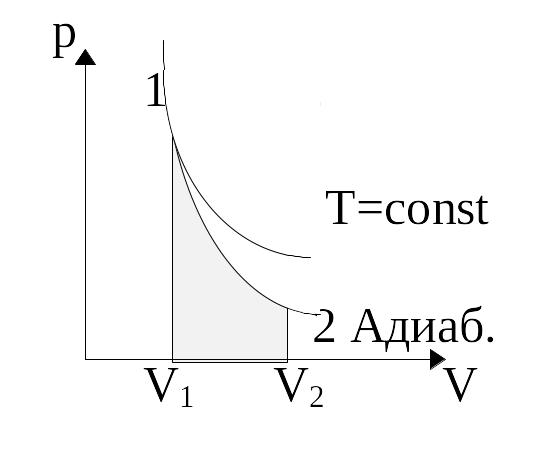 При
сопоставлении адиабатного и изотермического
процессов видно, что адиабата проходит
более круто, чем изотерма: для изотермы
–
pV=const,
для адиабаты
При
сопоставлении адиабатного и изотермического
процессов видно, что адиабата проходит
более круто, чем изотерма: для изотермы
–
pV=const,
для адиабаты
![]() ,
а g>1,
то есть давление при адиабатическом
процессе зависит сильнее. Объяснение
этого факта с молекулярно-кинетической
точи зрения: давление газа обусловлено
дарами молекул о стенки сосуда. При
изотермическом процессе изменяется
число ударов молекул в единицу времени
на единицу площади, а средняя сила ударов
не изменяется. При адиабатном процессе
изменяется и среднее число ударов в
единицу времени, и средняя сила ударов.
,
а g>1,
то есть давление при адиабатическом
процессе зависит сильнее. Объяснение
этого факта с молекулярно-кинетической
точи зрения: давление газа обусловлено
дарами молекул о стенки сосуда. При
изотермическом процессе изменяется
число ударов молекул в единицу времени
на единицу площади, а средняя сила ударов
не изменяется. При адиабатном процессе
изменяется и среднее число ударов в
единицу времени, и средняя сила ударов.
