
- •Выбор области спектра
- •Электрохимические методы Классификация электрохимических методов анализа
- •Электрические параметры химической системы
- •Электрогравиметрия
- •Два варианта электрогравиметрического метода
- •2 Способа внутреннего электролиза:
- •Полярография
- •Полярографический метод основан на явлениях концентрационной поляризации на капельном ртутном электроде, возникающих при прохождении электрического тока через раствор электролита
- •Концентрационная поляризация - связана с уменьшением концентрации восстанавливающихся ионов в прикатодном слое в процессе электролиза
- •Полярографические токи
- •Формула Ильковича
- •Потенциометрический анализ
Лекция 4
КОЛОРИМЕТРИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
Метод анализа, основанный на сравнении качественного и количественного изменения световых потоков при их прохождении через исследуемый и стандартный растворы, называется колориметрическим методом анализа.
Этот анализ называют также абсорбционным спектральным анализом (т.к. он, в сущности, основан на измерении количества света, поглощаемого определяемым веществом), который подразделяется на спектрофотометрический и фотометрический.
Сущность колориметрических определений состоит в следующем: определяемый компонент (простой ион, сложный ион, органическое соединение) при помощи химической реакции переводят в окрашенное соединение, после чего каким – либо способом измеряют интенсивность окраски.
Основные оптические свойства растворов окрашенных соединений
При прохождении пучка белого света с интенсивностью I0 через стеклянный сосуд, заполненный раствором, происходит ослабление этого первоначального потока света, и выходящий из сосуда поток света будет иметь интенсивность I<I0. Ослабление светового потока связано с
- отражением на границах стекло – воздух и стекло - раствор Iотр
- рассеянием света, вызываемым присутствующими в растворе частицами Iр
- поглощением (абсорбцией) световой энергии раствором Iа
I0 = Ia + Iотр + Iр + I
I0 = Ia + I
Интенсивность падающего и прошедшего светового потока можно измерить.
Степень поглощения светового потока жидкостью не одинакова для различных длин волн, составляющих белый цвет. В результате этого выходящий свет часто бывает окрашен. Цвет раствора, который воспринимается глазом, обусловлен светом той части падающего пучка света, которая прошла через раствор не поглощенной.
Таким образом, основными оптическими характеристиками растворов окрашенных соединений в колориметрии являются ИНТЕНСИВНОСТЬ ОКРАСКИ и ЦВЕТ раствора.
Падающее на вещество электромагнитное излучение характеризуется спектром—набором длин волн в определенной последовательности. Длины волн λ связаны с частотой излучения (ν):
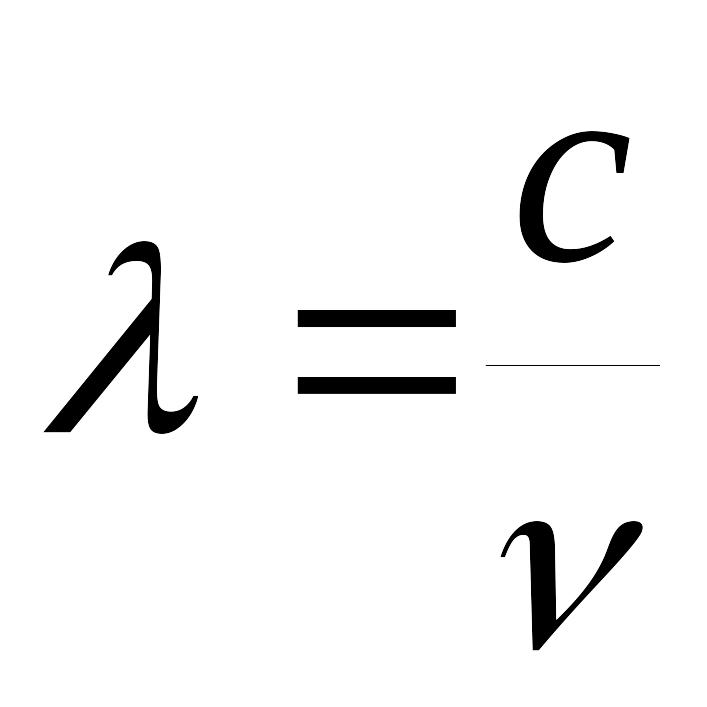
где с—скорость света, равная 3*108 м/с.
Ниже приведены характеристики областей электромагнитного излучения:
Области электромагнитного излучения
Область |
λ, нм |
ν, с-1 |
Радиоволновая |
>400 000 |
<1012 |
Инфракрасная (ИК.) |
700 – 400 000 |
1015 - 1012 |
Видимая |
315 - 700 |
4*1014 – 7*1014 |
Ультрафиолетовая (УФ) |
10 - 315 |
7*1014 – 3*1016 |
Рентгеновская |
<10 |
>3*1016 |
Интенсивность поглощения веществом электромагнитного излучения (интенсивность окраски) выражается величиной ОПТИЧЕСКОЙ ПЛОТНОСТИ D.
Закон Бугера - Ламберта
Слои данного вещества одинаковой толщины, при прочих равных условиях, всегда поглощают одну и ту же часть падающего на них светового потока, или оптическая плотность вещества прямо пропорциональна толщине поглощающего слоя.
Закон Бера
При прохождении света через газы и растворы веществ степень поглощения света зависит от числа частиц в единице объема, встречающихся на пути светового потока, т.е. поглощение света зависит от концентрации вещества.
Оптическая плотность пропорциональна концентрации вещества и толщине поглощающего слоя. Эта зависимость выражается законом Бугера— Ламберта —Бера:
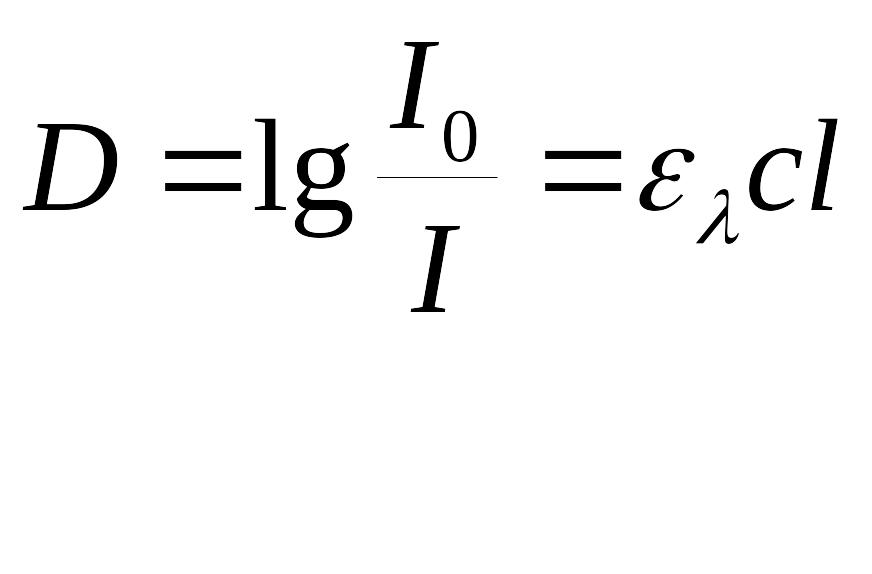
где I0 , I - интенсивность света до и после его прохождения через вещество;
ελ - молярный коэффициент поглощения, характеристическая постоянная вещества;
С—концентрация вещества, моль/дм3;
l—толщина поглощающего слоя, см;
D—экстинкция (оптическая плотность раствора).
Если D1=D2 , то εС1l1 = εС2l2 отсюда
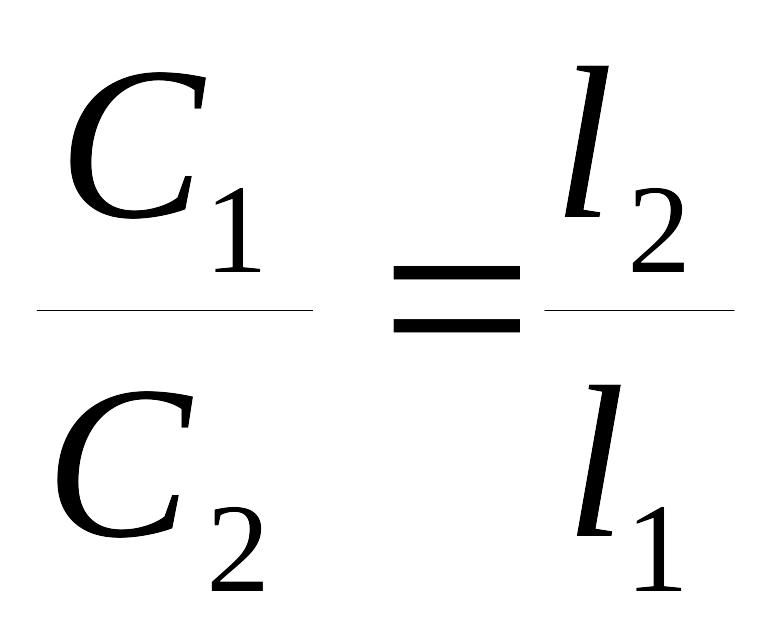
При одинаковой интенсивности окраски двух растворов данного вещества их концентрации обратно пропорциональны толщинам поглощающих слоев.
Отношение τ=I/Io характеризует пропускание (прозрачность раствора). Величина τ может меняться от 0 до 100%.
I0/I – непрозрачность или поглощение раствора
Величина D характеризует поглощение света и может принимать значения от 0 до ∞ (практически D измеряется в интервале от 0 до 3). Оптическая плотность является десятичным логарифмом непрозрачности.
Молярный коэффициент поглощения (погашения) служит мерой поглощательной способности вещества при данной длине волны. Величина ε не зависит от концентрации, толщины слоя и интенсивности падающего света, зависит от длины волны падающего света и природы окрашенного соединения. ε является важной характеристикой чувствительности определения.
Численное значение молярного коэффициента поглощения равно оптической плотности такого раствора, концентрация которого равна 1 моль/л при толщине поглощающего слоя в 1см.
Чем больше величина молярного коэффициента поглощения, тем выше чувствительность колориметрического анализа.
Длину волны, соответствующую максимуму светопоглощения принято обозначать λmax.
Наибольшая величина молярного коэффициента поглощения, а, следовательно, и наибольшая чувствительность определения, соответствует максимуму светопоглощения.
D
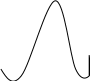

 λ
λ
λmax1 λmax2
Рисунок 4.1 - График зависимости D от λ
Закон Бэра наиболее строго выполняется для монохроматического излучения; но и полихроматический свет (выделенный светофильтрами) зачастую пригоден для колориметрических определений.
На величину отклонения от закона влияет ряд факторов:
1. Прочность комплексных соединений, характеризуемая константой диссоциации (константой нестойкости).
Х +nR=ХRn
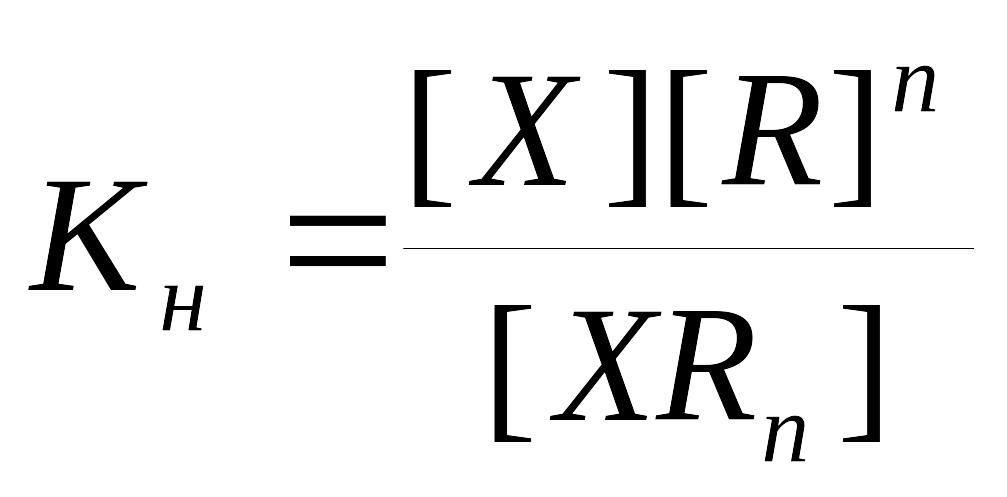 рКн=
-lgКн
рКн=
-lgКн
2. Присутствие посторонних комплексообразующих ионов. В этом случае возможны параллельные реакции. (если КХА<К ХR значит комплекс с примесью А прочнее; определить комплекс с реактивом R невозможно). Примесь следует удалять.
3. Влияние концентрации водородных ионов.
Фотометрические методы анализа
Фотометрическими методами анализа называют группу методов, в которых определение концентрации веществ основано на измерении взаимодействия электромагнитного излучения с анализируемым веществом.
Наиболее распространенным из них является молекулярно-абсорбционный анализ по спектрам поглощения молекул, к которому относятся: колориметрия, фотоэлектроколориметрия, спектрофотометрия.
Измерительные системы. Для измерения светопоглощения используют различные приборы (колориметры, фотоэлектроколориметры, спектрофотометры). Они построены по следующей общей схеме:
Источник сплош-ного
излучения
моно-хроматор
Анализируемый
раствор
Приемник излучения
Измерительное
устройство

Выбор области спектра
Спектр поглощения каждого вещества графически представляет собой сложную кривую. Каждая полоса поглощения (пик на рисунке) имеет в максимуме определенное значение молярного коэффициента поглощения ελ. Измерения следует проводить в участках спектра, отвечающих максимальному значению величины ελ. (ελ1, ελ2).
Это достигается монохроматизацией падающего светового потока, т. е. выделением из сплошного спектра узкого участка. Чем выше степень монохроматизации, тем с большей точностью можно измерить величину молярного коэффициента поглощения и, следовательно, тем точнее определить концентрацию вещества.
В качестве монохроматоров часто используют светофильтры — избирательные поглотители света, представляющие собой окрашенные стекла или специальные окрашенные растворы.
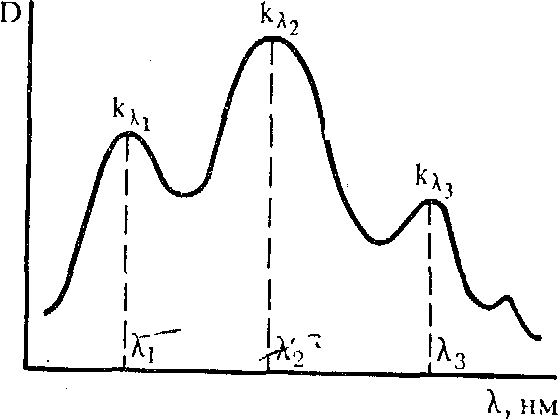
Спектр поглощения вещества
Зависимость
оптической плотности от длины волны
излучения для различных концентраций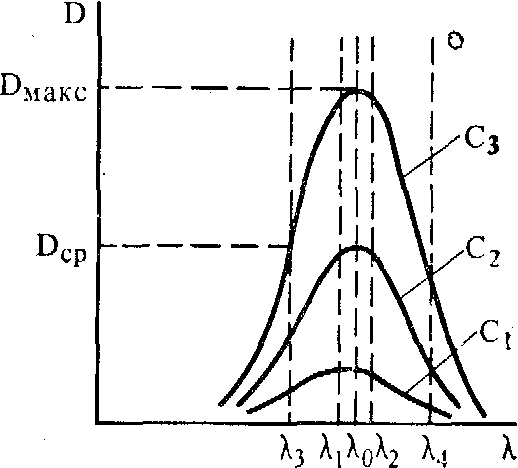
Область максимального поглощения лучей характеризуется также размытостью максимума поглощения, отвечающим половинным значениям εмакс или 1/2Dмакс.
Положение максимума спектра является важной оптической характеристикой вещества, а характер и вид спектра характеризуют его качественную индивидуальность.
Выбор светофильтра основан на следующей зависимости спектров поглощения и пропускания: максимум спектра поглощения определяемого вещества должен совпадать с максимумом пропускания (минимумом поглощения) светофильтра.
Более совершенна монохроматизация с помощью призм и дифракционных решеток. При этом в качестве аналитической можно использовать любую полосу спектра поглощения вещества, свободную от наложения со стороны полос других веществ, присутствующих в растворе, и по возможности с большим молярным коэффициентом поглощения.
τ
Рисунок 4.2 -
Спектральные характеристики светофильтра
(2) и
исследуемого раствора (1)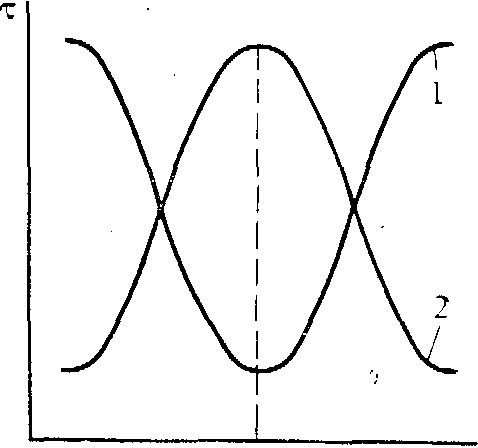
λ, нм
Лекция 5 (1 час)
Методы определения концентрации
В фотометрических методах анализа могут быть использованы все способы определения концентрации.
Метод уравнивания. Сравнение с эталоном наиболее часто используется в визуальной колориметрии. В строго одинаковых условиях готовят эталонный раствор и анализируемый. На колориметре погружения (Дюбоска) при одном и том же светофильтре измеряют толщины слоев, при которых наблюдается одинаковая интенсивность окраски. Неизвестная концентрация определяется, по формуле
![]()
Метод стандартных серий. Готовят серию эталонных растворов и в тех же условиях подготавливают анализируемый раствор. Сравнивают интенсивность окраски анализируемого раствора с эталонной серией. Концентрация Сх принимается равной концентрации эталонного раствора, одинакового с ним по интенсивности окраски.
Метод градуировочного графика. В фотоэлектроколориметрии и спектрофотометрии измеряют на соответствующем приборе оптические плотности серии эталонных растворов и анализируемого раствора. Строят градуировочный (калибровочный) график D=f(C), по которому находят искомую концентрацию Сх.
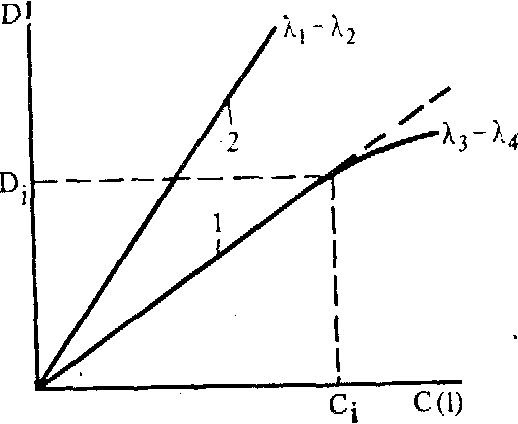
Метод добавок. Применяется в фотоэлектроколориметрии и спектрофотометрии. Измерив предварительно оптическую плотность исследуемого раствора (Dx), прибавляют к нему известное количество определяемого вещества (Сэт) и снова измеряют оптическую плотность (Dx+эт). Неизвестную концентрацию (Сх) находят по формуле
![]()
или графически.
Титрование. Колориметрическое титрование заключается в том, что к дистиллированной воде или специально подготовленному раствору, не содержащему определяемого элемента, прибавляют из бюретки стандартный раствор определяемого вещества до тех пор, пока интенсивность окраски не сравняется с интенсивностью окраски анализируемого раствора. При этом принимают Сх = Сэт..
Разновидностью является метод разбавления. Готовят в одинаковых условиях эталонный и анализируемый раствор. Раствор, окрашенный более интенсивно, разбавляют до тех пор, пока интенсивности окрасок обоих растворов станут одинаковыми. Измеряют объемы эталонного (Vст) и анализируемого (Vx) растворов:
![]()
где Сст—массовая концентрация.
При спектрофотометрическом титровании измеряют изменение оптической плотности D в процессе титрования и строят график в координатах D—С.
Правила проведения фотометрических анализов.
Исследуемый и эталонные растворы готовят одновременно, прибавляя реагенты в одной и той же последовательности и в одних и тех же количествах.
. Измерения проводят в течение небольшого интервала времени.
. Интенсивность окрасок исследуемого и эталонных растворов сравнивают в одинаковых сосудах и при одинаковом освещении, при визуальном колориметрировании—на фоне матового стекла или белой бумаги в светлой комнате с рассеянным светом.
. Предпочтительно работать с тонкими поглощающими слоями.
Минимальная ошибка наблюдается в интервале 0,3 - 0,7 единиц оптической плотности; при измерении меньших и больших оптических плотностей ошибки измерения возрастают. Наименьшая ошибка измерения соответствует D = 0,434 (светопропускание 36.8%) (доказано экспериментально и теоретически).
Фотометрические методы – спектрофотометрия и фотоколориметрия – относятся к методам абсорбционной спектрометрии, основаны на избирательном поглощении (абсорбции) света анализируемым раствором. Эти методы отличаются применяемой аппаратурой.
Спектрофотометрия основана на поглощении монохроматического излучения, или точнее света в очень узком интервале длин волн (1 –2 нм).
Аппаратурой являются спектрофотометры, позволяющие работать как с окрашенными, так и с неокрашенными растворами, поглощающими излучение в ультрафиолетовой, видимой или ближней инфракрасной областях спектра.
Фотоколориметрия основана по поглощении анализируемым раствором
полихроматического света. Аппаратура представляет собой фотоэлектроколориметры, снабженные светофильтрами, выделяющими свет в достаточно узком интервале длин волн. Для наиболее узкополосных светофильтров современных фотоэлектроколориметров ширина области пропускания составляет 20 – 30 нм.
Колориметрический анализ основан на определении концентрации элемента по интенсивности окраски раствора, оценку которой производят или визуально путем сравнения с эталонным раствором, или с помощью простых оптических приборов (фотометров или колориметров).
Фотоколориметры (КФК, ФЭК)
Приборы, в которых фотоэлементы используют для целей колориметрического анализа называются фотоэлектрическими колориметрами (фотоколориметрами ).
На ФЭКах определяются практически все тяжелые цветные металлы. Выделяемая область спектра достаточно широкая (315 – 630нм). Измеряют пропускание или оптическую плотность растворов и определяют концентрацию веществ. Также производят относительные измерения интенсивности рассеяния взвесей и коллоидных растворов в проходящем свете.
Измеряют пропускание от 100 до 5% (D= 0 - 1,3).
Источник света - лампа накаливания (6,3В, 15 Вт); узкополосные светофильтры.
ФЭКи делятся на
фотоколориметры с 1 фотоэлементом (однолучевые)
фотоколориметры с 2 фотоэлементами (двулучевые).
Спектрофотометры
Измеряют пропускание и D растворов и твердых веществ в диапазоне 180 – 1100нм.
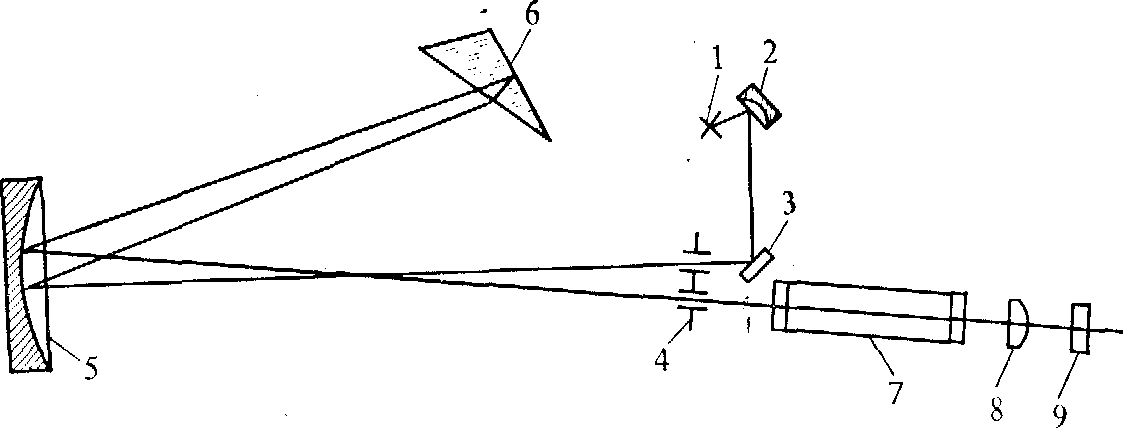
1—источник излучения (лампа); 2, 3— зеркала; 4 — щель монохроматора;
5—зеркальный объектив; 6—диспергирующая призма; 7—кювета; 8—линза;
9—фотоэлемент
Рисунок 4.3 - Оптическая схема спектрофотометра:
ИК – спектрометрия
Молекула имеет квантовые энергетические уровни, и ее энергия состоит из энергии электронного, колебательного и вращательного состояний
Е = Еэл + Екол + Евр.
Поглощение излучения вызывает изменение в энергии этих состояний, в результате чего возникают электронные, колебательные и вращательные спектры.
Вращательным спектрам соответствует энергия перехода порядка
10-2 – 10-3ккал/моль, и они находятся в далекой ИК и микроволновой областях.
Колебательные спектры связаны с изменением колебательной энергии и для большинства молекул проявляются в средней и ближней ИК областях (1 – 40 мк) (2 – 50 мк). Соответствующая энергия переходов составляет 1 –10 ккал/моль. Эта область исследуется методом ИК-спектроскопии).
Электронные спектры возникают в результате переходов между электронными состояниями и наблюдаются в ультрафиолетовой, видимой и ближней ИК областях (120 – 1000нм). При поглощении такой энергии одновременно происходит изменение в колебательном и вращательном состояниях.
Для ИК области спектра отклонения от закона Бера встречаются чаще. Это вызвано тем, что при измерении спектров поглощения веществ в ИК области используются концентрированные растворы, межмолекулярные взаимодействия в которых достаточно сильны.
В ИК области спектра запись производится обычно в процентах пропускания или процентах поглощения.
Спектр поглощения характеризуется следующими величинами:
длинами волн максимумов поглощения и интенсивностью в этих максимумах;
длинами волн в минимумах кривой поглощения и интенсивностью в этих точках
длинами волн, отвечающих перегибам кривой поглощения, и интенсивностью для этих точек.
ИК-спектроскопией определяются структура органические соединения, углеводороды, металлорганические соединения. В области колебаний с волновым числом (ν=1/λ) 1500 – 700 см-1, характер спектра в этом интервале существенно изменяется даже при небольших изменениях в структуре соединения. Это используется для идентификации, поскольку каждое вещество имеет только ему присущий набор полос поглощения. Эта область называется областью «отпечатков пальцев».
Валентные, деформационные (маятниковые, ножничные, веерные) колебания. Каждому колебанию соответствует свое волновое число.
Икспектрометр состоит из источника излучения, щели, диспергирующего элемента (призмы, дифракционные решетки), приемника и различных зеркал.
Лекция 5 (1 час)
