
11 himpopel p u
.pdf219. Яким об'ємом води потрібно розбавити 150 мл оцтової есенції (розчин оцтової кислоти з її масовою часткою 70 % і густиною 1,07 г/см3), щоб виготовити розчин із масовою часткою оцтової кислоти 5 %?
220. У суміш мурашиної та оцтової кислот масою 8,3 г добавили достатню кількість питної соди. При цьому виділилося 3,36 л газу (н. у.). Визначте масові частки кислоту суміші. Вважайте, що газ не розчиняється в рідині.
ПРАКТИЧНА РОБОТА № 2
Властивості етанової (оцтової) кислоти
Д О С Л І Д 1
Порівняння етанової та хлоридної кислот
за їх здатністю до дисоціації
З а н у р т е с к л я н у |
п а л и ч к у в |
п р о б і р к у |
з р о з б а в л е н и м розчи - |
||||
ном |
етанової к и с л о т и |
і н а н е с і т ь |
його |
к р а п л ю на |
у н і в е р с а л ь - |
||
н и й |
і н д и к а т о р н и й |
п а |
п і р е ц ь . |
Те |
с а м е |
в и к о н а й т е |
з розбавле - |
н о ю х л о р и д н о ю к и с л о т о ю . З і с т а в т е з а б а р в л е н н я і н д и к а т о р а і зробіть в і д п о в і д н и й в и с н о в о к .
Н а п и ш і т ь р і в н я н н я електролітичної дисоціації кислот .
Д О С Л І Д 2
Реакція етанової кислоти з металом
У пробірку помістіть н е в е л и к у к і л ь к і с т ь п о р о ш к у або с т р у ж - ки м а г н і ю і добавте 1 — 2 мл р о з ч и н у етанової к и с л о т и . Що відбувається?
Д О С Л І Д З
Реакція етанової кислоти з основним (амфотерним) оксидом
У п р о б і р к у помістіть н е в е л и к у к і л ь к і с т ь м а г н і й о к с и д у ( ц и н к оксиду) і добавте 1—2 мл р о з ч и н у етанової к и с л о т и . Що спостерігаєте? За потреби нагрійте вміст пробірки .
.178
ДОСЛІД 4
Реакція етанової кислоти з розчином амоніаку1
У п р о б і р к у н а л и й т е 1 мл р о з б а в л е н о г о р о з ч и н у а м о н і а к у і добавте 1 — 2 к р а п л і р о з ч и н у ф е н о л ф т а л е ї н у . Щ о спостеріга - є т е ? Д о б а в л я й т е в п р о б і р к у п о к р а п л я х р о з ч и н е т а н о в о ї к и с л о т и . Я к і з м і н и в і д б у в а ю т ь с я в п р о б і р ц і ?
ДОСЛІД 5
Реакція етанової кислоти з нерозчинною основою (амфотерним гідроксидом)
У п р о б і р к у н а л и й т е 1 мл |
р о з ч и н у л у г у і добавте н е в е л и к у |
к і л ь к і с т ь р о з ч и н у нікель(ІІ) |
с у л ь ф а т у ( ц и н к с у л ь ф а т у ) . Щ о |
спостерігаєте? |
|
Д о л и й т е до утвореного осаду 2 мл р о з ч и н у етанової к и с л о т и . Я к і з м і н и в і д б у л и с я в пробірці?
ДОСЛІД 6
Реакції етанової кислоти із солями
В одну п р о б і р к у н а л и й т е 1 мл р о з ч и н у н а т р і й к а р б о н а т у , а в і н ш у — с т і л ь к и само р о з ч и н у н а т р і й г і д р о г е н к а р б о н а т у . В оби-
дві п р о б і р к и д о л и й т е п о 1 — 2 |
м л р о з ч и н у етанової к и с л о т и . Щ о |
спостерігаєте? |
|
Р е з у л ь т а т и е к с п е р и м е н т і в |
внесіть у т а б л и ц ю : |
Послідовність дій |
|
Спостереження |
|
Висновки |
|
|
|
|
|
Дослід 1. ... |
|
|
|
|
|
|
|
||
|
|
|
|
|
Р і в н я н н я реакції (реакцій) у м о л е к у л я р н і й |
і йонно- |
|||
молекулярній формах: |
|
|
|
|
|
|
|
|
|
1 Замість водного розчину амоніаку можна взяти розчин лугу.
.179

в
221. Із якою метою в досліді 4 використовують індикатор?
222. Якими будуть результати досліду 6, якщо замість указаних солей взяти барій карбонат, барій сульфат? Відповідь обґрунтуйте.
223. Чи знебарвиться розчин калій перманганату після добавляння до нього оцтової кислоти?
Вищі карбонові кислоти.
Мила і синтетичні мийні
засоби
Матеріал параграфа допоможе вам:
отримати відомості про вищі карбонові кислоти; дізнатися про сполуки, які виявляють мийну дію; з'ясувати, чим різняться мила і синтетичні мийні засоби.
Вищі карбонові кислоти. Серед |
в и щ и х кар - |
||
бонових |
к и с л о т н а й в а ж л и в і ш и м и |
є насичені |
|
к и с л о т и |
— п а л ь м і т и н о в а С1 5 Н3 1 СООН і стеа- |
||
ринова |
С1 7 Н3 5 СООН, |
а т а к о ж ненасичена — |
|
олеїнова С]7 Н3 3 СООН. |
М о л е к у л и |
ц и х к и с л о т |
|
м а ю т ь н е р о з г а л у ж е н у будову (мал . |
78). |
||
Мал. 78. Кулестержневі моделі молекул стеаринової (а) і олеїнової (б) кислот
.180
В и щ і к а р б о н о в і к и с л о т и р а н і ш е д о б у в а л и т і л ь к и з р о с л и н н и х і т в а р и н н и х ж и р і в . Т о м у
їх ще називають жирними кислотами.
П а л ь м і т и н о в а і с т е а р и н о в а к и с л о т и — тверді р е ч о в и н и білого к о л ь о р у , а олеїнова — ріди - н а . В о н и п р а к т и ч н о не р о з ч и н я ю т ь с я у воді.
З а х і м і ч н и м и в л а с т и в о с т я м и в и щ і карбоно - ві к и с л о т и подібні до оцтової, а л е є д у ж е слаб- к и м и . Ц і с п о л у к и р е а г у ю т ь і з л у г а м и :
С 1 7 Н3 5 СООН + К а О Н -> С 1 7 Н 3 5 С О ( Ж а + Н 2 0 .
стеаринова кислота натрій стеарат
Я к щ о до розчину солі вищої карбонової кисло - ти добавити розбавлену сульфатну кислоту, то відбувається р е а к ц і я обміну:
2С1 5 Н3 1 СООК + Н 2 8 0 4 |
-> 2С 1 5 Н 3 1 СООН^ + К 2 8 0 4 . |
калій пальмітат |
пальмітинова кислота |
Олеїнова к и с л о т а є н е н а с и ч е н о ю с п о л у к о ю і т о м у вступає в р е а к ц і ї п р и є д н а н н я з галогена -
м и , г а л о г е н о в о д н я м и , воднем: |
|
|
|||
С 1 7 Н 3 3 СООН + |
|
С 1 7 Н 3 5 СООН, |
|
||
або |
|
|
|
|
|
С Н 3 - ( С Н 2 ) 7 - С Н = С Н - ( С Н 2 ) 7 - С О О Н + Н2 |
* - т |
> |
|||
|
олеїнова кислота |
|
|
|
|
- > С Н 3 - ( С Н 2 ) 7 - С Н 2 - С Н 2 - ( С Н 2 ) 7 - С О О Н . |
|
||||
|
стеаринова кислота |
|
|
||
К р і м того, олеїнова |
к и с л о т а о к и с н ю є т ь с я |
ка - |
|||
л і й п е р м а н г а н а т о м , і н ш и м и о к и с н и к а м и . |
|
||||
В и щ і к а р б о н о в і |
к и с л о т и д о б у в а ю т ь , |
здій- |
|||
с н ю ю ч и |
з а п е в н и х |
умов |
р е а к ц і ї п р и р о д н и х |
||
ж и р і в із |
водою, а т а к о ж |
о к и с н е н н я м високо - |
|||
м о л е к у л я р н и х в у г л е в о д н і в н а ф т и . |
|
|
|||
М и л а . Солі л у ж н и х елементів і карбонових |
|||||
к и |
с л о т із к і л ь к і с т ю атомів Карбону в аніоні від |
10 |
до 20 н а з и в а ю т ь милами. ( Я к щ о атомів Кар - |
бону в аніоні солі |
м е н ш е 10, то сполука не |
ви- |
|
я в л я є м и й н о ї дії, |
а я к щ о більше 20, то |
сіль |
|
п р а к т и ч н о нерозчинна у воді.) Натрієві солі |
є |
||
твердими речовинами, а к а л і й н і — р і д и н а м и . |
|
||
Т р а д и ц і й н и й процес м и л о в а р і н н я п о л я г а є |
в |
||
нагріванні ж и р і в або олій з лугом . У результаті
.181
у т в о р ю є т ь с я |
однорідна т я г у ч а р і д и н а . |
П р и |
д о б а в л я н н і до |
неї насиченого розчину кухон - |
|
ної солі розчинність м и л а з м е н ш у є т ь с я ; |
воно |
|
в и д і л я є т ь с я з розчину і спливає на поверхню .
Ц е й |
процес н а з и в а ю т ь |
висолюванням. |
М и л о |
||
з б и р а ю т ь і з а п о в н ю ю т ь |
н и м |
ф о р м и , де |
воно |
||
твердне. З а л е ж н о |
від сорту |
м и л а в нього під |
|||
час |
в и г о т о в л е н н я |
д о б а в л я ю т ь б а р в н и к и , |
аро- |
||
м а т и з а т о р и , е к с т р а к т и р о с л и н ( к а л е н д у л и , л и п и , р о м а ш к и т а ін.).
Мийна дія мила полягає у відокремленні
часточок |
бруду, |
н а п р и к л а д , від поверхні тка - |
||
н и н и , й |
утворенні |
емульсії чи суспензії. Роз- |
||
г л я н е м о , |
я к ц е |
відбувається . |
||
• П р и г а д а й т е , що |
т а к е |
емульсія, суспензія . |
||
П о т р а п л я ю ч и |
у |
воду, |
м и л о р о з ч и н я є т ь с я і |
|
частково взаємодіє з нею . Це — р е а к ц і я гідро- л і з у . П і д ч а с г і д р о л і з у м и л а у т в о р ю ю т ь с я слабка к и с л о т а і с и л ь н а основа (луг):
С1 7 Н3 5 СОСШа + Н 2 0 <± С1 7 Н3 5 СООН + МаОН, С1 7 Н3 5 СОО" + Н 2 0 <± С1 7 Н3 5 СООН + ОН".
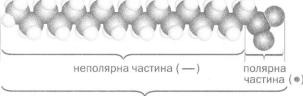
Аніон С17Н35СОО~ складається із двох частин — п о л я р н о ї ( - СОО ) і неполярної (С 1 7 Н 3 5 - ) (мал . 79):
Н Н Н Н Н Н Н Н Н Н Н Н Н Н Н Н Н
ІІ І І І І І І І І І І І І І І І л0>
н-сІ -сі -сі -сі-сі-сі-сІ-сІ-сІ-сі-сі-сІ-с-І с-І с-іс-іс-іс(~о
НН Н Н Н Н Н Н Н Н Н Н Н Н Н Н Н
Мал. 79. Масштабна модель аніона вищої карбонової кислоти
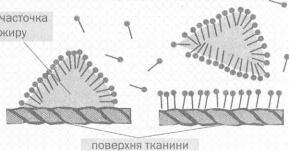
Н е п о л я р н а ч а с т и н а йона « р о з ч и н я є т ь с я » в ж и р о в і й с к л а д о в і й з а б р у д н е н н я , а п о л я р н а з а л и ш а є т ь с я у воді (мал . 80), с п о л у ч а ю ч и с ь із 'її молекулами водневими з в ' я з к а м и . Унаслідок
аніон вищої карбонової кислоти ( — • )
.182
т а к ої |
взаємодії |
з а б р у д н е н н я в і д о к р е м л ю є т ь с я |
||||||
від |
п о в е р х н і |
т к а н и н и |
р а з о м і з |
а н і о н а м и |
||||
к и с л о т и у |
в и г л я д і |
м а л е н ь к и х |
ж и р о в и х |
крап - |
||||
л и н о к або |
твердих |
часточок . |
Вони |
не |
злипа - |
|||
ю т ь с я , о с к і л ь к и |
м а ю т ь |
н а |
своїй |
п о в е р х н і |
||||
о д н о й м е н н и й з а р я д ( я к и й ? ) , а з б и р а ю т ь с я н а в к о л о б у л ь б а ш о к повітря в піні.
водний розчин мила
Мал. 80.
Мийна дія мила:
.і — сполучення
.ініонів із часточкою жиру;
б — відокремлення часточки жиру від тканини
В и к о р и с т а н н я м и л а має певні н е д о л і к и . Л у г , н е в е л и к а к і л ь к і с т ь я к о г о у т в о р ю є т ь с я у
водному р о з ч и н і м и л а , повільно роз'їдає тка - |
||
н и н и , р у й н у є д е я к і б а р в н и к и . |
М и л о втрачає |
|
свої властивості у твердій |
воді, |
бо й о н и К а л ь - |
цію і Магнію, що м і с т я т ь |
с я в ній, у т в о р ю ю т ь |
|
з а н і о н а м и ж и р н и х к и с л о т м а л о р о з ч и н н і солі:
Са2+ + 2С1 7 Н3 5 СОО |
|
(С1 7 Н3 5 СОО)2 СаІ. |
||||||
М и л а н а л е ж а т ь |
до |
поверхнево активних |
||||||
речовин |
(скорочено |
— |
П А Р ) . |
Це |
група |
орга- |
||
н і ч н и х |
с п о л у к , |
м о л е к у л и |
або |
й о н и |
я к и х |
|||
м і с т я т ь п о л я р н і групи |
атомів |
різного с к л а д у і |
||||||
н е п о л я р н і |
довгі карбонові л а н ц ю г и . |
|
||||||
Усі П А Р |
с п р и я ю т ь |
ш в и д к о м у з м о ч у в а н н ю |
||||||
водою забруднених поверхонь, відокремлен - ню від н и х часточок бруду і п о т р а п л я н н ю їх у р о з ч и н м и й н о г о засобу.
Синтетичні мийні засоби. Н и н і м и л а посту-
пово в и т і с н я ю т ь с я |
с и н т е т и ч н и м и |
м и й н и м и |
засобами (скорочено |
— СМЗ), я к і |
позбавлені |
.183

в и щ е з г а д а н и х недоліків 1 (мал . 81). Основу С М З с т а н о в л я т ь поверхнево- а к т и в н і речовини . У н и х є т а к о ж різні добавки — вибілювачі (хіміч-
ні, о п т и ч н і ) , а р о м а т и з а т о р и , |
по- |
м ' я к ш у в а ч і води, а н т и с т а т и к и , |
дез- |
і н ф е к ц і й н і речовини тощо . До скла - д у б а г а т ь о х С М З в х о д я т ь к і л ь к а
п о в е р х н е в о - а к т и в н и х речовин, |
я к і |
за в л а с т и в о с т я м и доповнюють |
одна |
одну. Вміст П А Р р і з н и х типів у ц и х засобах сягає в середньому 35 % за масою.
ЛАБОРАТОРНИЙ ДОСЛІД № 12
Порівняння властивостей мила і СМЗ
Н а л и й т е в о д н у п р о б і р к у 2 мл в о д н о г о р о з ч и н у м и л а ( к р а щ е — господарського), а в д р у г у — с т і л ь к и само р о з ч и н у п р а л ь н о г о п о р о ш к у . В и п р о б у й т е р о з ч и н и у н і в е р с а л ь н и м и і н д и к а т о р н и м и п а п і р ц я м и . Я к е с е р е д о в и щ е в о д н и х р о з ч и н і в м и л а , п р а л ь н о г о п о р о ш к у ?
У к о ж н у п р о б і р к у д о л и й т е по 1 мл р о з ч и н у м а г н і й с у л ь ф а т у
або к а л ь ц і й |
х л о р и д у . Щ о спостерігаєте? |
|
|
|
П о я с н і т ь |
р е з у л ь т а т и досліду . Н а п и ш і т ь |
р і в н я н н я |
р е а к ц і й з а |
|
участю м и л а , в в а ж а ю ч и його натрій стеаратом . |
|
|||
|
І з в и к о р и с т а н н я м С М З |
п о в ' я з а н і |
певні еко- |
|
|
л о г і ч н і п р о б л е м и . |
Сучасні п р а л ь н і |
п о р о ш к и і |
|
|
р і д к і м и й н і засоби |
м і с т я т ь д о с и т ь с т і й к і речо- |
||
|
в и н и . ї х з а л и ш к и р а з о м з і с т і ч н и м и в о д а м и |
|||
|
п о т р а п л я ю т ь у р і ч к и , в о д о й м и , ґ р у н т , н а к о - |
|||
|
п и ч у ю т ь с я в н и х і н е г а т и в н о в п л и в а ю т ь на |
|||
|
ж и в у п р и р о д у . У |
д е я к и х |
С М З м і с т я т ь с я фос- |
|
|
ф а т и . Н а д х о д ж е н н я ї х у в о д у с п р и ч и н я є |
|||
|
і н т е н с и в н е р о з м н о ж е н н я |
водоростей, я к і зго- |
||
|
дом в і д м и р а ю т ь , г н и ю т ь , |
а вода з б і д н ю є т ь с я |
||
1 Такі речовини ще називають детергентами. Термін походить від англійського слова сіеіег^епі; — мийний засіб.
.184
н а к и с е н ь , н е о б х і д н и й р и б а м т а і н ш и м м е ш - к а н ц я м р і ч о к і озер .
Д о С М З с т а в л я т ь н и з к у в и м о г . В о н и м а ю т ь добре р о з ч и н я т и с я у воді, зберігати змочу - в а л ь н у та м и й н у д і ю у твердій і м о р с ь к і й воді, бути е к о л о г і ч н о б е з п е ч н и м и і н е т о к с и ч н и м и . Х і м і к и п р а ц ю ю т ь н а д с т в о р е н н я м т а к и х С М З ,
я к і |
б |
ш в и д к о р о з к л а д а л и с я в п р и р о д н и х умо - |
|||
вах |
і |
не з а в д а в а л и |
ш к о д и д о в к і л л ю . |
||
ВИСНОВКИ |
|
|
' |
||
Найважливішими вищими карбоновими кислотами є пальмітинова, стеаринова і олеїнова. Це дуже слабкі кислоти. їх натрієві та калійні солі називають милами.
Мило частково реагує з водою; при цьому утворюються відповідні кислота і луг.
Мила належать до поверхнево-активних речовин (ПАР). Наявність полярної й неполярної частин у молекулах ПАР зумовлює змочування їхніми розчинами різних поверхонь і видалення з них забруднень.
Синтетичні мийні засоби (СМЗ) набагато ефективніші за мила, але їх залишки, потрапляючи в довкілля, завдають шкоди рослинному і тваринному світу.
'24. Які сполуки належать до вищих карбонових кислот?
'25. Напишіть рівняння реакцій олеїнової кислоти з бромною водою, барій гідроксидом, натрій карбонатом.
'26. Складіть молекулярні та йонно-молекулярні рівняння реакцій: а) калій пальмітату з водою;
б) магній стеарату із хлоридною кислотою.
!7. Чи здатні виявляти мийну дію: а) натрій сульфат; б) натрій ацетат; в) калій стеарат? Відповіді поясніть.
.185

228. Визначте формулу насиченої одноосновної карбонової кислоти (лауринової), якщо масова частка Оксигену в сполуці становить
16 %.
229. Яка маса натрій стеарату витратиться на осадження 1 г йонів Кальцію в деякому об'ємі річкової води?
27 Естери. Жири
Матеріал параграфа допоможе вам:
дізнатися про склад, назви і властивості естерів; розширити свої знання про жири та їх роль в організмі.
Естери. З а п а х б а г а т ь о х к в і т і в , ф р у к т і в , і н ш и х рослин з у м о в л е н и й н а я в н і с т ю в н и х о р г а н і ч н и х сполук певного к л а с у — естерів.
Похідні карбонових кислот, у молекулах яких атом Гідрогену карбоксильної групи заміщений на вуглеводневий залишок, називають естерами
Естери З а г а л ь н а ф о р м у л а естерів — К — , або
р |
|
|
КСООК'. |
|
|
|
|
|
|
|
|
|
|
и к |
|
|
Добування. |
Естери |
у т в о р ю ю т ь с я |
при |
взає- |
||||||
|
|
|
модії |
к а р б о н о в и х |
к и с л о т зі с п и р т а м и за наяв - |
||||||||
|
|
|
ності |
к о н ц е н т р о в а н о ї сульфатної |
(або |
орто- |
|||||||
|
|
|
фосфатної) к и с л о т и : |
|
|
|
|
|
|||||
|
^О |
|
|
|
Н2804 (КОНЦ.) |
|
//О |
|
|
||||
с н д - с ; |
> о н + н + о - с н я ' |
|
, ' |
" |
— = і с н ч |
- с |
ю с н , |
+ НоО. |
|||||
3 |
|
|
|
|
|
3 |
|
2 |
|||||
кислота |
спирт |
|
|
|
|
|
естер |
|
|
||||
|
|
|
Т а к і р е а к ц і ї , |
|
я к |
вам |
відомо, |
н а з и в а ю т ь |
реак - |
||||
|
|
|
ц і я м и естерифікації . |
Вони є оборотними; вод- |
|||||||||
1 Раніше такі сполуки називали складними ефірами.
186
н о ч ас |
і з |
п р я м о ю р е а к ц і є ю |
в і д б у в а є т ь с я зво- |
р о т н а |
— |
в з а є м о д і я естеру з |
водою (гідроліз) . |
Щ о б |
д о с я г т и я к о м о г а п о в н і ш о г о перетворен - |
||
ня к и с л о т и |
і с п и р т у на естер, р е а к ц і й н у с у м і ш |
н а г р і в а ю т ь |
д л я в и д а л е н н я п а р и одного і з про- |
д у к т і в п р я м о ї р е а к ц і ї . |
|
Назви. С и с т е м а т и ч н і |
н а з в и естерів с к л а д а - |
||||
ю т ь с я |
із двох ч а с т и н . П е р ш о ю ч а с т и н о ю є |
||||
н а з в а вуглеводневого |
з а л и ш к у , |
щ о м і с т и т ь с я |
|||
в м о л е к у л і |
с п и р т у , а |
д р у г о ю — |
н а з в а |
вугле - |
|
водню, |
від |
я к о г о п о х о д и т ь к и с л о т а , і з |
з а к і н - |
||
ч е н н я м |
- о а т: |
|
|
|
|
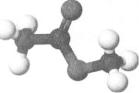
Мал. 82. Кулестержнева модель
молекули метилетаноату
О
СН,-С ЮСН,
метилетаноат
В і н ш и х н а з в а х естерів в и к о р и с т о - в у ю т ь н а з в и вуглеводневого з а л и ш к у м о л е к у л и с п и р т у і к а р б о н о в о ї к и с л о - ти (або її з а л и ш к у ) . Н а п р и к л а д , естер
СН3СООСН3 (мал. 82) називають
м е т и л о в и м естером оцтової к и с л о т и або м е т и л а ц е т а т о м .
Цікаво знати І Іенасичений естер метилів етакрилат пикористоиують у виробництві
< ірганічного скла.
• З а п р о п о н у й т е і н ш у н а з в у д л я е т и л п р о п а н о - ату і зобразіть с т р у к т у р н у ф о р м у л у м о л е к у - л и с п о л у к и .
Властивості. Естери з н е в е л и к и м и молеку -
л я р н и м и м а с а м и є |
безбарвними л е т к и м и |
ріди- |
н а м и здебільшого |
з п р и є м н и м з а п а х о м . |
Т а к , |
метилбутаноат СНзСН2 СН2 СООСНз має аромат я б л у к , бутилетаноат СН 3 СООСН 2 СН 2 СН 2 СН 3 —
г р у ш , е т и л б у т а н о а т С Н 3 С Н 2 С Н 2 С О О С 2 Н 5 |
— |
а н а н а с у , а б е н з и л е т а н о а т СН 3 СООСН 2 С 6 Н 5 |
— |
ж а с м і н у . Е с т е р и з к і л ь к о м а д е с я т к а м и а т о м і в К а р б о н у в м о л е к у л а х — тверді р е ч о в и н и , що
не м а ю т ь з а п а х у . |
Т а к і е с т е р и м і с т я т ь с я у |
||
б д ж о л и н о м у в о с к у . |
|
|
|
|
Е с т е р и н е р о з ч и н н і у воді, |
а л е р о з ч и н я ю т ь с я |
|
в |
о р г а н і ч н и х р о з ч и н н и к а х . |
С п о л у к и повіль - |
|
но |
в з а є м о д і ю т ь із |
водою (гідролізують) . За |
|
.187
