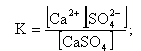- •1. Классификация и типы паровых котлов.
- •1.1. Паровой котел. Общее устройство и определения.
- •3.3. Общие технические характеристики топлив.
- •3.5.1. Характеристики твердого топлива.
- •3.5.2. Характеристики мазута.
- •3.5.3. Характеристики природного газа.
- •3.6.1. Размолоспособность топлива.
- •3.6.2. Тонкость размола пыли.
- •3.6.3. Затраты энергии на размол топлива.
- •3.6.4. Характеристика угольной пыли.
- •4.1. Основы кинетики химических реакций.
- •4.2.1. Горение газового топлива
- •4.2.2. Горение твердого топлива.
- •4.2.3. Горение жидкого топлива.
- •4.3. Развитие и воспламенение топливно-воздушной струи в топочном объеме.
- •4.4. Продукты сгорания топлива.
- •5.1. Введение.
- •5.2. Топочные камеры и горелки для сжигания твердых топлив.
- •5.3. Газомазутные топки и горелки.
- •6. Эффективность работы и основы теплового расчета котла.
- •6.1. Общее уравнение теплового баланса котла.
- •6.2. Коэффициент полезного действия парового котла и котельной установки.
- •6.3.1. Потери теплоты с уходящими газами.
- •6.3.2. Потери теплоты с химическим недожогом топлива.
- •6.3.3. Потери теплоты с механическим недожогом топлива.
- •6.3.4. Потери теплоты от наружного охлаждения.
- •6.3.5. Потери с физической теплотой удаляемых шлаков.
- •6.3.6. Оптимизация показателей работы парового котла по сумме тепловых потерь.
- •7. Эксплуатация паровых котлов.
- •7.1. Эксплуатационные режимы паровых котлов.
- •7.2. Статические характеристики парового котла в нерасчетных режимах работы.
- •7.3. Переходные процессы в котле при изменении нагрузки.
- •7.4.Регулирование температуры пара.
- •7.4.1. Методы парового регулирования температуры пара.
- •7.4.2. Методы газового регулирования.
- •7.5. Загрязнения и абразивный износ конвективных поверхностей нагрева.
- •7.6.1. Высокотемпературная коррозия.
- •7.6.2. Низкотемпературная коррозия.
- •7.7. Сокращение вредных выбросов в окружающую среду.
- •8.Характеристики и виды движения водного теплоносителя в паровых котлах
- •8.1.Водный теплоноситель в паровых котлах и его физико-химические характеристики.
- •8.2 Общие уравнения движения жидкости в трубах.
- •8.2.1.Уравнения неразрывности, движения, энергии и состояния жидкости.
- •8.2.2.Уравнение движения однофазного потока в трубах.
- •8.2.3.Уравнение движения двухфазного потока в трубах.
- •8.3.Режимы течения двухфазного потока.
- •8.4.Перепад давления при движении рабочей среды в трубе.
- •8.5.Виды движения жидкости.
- •9.Гидродинамика водного теплоносителя в паровых котлах.
- •9.1.Гидродинамика водного теплоносителя в поверхностях с принудительным движением.
- •9.1.1.Теплогидравлические характеристики поверхностей нагрева парового котла.
- •9.1.2.Гидравлическая характеристика горизонтальных одиночных труб.
- •9.1.3.Гидравлические характеристики вертикальных одиночных труб.
- •9.1.4.Гидравлические характеристики системы труб парового котла.
- •9.1.5.Гидравлическая разверка в системе труб парового котла.
- •9.1.6.Пульсация потока в системах труб парового котла.
- •9.2.Гидродинамика водного теплоносителя при естественной циркуляции.
- •9.2.1.Движущий и полезный напоры контура циркуляции.
- •9.2.2.Гидравлические характеристики контура циркуляции.
- •9.2.3.Расчет контуров циркуляции.
- •9.2.4.Показатели надежности работы контура циркуляции.
- •9.3. Организация сепарации влаги и пара в барабанных котлах.
- •9.3.1.Барабан - сепарационное устройство барабанного котла.
- •9.3.2.Гидродинамические процессы в барабане парового котла.
- •10. Температурный режим поверхностей нагрева паровых котлов.
- •10.1.Металл паровых котлов.
- •10.2.Расчет температурного режима обогреваемых труб парового котла.
- •10.3.Условия теплообмена на стенке прямолинейной части трубы парового котла.
- •10.3.1.Теплообмен при докритическом давлении водного теплоносителя.
- •10.3.2.Теплообмен при сверхкритическом давлении водного теплоносителя.
- •10.4.Особенности температурного режима горизонтальных труб, криволинейных труб и каналов и газоплотных экранов.
- •10.5.Влияние внутритрубных отложений на температурный режим обогреваемых труб парового котла.
- •11.Физико-химические процессы в пароводяном тракте парового котла.
- •11.1.Материальный баланс примесей в пароводяном тракте парового котла.
- •11.2.Коррозия металла в пароводяном тракте парового котла.
- •11.3.Растворимость примесей в водном теплоносителе.
- •11.4.Переход примесей из воды в насыщенный пар.
- •11.5.Внутритрубные отложения примесей водного теплоносителя.
- •11.6.Образование отложений примесей в пароводяном тракте прямоточного котла.
- •11.7.Образование отложений примесей в пароводяном тракте барабанного котла.
- •11.7.1.Удаление примесей с непрерывной продувкой воды из водяного тракта барабанного котла.
- •11.7.2.Организация ступенчатого испарения в барабанном котле.
- •12.Водно-химические режимы паровых котлов.
- •12.1.Водно-химические режимы и нормы качества пара и питательной воды.
- •12.2.Водно-химические режимы прямоточных котлов.
- •12.3.Водно-химические режимы барабанных котлов.
- •12.4.Влияние внутрибарабанных устройств на качество котловой воды и насыщенного пара.
- •12.5.Химические очистки паровых котлов.
- •12.6.Консервация паровых котлов.
11.3.Растворимость примесей в водном теплоносителе.
Примеси, поступающие в водный теплоноситель, можно разделить на две группы: естественные примеси и продукты коррозии. Естественные примеси поступают в водяной тракт за счет присосов воды в конденсаторе и сетевых подогревателях, с добавочной водой; остаточная концентрация катионов Na, К, Са, Mg не изменяется после БОУ (после конденсатора, если нет БОУ). Продукты коррозии (катионы Fe, Cu, Al и др.) образуются в самом водяном тракте, их количество увеличивается по мере прохождения среды по тракту.
Естественные примеси делятся на две группы: трудно (мало) растворимые и легко (хорошо)растворимые.
К труднорастворимым соединениям относятся соединения Са и Mg: сульфат CaSO4, карбонаты СаСО3, MgCO3, силикаты СаSiO3, MgSiO3, гидроксиды Са(ОН)3, Mg(OH)2.
К легкорастворимым соединениям Са и Mg относятся: сульфат MgSO4, хлориды CaCI2, MgCL2, бикарбонаты Са(НСО3)2, Mg(HCO3)2. Все натриевые соединения обладают высокой растворимостью в воде.
Поступление в паровой котел труднорастворимых соединений кальция и магния с питательной водой лимитируется на достаточно низком уровне. При нарушениях в работе конденсатоочистки, увеличении присосов воды в конденсаторе количество поступающих соединений Са и Mg значительно возрастает.
Такие соединения, как CaSO4, CaCO3, Mg(OH)2, имеют отрицательный температурный коэффициент растворимости, т.е. с ростом температуры растворимость падает (рис. 11.5). В природных водах содержание Са существенно выше, чем Mg, поэтому при анализе поведения труднорастворимых соединений обычно рассматривают только соединения Са.
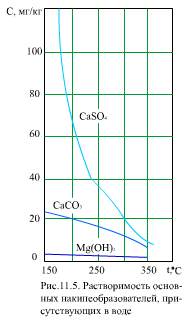
Труднорастворимые соединения в воде частично диссоциируют на ионы (катионы Mem+и анионы Ann-). Например:
|
|
(11.13) |
Степень диссоциации К равна (вместо активностей рассматриваем концентрации ионов, что для разбавленных растворов допустимо)
|
|
(11.14) |
|
|
(11.15) |
Произведение концентрации (активностей) ионов труднорастворимой соли в насыщенном растворе, называемое произведением растворимости ПР, постоянно при данной температуре и зависит от температуры системы.
При упаривании воды в испарительных поверхностях нагрева концентрация всех ионов повышается и может достигнуть насыщения. В первую очередь кристаллизоваться из водного раствора будут те соединения, произведение растворимости которых минимально. Соединения с отрицательным коэффициентом растворимости кристаллизуются в основном на поверхности нагрева, образуя накипь. Такие вещества называют накипеобразователями. Другие вещества, с положительным коэффициентом растворимости, кристаллизуются в объеме раствора на грубодисперсных и коллоидных частицах, образуя шлам, т.е. мелкие взвешенные в воде частички (вещества - шламообразователи).
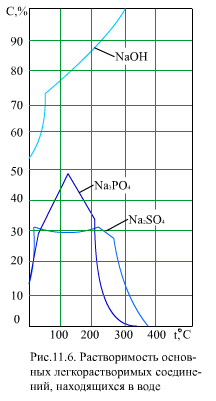
На (рис. 11.6) приведены значения растворимости для некоторых легкорастворимых соединений. Видно, что некоторые из них (NaOH) имеют положительный коэффициент растворимости во всем приведенном диапазоне температур, другие (Na3PO4, Na2SO4) - только до 100…150°С, а при температуре свыше 200°С имеют отрицательный коэффициент растворимости. При нормальной работе барабанных котлов концентрация этих примесей обычно значительно меньше их растворимости, и кристаллизоваться на стенках трубы или в объеме среды они не будут. Только в местах упаривания воды (в отложениях на стенке, в прикипевшем к стенке шламе) и в зоне кризиса теплообмена возможно достижение насыщения и выпадение легкорастворимых соединений.
Растворимость веществ в воде и паре определяется физико-химическими свойствами вещества и водного теплоносителя, которые, в свою очередь, зависят от температуры и давления. В области, примыкающей к температуре кипения при ДКД и в зоне большой теплоемкости при СКД, плотность водного теплоносителя резко падает до относительно низких значений в паровой фазе. Соответственно растворяющая способность теплоносителя снижается.
В питательной воде содержится заметное количество различных продуктов коррозии конструкционных материалов. Наиболее важную роль в образовании внутритрубных отложений, в интенсивности коррозии играет магнетит Fe3O4. Растворимость магнетита в воде представлена на (рис. 11.7). Видно, что максимум растворимости магнетита приходится на температуру порядка 150°С, а затем растворимость уменьшается до температуры 300…350°С. С увеличением концентрации аммиака (при этом рН растет с 8,75 до 9,7) растворимость магнетита падает.
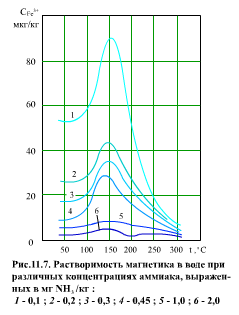
В действительности концентрация магнетита в питательной воде может быть в несколько раз выше растворимости. Это означает, что в воде магнетит находится не только в растворенной форме, но и имеются коллоидные и грубодисперсные частицы. Растворимость других оксидов металлов в воде имеет такой же порядок, что и растворимость магнетита (рис. 11.8).

Растворимость веществ в перегретом паре описывается формулой
|
|
(11.16) |
где К - постоянная для данного вещества величина; m- координационное число, показывающее среднестатистическое количество молекул воды, скоординированных около одной частицы растворяющегося вещества; ∆Н - тепловой эффект реакции растворения. Так как плотность пара ρ с ростом температуры уменьшается, а экспонента увеличивается, то можно ожидать, что растворимость веществ в паре будет иметь минимум при какой-то температуре.
На (рис. 11.9) для примера показана растворимость NaCI в перегретом паре для нескольких значений давления. Видно, что при р = 14 МПа и 18 МПа, имеются минимумы растворимости при температуре 470…500°С. С увеличением давления плотность пара и растворимость веществ растет.
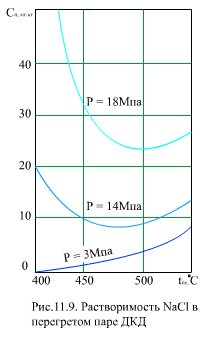
При сверхкритическом давлении плотность среды плавно изменяется от плотности воды до плотности пара, наиболее интенсивное (по температуре) изменение плотности происходит в ЗБТ. Поэтому растворимость веществ в жидкой фазе (до ЗБТ) при СКД аналогично растворимости в воде при ДКД, т.е. может иметь положительный или отрицательный температурный коэффициент растворимости. В зоне большой теплоемкости растворимость веществ из-за резкого уменьшения плотности среды снижается, а затем, при переходе в область перегретого пара, может дальше снижаться или, после прохождения минимума, расти (рис. 11.10).