
Акушерство для студентов / Запоражан том 2
.pdf
Розділ 20. Пухлини яєчників...
ротомія вже не може бути стандартом лікування, оскільки моніторинг щодо успіху ліку вання і розвитку рецидивної хвороби проводять за допомогою контролю сироваткового рівня СА 125. На жаль, епітеліальні пухлини яєчників часто рецидивують, незважаючи на агресивне лікування.
Прогноз. Середнє 5 річне виживання хворих з епітеліальним раком яєчників стано вить менше ніж 20 % (80–95 % — для стадії І, 40–70 % — для стадії ІІ, 30 % — для стадії
ІІІ і менш ніж 10 % — для IV стадії раку).
Зародковоклітинні пухлини яєчників
Патогенез. Зародковоклітинні (герміногенні) пухлини виникають із поліпотентних зародкових клітин, які здатні диференціюватися в три зародковоклітинні типи: жовтко вий мішок, плаценту і плід (рис. 20.2). Зародковоклітинні пухлини яєчника подібні до зародковоклітинних пухлин в яєчках. Найбільш частим типом зародковоклітинного раку яєчників є дисгерміноми і незрілі тератоми. Ембріональна карцинома, пухлина ендодер мального синуса (жовткового мішка), негестаційна хоріокарцинома і змішані зародко воклітинні пухлини є менш частими. Більшість цих пухлин продукують сироваткові пух линні маркери, які звичайно використовують для контролю ефективності лікування (табл. 20.8).
Хоча існують значні варіації в експресії сироваткових маркерів яєчниковими пухли нами, в більшості випадків дисгермінома продукує ЛДГ, ембріональна карцинома і пух лина ендодермального синуса синтезують АФП, хоріокарцинома продукує β ХГЛ.
На відміну від епітеліальних пухлин, більшість зародковоклітинних пухлин яєчників маніфестують на ранній стадії під час діагностики. Тому більшість із них мають кращий прогноз, ніж епітеліальні пухлини і вважаються курабельними.
Епідеміологія. Зародковоклітинні пухлини становлять 15–20 % усіх яєчникових пух лин. Хоча 95 % з них є доброякісними, решта 5 % є злоякісними і виявляються переваж но у дітей і молодих жінок. Зародковоклітинні пухлини нерідко виникають у віці 10–20 років.
Клінічна маніфестація. На відміну від епітеліальних пухлин яєчників, симптоми за родковоклітинних пухлин є більш ранніми і виявляються від первинної пухлини, а не метастатичних уражень. Пацієнтки з зародковоклітинними пухлинами нерідко скаржать ся на біль у животі; при об’єктивному дослідженні виявляються об’ємні утворення при датків матки, що швидко зростають. Функціональні зародковоклітинні пухлини можуть продукувати β ХГЛ, АФП, ЛДГ і/або СА 125 залежно від клітинного типу (див. табл. 20.8).
Лікування. Враховуючи, що більшість зародковоклітинних пухлин виявляють на ранній стадії і вони рідко є двобічними, хірургічне лікування звичайно полягає у видаленні
|
Зародкова клітина |
|
Дисгермінома |
Ембріональна карцинома |
|
недиференційована |
|
|
Екстраембріональні |
Трофобластні |
Ембріональні |
(жовткового мішка) тканини |
(плацентарні) тканини |
(фетальні) тканини |
Пухлина ендодермального синуса |
Хоріокарцинома |
Тератома |
Рис. 20.2. Гістогенез зародковоклітинних пухлин яєчника
219

Акушерство і гінекологія. Том 2
Сироваткові маркери зародковоклітинних пухлин яєчників |
Таблиця 20.8 |
||||
|
|
||||
|
|
|
|
|
|
Пухлина |
|
Пухлинні маркери |
|
|
|
β ХГЛ |
АФП |
ЛДГ |
|
СА 125 |
|
|
|
||||
Змішані зародковоклітинні пухлини |
+ |
+ |
+ |
|
+ |
Ембріональна карцинома |
+ |
+ |
|
|
+ |
Пухлина ендодермального синуса |
|
+ |
|
|
|
Дисгермінома |
|
|
+ |
|
+ |
Незріла тератома |
|
|
|
|
+ |
Хоріокарцинома |
+ |
|
|
|
|
ураженого яєчника — оваріоектомії, в тому числі лапароскопічній. Але повне хірургічне стадіювання повинне завжди виконуватися. Більшість випадків зародковоклітинного раку вважаються курабельними при застосуванні поліхіміотерапії (цисплатин, вінблас тин і блеоміцин або блеоміцин, етопозид і платин).
Променева терапія не є основним компонентом лікування зародковоклітинних пух лин яєчників, окрім дисгерміном, які є винятково чутливими до абдомінальної проме невої терапії.
Прогноз. Частота 5 річного виживання становить 85 % випадків для пацієнток із дис герміномою, 70–80 % — із незрілою тератомою і 60–70 % — для пацієнток із пухлиною ендодермального синуса.
Пухлини строми статевого тяжа
Патогенез. Ці пухлини виникають як зі статевого тяжа, так і з ембріональних гонад (до диференціації у чоловічу або жіночу стать) або зі строми яєчника (див. рис. 20.1). Найбільш частим типом цих клітин є гранульозо текаклітинні пухлини (70 % випадків), які мають низький малігнізуючим потенціал. Як гранульозо текаклітинні пухлини, так і Сертолі — Лейдига клітинні пухлини є гормонопродукуючими. Строма яєчника може диференціюватись в яєчникову або яєчкову. Отже, яєчникові гранульозо текаклітинні пухлини схожі на фетальні яєчники і продукують значну кількість естрогенів, тимчасом як Сертолі — Лейдига клітинні пухлини нагадують фетальні яєчка і продукують тесто стерон та інші андрогени.
Фіброма яєчника походить зі зрілих фібробластів і, на відміну від інших стромаль ноклітинних неоплазм, не є функціонуючою. В рідкісних випадках фіброма може супро воджуватись асцитом. Наявність пухлини яєчника, асциту і правобічного гідротораксу відомі під назвою синдрому Мейгса.
Епідеміологія. Стромальноклітинні пухлини яєчника звичайно розвиваються у жінок в постменопаузі. Вік хворих коливається від 40 до 70 років.
Клінічна маніфестація. Гранульозо текаклітинні пухлини яєчника часто продукують естрогени й інгібін, тому вони можуть спричинювати фемінізацію, передчасний стате вий розвиток, постменопаузальні кровотечі. Сертолі — Лейдига клітинні пухлини про дукують андрогени і можуть спричинити вірилізуючі ефекти, включаючи гірсутизм, зниження тембру голосу, акне і кліторомегалію.
Лікування. Вважаючи, що більшість стромальноклітинних пухлин яєчників виника ють у жінок у постменопаузі, лікування звичайно полягає у тотальній абдомінальній гістеректомії з білатеральною сальпінгоофоректомією (ТАНВSO). Хіміотерапія не є ефективною в лікуванні стромальноклітинних пухлин яєчника. Незважаючи на агресив
220

Розділ 20. Пухлини яєчників...
не лікування, ці пухлини часто рецидивують. Післяопераційне тазове опромінення може використовуватися при ранніх стадіях захворювання.
Прогноз. Частота 5 річного виживання хворих зі злоякісними стромальноклітинни ми пухлинами становить 90 % для І стадії. Але ці пухлини мають тенденцію до повільно го росту; рецидиви можливі навіть через 15–20 років після видалення первинного ура ження.
Рак маткових труб
Патогенез. Причинний фактор раку маткових труб є невідомим. Більшість випадків раку фаллопієвих труб представлені аденокарциномою і виникають зі слизової оболон ки труби — ендосальпінксу. Саркоми і змішані мюллерові пухлини є менш частими. Прогресування раку маткових труб є подібним до такого при раку яєчників, включаючи пряме перитонеальне поширення і розвиток асциту. Рак маткових труб є двобічним у 10–20 % випадків і нерідко може являти метастатичне ураження з інших первинних пухлин.
Епідеміологія. Первинний рак маткових труб є виключно рідкісним і становить 0,5 % випадків гінекологічного раку. Ці пухлини можуть виникати в будь якому віці (від 18 до 80 років), але середній вік хворих під час діагностики дорівнює 52 рокам.
Клінічна маніфестація. Класичні симптоми раку маткових труб включають біль, про фузні водянисті вагінальні виділення і менорагію (hydrops tubae profluens), тобто нага дують такі при позаматковій вагітності. Хворі можуть скаржитися на перемінний біль внизу живота. Але діагноз раку маткових труб рідко визначається на доопераційному етапі. Це захворювання часто є безсимптомним і нерідко діагностується лише під час лапаротомії за іншими показаннями або при підозрі на пухлину яєчника.
Лікування. Лікування раку маткових труб виконується подібно до такого при епітелі альному раку яєчників і включає тотальну абдомінальну гістеректомію з білатеральною сальпінгооваріоектомією, оментектомію і циторедукцію. Післяопераційна хіміотерапія включає цисплатин і циклофосфамід. Абдомінальну променеву терапію призначають пацієнткам із повним видаленням пухлини.
Прогноз при раку маткової труби не відрізняється від такого при епітеліальному раку яєчників і звичайно є несприятливим.
Контрольні питання
1.Охарактеризуйте гістогенез пухлин яєчників. Класифікація пухлин яєчників.
2.Як проводиться диференційна діагностика об’ємних утворень яєчників?
3.Рак яєчників: етіологія, патогенез, класифікація, стадіювання, хірургічне лікування, хіміотерапія.
4.Чи існує скринінговий метод діагностики раку яєчників?
5.Яка роль ультразвукового дослідження в діагностиці пухлин яєчників?
6.Яка роль біохімічних маркерів у моніторингу хворих на рак яєчників?
7.Що включають епітеліальні пухлини яєчників?
8.Поняття про зародковоклітинні пухлини яєчників.
9.Пухлини строми статевого тяжа: гістогенез, класифікація, клініка і діагностика.
10.Рак маткових труб: клініка, діагностика, лікування.
221

Акушерство і гінекологія. Том 2
Розділ 21
ГЕСТАЦІЙНА ТРОФОБЛАСТИЧНА ХВОРОБА
Гестаційна трофобластична хвороба (ГТХ) — різноманітна група взаємопов’язаних захворювань, які супроводжуються аномальною проліферацією трофобластної (плацен тарної) тканини, внаслідок запліднення яйцеклітини сперматозоїдом з аномальним вмістом ДНК. Гістологічні дані можуть включати як везикулярні хоріальні ворсинки, так і проліферуючий трофобласт.
Гестаційна трофобластична хвороба являє собою спектр неопластичних процесів, які класифікуються за чотирма основними групами (табл. 21.1): міхуровий занесок (молярна вагітність, 80 % випадків), інвазивний міхуровий занесок (10–15 % ), хоріокарцинома (2–5 %) і дуже рідкісна трофобластна пухлина плацентарної площини (placental site trophoblastic tumor, PSTT). Ці пухлини здатні продукувати хоріонічний гонадотропін лю дини (ХГЛ), який використовується і як пухлинний маркер, і як скринінговий тест для контролю за ефективністю лікування. Гестаційна трофобластична хвороба є винятково чутливою до хіміотерапії.
Доброякісна гестаційна трофобластична хвороба
Доброякісна гестаційна трофобластична хвороба представлена міхуровим занеском (hydatidiform mole), який становить 80 % випадків ГТХ. Понад 90 % випадків міхуровий занеска класифікуються як класичний, або повний міхуровий занесок, і є наслідком мо лярної дегенерації за відсутності плода (рис. 21.1, а). В 10 % випадків молярної вагіт ності має місце частковий, або неповний міхуровий занесок, який представлений мо лярною дегенерацією у сполученні з присутністю аномального плода (табл. 21.2). Міху ровий занесок у 90 % випадків є доброякісним захворюванням. Решта випадків пред ставлена інвазивним міхуровим занеском, хоріокарциномою або трофобластною пухли ною плацентарної площини.
|
Таблиця 21.1 |
Класифікація гестаційної трофобластичної хвороби |
|
|
|
Доброякісна ГТХ |
Злоякісна ГТХ* |
|
|
Міхуровий занесок (80 %) |
Інвазивний міхуровий занесок (10–15 %) |
Повний міхуровий занесок (класичний) |
Хоріокарцинома (2–5 %) |
Неповний міхуровий занесок (частковий) |
Трофобластична пухлина плацентарної |
|
площини |
|
|
Примітка. * — злоякісна ГТХ поділяється на неметастазуючу і метастазуючу.
222

Розділ 21. Гестаційна трофобластична хвороба
1
2 |
3 |
а |
б |
Рис. 21.1. Повний міхуровий занесок: а — схематичне зображення; б — цитоге нетичний механізм повного міхурового занеска, фертилізація порожньої яйцеклі тини (без ядра); всі хромосоми мають батьківське походження;
1 — матка; 2 — яйцеклітина; 3 — тільки батьківські хромосоми
Повний міхуровий занесок
Патогенез. Хоча причина цього захворювання залишається невідомою, вважають, що більшість випадків повного міхурового занеска виникають внаслідок фертилізації без’я дерної яйцеклітини («порожнього яйця»), в якій ядро втрачене або не функціонує, од ним нормальним сперматозоїдом (рис. 21.1, б).Отже, всі хромосоми продукту заплід нення в цьому разі мають батьківське походження. В 90 % випадків повний міхуровий
|
|
Таблиця 21.2 |
Порівняльна характеристика повного і неповного міхурового занеска |
||
|
|
|
Риси |
Повний/класичний |
Неповний/частковий |
|
|
|
Генетика |
|
|
Найбільш частий каріотип |
46, XX |
69, XXY |
Хромосомне походження |
Усі батьківського |
Додатковий батьківський |
Патологія |
походження |
набір хромосом |
|
|
|
Супутній плід |
Відсутній |
Присутній |
Хоріальні ворсинки |
Гідропічні, роздуті |
Фокальні, видимий набряк |
Гіперплазія трофобласта |
Дифузна, виражена |
Фокальна, мінімальна |
Клінічна презентація |
|
|
Симптоми/ознаки |
Аномальні піхвові |
Missed abortion |
|
кровотечі |
|
Розмір матки |
на 50 % менше гестацій |
Відповідає гестаційному |
|
ного віку |
віку |
|
на 30 % більше гестацій |
|
Персистуюча (злоякісна) |
ного віку |
|
|
|
|
ГТХ |
|
|
Неметастазуюча |
15–25 % |
3–4 % |
Метастазуюча |
4 % |
0 |
223

Акушерство і гінекологія. Том 2
занесок має каріотип 46,ХХ, в 10 % випадків — 46,XY. У рідкісних випадках повний міху ровий занесок утворюється при фертилізації порожньої яйцеклітини двома нормальни ми сперматозоїдами. Отже, і в цьому разі всі хромосоми продукту запліднення мають батьківське походження.
Плацентарна аномалія при повному міхуровому занеску характеризується проліфе рацією трофобласта і гідропічною дегенерацією або відсутністю частин плода. Хоча більшість випадків захворювання є доброякісними, повний міхуровий занесок має більший малігнізуючий потенціал, ніж неповний (див. табл. 21.2).
Епідеміологія. Частота міхурового занеска коливається від 1:200 до 1:1000 вагітнос тей у різних країнах світу, збільшуючись в азіаток.
Фактори ризику. Гестаційна трофобластична хвороба виникає у репродуктивному віці (20–40 років). Зростання частоти захворювання має місце в тих географічних зонах, де дієта є бідною на бета каротин і фолієву кислоту. Частіше ГТХ розвивається у жінок, які мали в анамнезі самовільні викидні або міхуровий занесок.
Клінічна маніфестація
Анамнез. Найбільш частим симптомом міхурового занеска є нерегулярні або значні піхвові кровотечі в ранньому терміні вагітності (в 97 % випадків). Кровотеча звичайно є неболючою, але може бути асоційована з матковими скороченнями. Інші стани, асоц ійовані з цим захворюванням, подано в табл. 21.3. Але завдяки сучасній ранній діагнос тиці міхурового занеска ці ускладнення спостерігаються рідко.
Симптоми міхурового занеска потребують диференціації з іншими станами, асоційо ваними з підвищенням рівня ХГЛ: тяжка нудота і блювання — з нестримним блюванням вагітних; роздратованість, запаморочення, фотофобія — з прееклампсією, нервозність, анорексія, тремор — з гіпертиреоїдизмом. Прееклампсія до 24 тиж вагітності має силь ний кореляційний зв’язок з міхуровим занеском.
Об’єктивне обстеження. У разі повного міхурового занеска при гінекологічному до слідженні може спостерігатись експульсія гроноподібних молярних часточок у піхву або кровотеча з цервікального каналу. Інколи можуть бути виявлені двобічні тека лютеїнові кісти, які виникають внаслідок стимуляції яєчників високим рівнем ХГЛ. Виявляють невідповідність матки гестаційному віку, відсутність серцебиття і рухів плода. При клінічному дослідженні можуть бути виявлені ознаки гіпертиреоїдизму або прееклампсії: тахікардія, тахіпное і гіпертензія.
Діагностика. У разі міхурового занеска рівень ХГЛ є значно вищим (> 100 000 мМО/ мл), ніж при нормальній вагітності. Діагноз підтверджується при ультразвуковому до слідженні, при якому виявляють «синдром снігової заметілі» внаслідок набряку хоріоніч них ворсин (рис. 21.2). У разі
|
Таблиця 21.3 |
повного занеска елементи |
Симптоми, асоційовані з міхуровим занеском |
плода при ультразвуковому |
|
|
|
дослідженні не візуалізують |
Симптоми |
Частота, % |
ся. |
|
|
|
Піхвові кровотечі |
90–97 |
Диференційну діагностику |
Виділення молярних пухирців |
80 |
виконують тоді, коли має міс |
Невідповідність розмірів матки |
|
це підвищення рівня ХГЛ |
гестаційному віку |
30–50 |
і/або збільшена плацента (ба |
Двобічні тека лютеїнові кісти |
15–50 |
гатоплідна вагітність, неімун |
Нестримне блювання вагітних |
10–25 |
на водянка плода, внутрішньо |
Прееклампсія до 24 тиж гестації |
10–15 |
маткова інфекція, міома мат |
Гіпертиреоїдизм |
10 |
ки, загрожуючий аборт, екто |
Трофобластичні легеневі емболи |
2 |
пічна і маткова вагітність). |
|
|
|
224

Розділ 21. Гестаційна трофобластична хвороба
Лікування міхурового занеска, незалежно |
|
|
віж терміну вагітності, полягає у терміново |
|
|
му видаленні вмісту матки. Якщо пацієнтка |
|
|
бажає зберегти фертильність, виконують ва |
|
|
куум аспірацію вмісту матки з подальшим |
|
|
вишкрібанням її порожнини гострою кюрет |
|
|
кою. Після видалення всієї маси міхурового |
|
|
занеска виконують внутрішньовенне введен |
|
|
ня окситоцину для стимуляції маткових ско |
|
|
рочень і мінімізації крововтрати. Якщо паці |
|
|
єнтка не бажає зберегти фертильність, аль |
|
|
тернативним варіантом лікування може бу |
|
|
ти гістеректомія. Ризик рецидивного захво |
|
|
рювання становить 3–5 %, навіть у разі |
|
|
гістеректомії. |
Рис. 21.2. Ультразвукові ознаки міхурово |
|
Моніторинг хворих. Прогноз міхурового |
го занеска (HM). Тека лютеїнова кіста (ТC) |
|
занеска є сприятливим (95–100 % випадків |
яєчника |
|
ефективного лікування). Персистенція за |
|
|
хворювання спостерігається у 15–25 % паці |
N |
|
єнток із повним і у 4 % — з частковим занес |
|
|
ком. Отже, ретельне спостереження за хво |
|
|
рими є необхідним. |
|
|
Після евакуації міхурового занеска кон |
|
|
трольні дослідження рівня β ХГЛ проводять |
|
|
щотижня до одержання трьох нормальних ре |
|
|
зультатів. Після цього проводять щомісяч |
|
|
ний моніторинг рівня β ХГЛ протягом що |
|
|
найменше 1 року. На рис. 21.3 продемонст |
|
|
ровано нормальну регресію титру β ХГЛ |
|
|
після евакуації міхурового занеска. Протя |
|
|
гом періоду моніторингу пацієнтка повинна |
|
|
утримуватися від вагітності. |
|
|
Пацієнтки після успішного лікування |
|
|
міхурового занеска не мають зростання ри |
|
|
зику самовільних абортів і природжених |
|
|
аномалій розвитку. Ризик розвитку ГТХ при |
|
|
подальшій вагітності становить 1–5 %. |
|
|
Неповний |
Норма |
|
|
||
міхуровий занесок |
D |
|
Патогенез. Неповний міхуровий занесок |
||
Рис. 21.3. Нормальна регресія β ХГЛ |
||
утворюється внаслідок фертилізації нор |
||
після евакуації міхурового занеска: |
||
мальної яйцеклітини двома сперматозоїдами |
||
N — рівень бета субодиниці ХГЛ у си |
||
одномоментно (рис. 21.4). Це призводить до |
||
роватці крові, мМО/мл; D — тижні після |
||
розвитку триплоїдного каріотипу з 69 хро |
||
евакуації міхурового занеска |
||
мосомами, з яких два хромосомних набори |
||
|
||
мають батьківське походження. Каріотип не |
|
повного міхурового занеска у 80 % випадків 69,XXY, у 20 % — 69,ХХХ і 2/3 ДНК мають батьківське походження. Плацентарні аномалії при неповному міхуровому занеску супро воджуються фокальними гідропічними ворсинками і гіперплазією синцитіотрофобласта.
225
Акушерство і гінекологія. Том 2
2
1
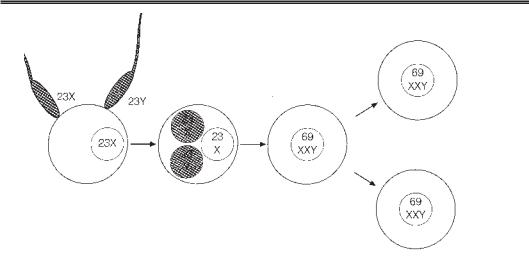
Рис. 21.4. Цитогенетичний механізм неповного міхурового занеска. Ферти лізація нормальної яйцеклітини двома сперматозоїдами (діандрія): 1 — діандрія; 2 — триплоїдія 69, XXY (додатковий батьківський набір хромосом)
Неповний міхуровий занесок часто супроводжується наявністю супутнього плода з триплоїдним генотипом і численними аномаліями. Більшість плодів, асоційовані з міху ровим занеском, можуть прожити лише кілька тижнів у матці перед виникненням само вільного аборту в кінці першого — на початку другого триместру гестації. Неповний міху ровий занесок звичайно є більш доброякісним і має менший малігнізуючий потенціал, ніж повний.
Клініка і діагностика. Неповний міхуровий занесок маніфестує затримкою менструа ції та симптомами вагітності. У 90 % пацієнток з неповним міхуровим занеском відбу вається викидень. Симптоми й ознаки неповного міхурового занеска подібні до таких при повному, але виражені звичайно в меншій мірі. Розміри матки можуть спочатку відповідати терміну вагітності, серцева діяльність плода може бути присутньою. Тому неповний міхуровий занесок може бути діагностований дещо пізніше. Діагноз визна чається при гістологічному дослідженні продукту запліднення.
Лікування часткового мізхурового занеска полягає у терміновій евакуації вмісту мат ки. Менш ніж у 4 % пацієнток неповний міхуровий занесок може прогресувати у малігні зуюче захворювання.
Моніторинг хворих полягає у серійному дослідженні рівня β ХГЛ за такими принци пами, як і у разі повного міхурового занеска. Для точного контролю за рівнем β ХГЛ важливим є запобігання вагітності.
Злоякісна гестаційна трофобластична хвороба
Патогенез. У 10 % пацієнток із ГТХ розвивається персистуюча (злоякісна, малігнізу юча) форма захворювання. Злоякісна ГТХ поділяється на 3 гістологічних типи:
1)інвазивний міхуровий занесок;
2)хоріокарцинома;
3)трофобластна пухлина плацентарної площини.
У 50 % випадків злоякісна ГТХ розвивається через місяці та роки після міхурового занеска. Інші 25 % випадків виникають після нормальної вагітності, ще 25 % — після самовільного викидня, ектопічної вагітності або аборту.
226

Розділ 21. Гестаційна трофобластична хвороба
Злоякісна ГТХ: |
|
|
Інвазивний занесок |
||
Хоріокарцинома |
|
|
Неметастазуюча |
Метастазуюча |
|
Захворювання не поширюється |
Захворювання поширюється |
|
за межі матки |
за межі матки |
|
|
|
|
|
|
|
Несприятливий прогноз: |
Сприятливий прогноз: |
|
Тривалість > 4 міс |
Коротка тривалість (< 4 міс) |
|
Рівень β ХГЛ > 40 000 мМО/мл |
Рівень β ХГЛ < 40 000 мМО/мл |
|
Неефективна попередня хіміотерапія |
Відсутність метастазів у мозку та печінці |
|
ГТХ після доношеної вагітності |
Відсутність попередньої хіміотерапії |
|
Рис. 21.5. Класифікація злоякісної гестаційної трофобластичної хвороби
У зв’язку з різним лікуванням і прогнозом, злоякісна ГТХ розподіляється також на неметастазуючу (не розповсюджується за межі матки) і метастазуючу (поширюється за межі матки). Метастатична хвороба, в свою чергу, може мати сприятливий або неспри ятливий прогноз залежно від часового проміжку після попередньої вагітності, рівня
βХГЛ, наявності метастазів у мозку та печінці, типу попередньої вагітності, результатів попередньої хіміотерапії (рис. 21.5).
Стадіювання гестаційної трофобластичної хвороби подано в табл. 21.4. Але ця систе ма класифікації не використовується в клінічній практиці, тому що не враховує важливі прогностичні фактори: ступінь метастазування, тип попередньої вагітності, тривалість захворювання. Всесвітньою організацією охорони здоров’я запропоновано систему про гностичних факторів ГТХ (табл. 21.5).
Клінічна маніфестація. Хоча три форми злоякісної ГТХ гістологічно є різними, клінічна вираженість має більше прогностичне значення, ніж гістологічні особливості. Гестаційна трофобластична хвороба, що виникає після міхурового занеска, типово діаг ностується у разі наявності плато або підвищеного рівня β ХГЛ протягом періоду моні торингу після евакуації міхурового занеска. На відміну від інших форм ГТХ, трофобла стична пухлина плацентарної площини характеризується хронічно низьким рівнем
βХГЛ. Пацієнтки з рівнем β ХГЛ > 100 000 мМО/мл, збільшенням розмірів матки, розвитком тека лютеїнових кіст мають найвищий ризик злоякісної ГТХ. Хоріокарци нома має тенденцію маніфестувати як метастатична хвороба.
Лікування. Гестаційна трофобластична хвороба є надзвичайно чутливою до хіміоте рапії. Лікування неметастазуючої ГТХ про
водиться одним агентом, звичайно мето
трексатом або актиноміцином D. Таблиця 21.4
Метотрексат є антиметаболітом, який |
Стадіювання гестаційної |
||
трофобластичної хвороби (за FIGO) |
|||
припиняє розвиток клітин у S фазі клітин |
|||
|
|
||
ного циклу шляхом зв’язування дигідрофо |
Стадія |
Поширеність захворювання* |
|
лат редуктази, що запобігає редукції дигід |
|
|
|
І |
Обмежена тілом матки |
||
рофолатів у тетрагідрофіолієву кислоту. Це, |
|||
ІІ |
Метастази в таз або піхву |
||
в свою чергу, інгібує тимідилат синтетазу і |
|||
ІІІ |
Метастази в легені |
||
продукцію пуринів, зменшення ДНК, РНК і |
|||
IV |
Віддалені метастази |
||
синтезу білка. |
|||
|
|
||
Побічні ефекти лікування метотрексатом |
Примітка. * — метастази за частотою роз |
||
включають мукозит (запалення слизових |
поділяються так: легені, піхва, таз, мозок, пе |
||
оболонок), виразки у ротовій порожнині, |
чінка. |
|
|
227

Акушерство і гінекологія. Том 2
Таблиця 21.5
Прогностичні фактори гестаційної трофобластичної хвороби*
Фактори ризику |
|
Оцінка, бали |
|
|
|
0 |
1 |
2 |
3 |
|
|
|
|
|
Вік, роки |
≤ 39 |
>39 |
|
|
Попередня вагітність |
Міхуровий |
Аборт |
Доношена |
|
|
занесок |
|
|
|
Інтервал після вагітності |
< 4 |
4–6 |
7–12 |
> 12 |
до лікування, міс |
|
|
|
|
Рівень β ХГЛ, МО/л |
<103 |
103–104 |
104–105 |
> 105 |
Група крові |
— |
0 або А |
В або АВ |
|
Кількість метастазів |
|
1–3 |
4–8 |
> 8 |
Місця метастазів |
|
Селезінка, |
Шлунок, |
Мозок |
|
|
нирки |
кишки, печінка |
|
Найбільша пухлина, |
< 3 |
3–5 |
> 5 |
|
включаючи маткову, см |
|
|
|
|
Попередня хіміотерапія |
Відсутня |
— |
1 препарат |
≥ 2 препаратів |
Примітка. * — загальна оцінка ризику для пацієнтки складається з сумарної оцінки всіх прогностичних факторів: ≤ 4 бали — низький ризик, 5–7 балів — помірний ризик, ≥ 8 балів — високий ризик.
нудоту, блювання, анорексію, втрату волосся, лейкопенію, гепатотоксичність і нефро токсичність. Для мінімізації побічних ефектів призначають лейковорин (кальцію фо лінат) через кілька годин після інфузії метотрексату.
При сприятливому прогнозі метастатична ГТХ звичайно лікується одним хіміотера певтичним агентом, при несприятливому прогнозі застосовується поліхіміотерапія (МАС: метотрексат, актиноміцин D і хлорамбуцил). Ефективність такого лікування становить 90–100 % для ГТХ зі сприятливим прогнозом і 50–70 % для ГТХ з несприятливим прогнозом.
Хірургія не відіграє значної ролі у лікуванні злоякісної гестаційної трофобластичної хвороби, за винятком трофобластної пухлини плацентарної площини, яка є нечутливою до хіміотерапії і підлягає лікуванню шляхом гістеректомії.
Променева терапія звичайно резервується для лікування віддалених метастазів у го ловному мозку та печінці.
Моніторинг хворих. Як і при інших формах ГТХ, ретельний моніторинг рівня β ХГЛ є необхідним при веденні хворих із злоякісною хворобою. Протягом цього періоду па цієнткам слід рекомендувати контрацепцію з метою точної оцінки рівня β ХГЛ.
Інвазивний занесок
Патогенез. Інвазивний занесок може бути наслідком малігнізуючої трансформації персистуючого доброякісного захворювання (75 %) або рецидиву ГТХ (25 % випадків). У разі інвазивного занеску, молярні ворсинки і трофобласт пенетрують локально міо метрій та інколи можуть досягати черевної порожнини. Незважаючи на цю обставину, інвазивний міхуровий занесок рідко метастазує.
228
