
- •Глава 1. Получение алкинов
- •Глава 2. Химические свойства алкинов
- •Глава 1. Получение алкинов
- •Карбидный метод
- •Получение алкингалогенидов
- •3.4 Реакции радикального присоединения
- •3.5 Реакции этинилирования
- •3.5.1 Получение ацетиленовых спиртов
- •3.5.2 Получение ацетиленовых эфиров и кислот
- •3.6 Реакции гидрирования
- •3.6.1 Гетерогенное гидрирование
- •3.6.2 Гомогенное гидрирование
- •3.7.2 Реакции окислительного расщепления
- •3.7.3 Реакции оксилительного сочетания
- •Реакции олигомеризации
- •Реакции полимеризации
- •3.9.3 Реакции циклообразования
- •Образование производных пиррола
- •Образование производных фурана
- •Образование прочих гетероциклов
3.4 Реакции радикального присоединения
В присутствии перекисей или других условиях, способствующих образованию свободных радикалов, присоединение к алкинам идет по радикальному механизму — против правила Марковникова (эффект Хараша):
![]()
По свободнорадикальному механизму* может протекать реакция алкинов с тиолами:
![]()
* — В присутствии оснований реакция идет по нуклеофильному механизму.
Аналогично происходит присоединение карбенов:
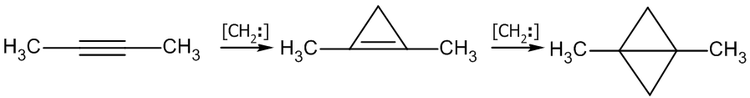
3.5 Реакции этинилирования
Реакциями этинилирования называют реакции увеличения углеродного скелета алкинов с сохранением тройной связи. Они могут протекать как по электрофильному, так и нуклеофильному механизму в зависимости от среды и условий реакции, характера субстрата, а также типа используемого катализатора.
3.5.1 Получение ацетиленовых спиртов
В присутствии сильных оснований алкины с концевой тройной связью способны присоединять карбонильные соединения с образованием спиртов (Реакция Фаворского):
![]()
Важнейшей реакцией из этой группы является присоединения формальдегида к ацетилену с образованием пропаргилового спирта и далее бутин-2-диола-1,4*:
![]()
![]()
* Бутин-2-диол-1,4 является важным промежуточным полупродуктом для получения бутиленгликоля, γ-Бутиролактона, изопрена итетрагидрофурана.
Эту реакцию разработал в 1925 году Реппе (Реакция Фаворского-Реппе). Она протекает при высоком давлении в присутствии ацетиленида меди.
3.5.2 Получение ацетиленовых эфиров и кислот
Ацетиленовые кислоты или их эфиры можно получить по реакции Цужи:
![]()
Катализаторы: PdCl2, CuCl.
3.6 Реакции гидрирования
3.6.1 Гетерогенное гидрирование
Гидрирование алкинов водородом на гетерогенных катализаторах, как правило, приводит к образованию цис-присоединения. Катализаторами гидрирования служат Ni, Pd, Pt, а также оксиды или комплексы Ir, Ru, Rh и некоторых других металлов.
На первой стадии образуется алкен, который практически сразу же гидрируется до алкана:

Для остановки реакции на стадии получения алкена используют катализаторы Линдлара (Pd/PbO/CaCO3) или борид никеля.
При гидрировании ацетилена на никель-кобальтовом катализаторе можно получить изобутилен:
![]()
3.6.2 Гомогенное гидрирование
Гомогенное гидрирование проводят в амидом натрия в жидком аммиаке или алюмогидридом лития в тетрагидрофуране. В ходе реакции образуются транс-алкены.

3.6.3 Гидроборирование
Алкины легко присоединяют диборан против правила Марковникова, образуя цис-алкенилбораны:
![]()
Реакция интересна тем, что далее алкенилбораны легко перевести в соответствующие цис-алкены простым действием уксусной кислоты:
![]()
или окислить H2O2 до альдегида или кетона:
![]()
3.6.4 Восстановительное карбоксилирование
По аналогии с реакциями алкенов, алкины вступают в реакцию восстановительного карбоксилирования. В зависимости от условий реакции и типов катализаторов, конечными продуктами могут стать спирты, альдегиды или алканы:
![]()
![]()
3.7 Реакции окисления
3.7.1 Реакции окислительного присоединения
Алкины окисляются более трудно чем алкены, однако при контролируемом окислении можно сохранить C-C связь и получить в качестве продуктов реакции карбонильные соединения:
![]()
В качестве окислителя может выступать озон (с последующим восстановлением и гидролизом озонида), KMnO4 в слабощелочной или нейтральной среде и некоторые другие вещества.
Ацетилен, в зависимости от окислителя может давать три продукта:
![]()
Глиоксаль — окисление разбавленной HNO3 в присутствии PdCl2 и NaNO2.
![]()
Глиоксалевая кислота — окисление KClO3 в субстрате вода+диэтиловый эфир.
![]()
Щавелевая кислота — окисление KMnO4 в кислой среде или HNO3 в присутствии PdCl2.
Отдельный тип реакций — реакции оксилительного карбоксилирования.
В растворах комплексов палладия образуются эфиры малеиновой кислоты:
![]()
