- •1. Загальні правила роботи в лабораторії
- •2. Запобіжні засоби і перша допомога при нещасних випадках
- •3. Основний лабораторний хімічний посуд
- •4. Зборка приладів
- •5. Миття і сушка хімічного посуду
- •5. Використання літератури і правила складання звіту
- •1. Нагрівання
- •2. Охолоджування
- •3. Вимірювання і регулювання температури
- •4. Подрібнення і перемішування
- •5. Розчинення і Властивості деяких органічних розчинників
- •6. Сушка і основні осушувачі
- •7. Фільтрування
- •1. Кристалізація
- •2. Возгонка (сублімація)
- •3. Екстракція
- •4. Перегонка
- •5. Хроматографія
- •1. Температура плавлення
- •2. Температура кипіння
- •3. Відносна густина
- •4. Показник заломлення
- •5. Молекулярна маса
- •1. Якісний аналіз
- •2. Фізико-хімічні методи встановлення структури речовини
- •3. Ідентифікація невідомої речовини
- •1. Відновлення воднем і реакції гідрУвання
- •2. Одержання металів, їх сплавів і деяких неметалів
- •Питомі теплові ефекти (q) відновлення оксидів алюмінієм
- •3. Одержання металів і деяких неметалів відновленням водних розчинів солей
- •4. Хлорування металів, неметалів і оксидів
- •5. Бромування металів і неметалів
- •6. Йодування металів, неметалів і оксидів
- •7. Одержання сульфідів, селенідів і телуридів
- •8. Нітрування. Одержання нітридів
- •9. Одержання карбідів
- •10. Термічне розкладання речовин з метою одержання оксидів
- •11. Зневоднення крісталогідратів
- •12. Одержання солей
- •1. НітрУвання
- •2. Нітрозування
- •3. Сульфування
- •4. Галогенування
- •5. Алкілювання
- •6. Ацилювання
- •7. ДіазоТуВаНня і Реакції діазосполук
- •8. АзоспОлуЧення
- •9. Відновлення
- •10. Окислення
- •11. Амінування
- •12. Гидроксилювання
- •13. Конденсація
- •14. Полімеризація і поліконденсація
Питомі теплові ефекти (q) відновлення оксидів алюмінієм
|
Оксид |
Питомий тепловий ефект, Дж |
Оксид |
Питомий тепловий ефект, Дж |
|
CuO |
4017 |
Fe3O4 |
3556 |
|
СгО3 |
6924 |
Мn3О4 |
2686 |
|
Со3О4 |
4184 |
V2O5 |
3364 |
|
СоО |
3316 |
Cr2O3 |
2444 |
|
NiO |
3284 |
Та2О5 |
1232 |
|
МоО3 |
4502 |
SiO2 |
2492 |
|
МоО2 |
3324 |
TiO2 |
1346 |
|
Fe2O3 |
3854 |
|
|
Коли в реакції беруть участь оксиди складу МеО, відносний вміст сплаву в продуктах реакції підвищується, тому коефіцієнт К має значення, рівне 0,8 – 0,9.
При відновлень оксидів алюмінієм метали і неметали утворюються в сплавленому вигляді і осідають на дно тигля. При використанні магнію, як відновника, метали утворюються у вигляді порошку. Пояснюється це тим, що оксид магнію, що утворюється, має високу температуру плавлення, під час реакції не розплавляється й ізолює один від одного окремі найдрібніші краплі металу. При практичному проведенні алюмотермічних реакцій необхідно дотримуватись правил ТБ і обережності.
Вихідні речовини (оксиди), а також реактор (тигель) необхідно заздалегідь просушити при 150 – 200°С (за наявності вологи спостерігається розкидання реакційної суміші). Після цього оксиди розтирають в порошок і просіюють на ситі. Алюміній беруть у вигляді дрібних крупинок. Порошкоподібний алюміній, що є у продажу під назвою алюмінієвої пудри, непридатний для алюмотермічних реакцій, оскільки він містить велику кількість окисленого металу; з якісними ж сортами такого не окисленого алюмінію реакції протікають дуже бурхливо, що знижує вихід одержуваного металу. Висушені і подрібнені вихідні речовини відважують на технічних терезах і ретельно перемішують. При проведенні реакції слід брати не менше 25 – 30 г вихідних речовин (сумарно). З великою кількістю речовин реакції йдуть ще краще, і вихід металів збільшується. Алюміній беруть у кількості, рівній теоретично розрахованому, і тільки в деяких випадках (вигорання алюмінію, одержання алюмінієвих сплавів) – більше теоретично необхідної кількості. Щоб отримати метал або сплав без алюмінію, слід брати його дещо менше теоретично розрахованої кількості (на 3 – 4%).
Приготування запалювальної суміші. Існує декілька рецептів приготування запалювальної суміші: 1) 9 мас.ч. розтертого пероксиду барію змішують з 1 мас.ч. порошкоподібного алюмінію; 2) беруть 3 мас.ч. розтертого нітрату калію і 1,3 мас.ч. алюмінієвої пудри; 3) готують суміш 4 мас.ч. розтертого пероксиду барію і 1 мас.ч. порошкоподібного алюмінію і додають 0,7 мас.ч. окремо розтертого хлорату калію. Запалювальну суміш зберігають у сухій, добре закупореній скляній банці, готувати її у великих кількостях не рекомендується.
Заповнення реактора шихтою. Як реактор використовують магнезіальні або корундові тиглі, оскільки вони термічно стійкі і речовини при роботі з ними менше забруднюються. Фарфорові тиглі, як правило, руйнуються. Тому їх потрібно поміщати в пісок, щоб розплавлена маса не виливалася. Більш зручні шамотові або глиняні тиглі, але в цьому випадку продукт забруднюється кремнієм і іншими речовинами.
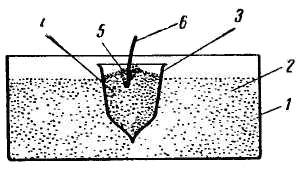
Тигель 1 (рис. 71) заповнюють на 3/4 його висоти сумішшю з оксиду і відновника, утрамбовують, роблять невелике заглиблення і засинають зверху тонким шаром (близько 1 – 1,5 мм) запалювальної суміші. Стрічку магнію 4 вставляють в заглиблення, яке потім заповнюють запалювальною сумішшю у формі гори. Якщо стрічка магнію покрита шаром оксиду, її слід очистити ножем. Реакцію можна проводити в піску або в оксиді магнію, заздалегідь прожарених. У такому матеріалі, насипаному в сталевий ящик, роблять заглиблення, в яке і поміщають реакційну суміш в паперовому кульку (рис. 72).
Запобіжні засоби. Зважаючи на те, що при реакції виділяється дуже багато теплоти і відбувається розкидання розжарених частинок, необхідно дотримувати запобіжні засоби. Реакцію проводять у витяжній шафі, звідки прибирають всі легкозаймисті матеріали. Тигель поміщають на пісок. Працюють в захисних окулярах.
Проведення досліду. Запалювальну суміш підпалюють за допомогою магнієвої стрічки. Якщо є магнієві стружки, то можна підпалити магній і кинути його на запалювальну суміш.
|
|
|
|
Рис. 71. Алюмотермічне відновлення оксиду в тиглі: 1 – тигель; 2 – суміш оксиду з алюмінієм; 3 – запалювальна суміш; 4 – стрічка магнію. |
Рис. 72. Алюмотермічне відновлення оксидів у піску: 1 – металевий ящик; 2 – пісок; 3 – паперовий кульок; 4 – суміш оксидів з алюмінієм; 5 – запалювальна суміш; 6 – стрічка магнію. |
Розділення продуктів реакції. Продукти реакції (метал і шлак) дуже міцно утримуються в тиглі. Тому після закінчення реакції тигель охолоджують, розбивають і «корольок» металу відділяють від шлаку. Іноді шматочки металу залишаються в шлаку у вигляді включень. У цьому випадку шлак потрібно розбити на шматочки і відібрати метал; шматочки шлаку, що пристав до металу, видаляють за допомогою молотка на сталевій плиті.
Вихід продуктів реакції. Вихід продуктів реакції в лабораторних умовах в кращому разі складає 80 – 90% від теоретичного. Найчастіше він складає 60 – 70%. Вихід у значній мірі визначається чистотою відділення металу від шлаку, в якому метал часто залишається у вигляді дрібних включень.