
- •1. Предмет і завдання курсу "біохімія"
- •2. Історія розвитку біохімії
- •3. Рівні структурної організації та хімічний склад живих організмів.
- •Відокремлюється тільки при хімічній взаємодії, зокрема при відщепленні гідроксильних (-он) груп від окремих молекул
- •Осмотичне утримування
- •Добова потреба організму у воді - 2,5...3,0 л.
- •4.Роль обміну речовин у життєдіяльності організму
- •1. Білки. Амінокислотний склад
- •2. Біологічна роль білків в організмі
- •3. Сучасні уявлення про структуру білків у білках розрізняють чотири рівні структурної організації:
- •4. Фізико-хімічні властивості білків
- •1. Нуклеїнові кислоти, їх хімічна природа
- •2. Відмінні властивості днк і рнк
- •3. Будова нуклеозидів та нуклеотидів
- •4. Атф - хімічна природа, біологічна роль
- •5.Структура нуклеїнових кислот
- •Тема 5. Ферменти
- •1. Ферменти як біологічні каталізатори
- •2. Хімічна природа та будова ферментів
- •3. Механізм дії ферментів та основи кінетики каталізу
- •4. Активність ферментів, вплив на неї різних факторів. Властивості ферментів
- •5. Номенклатура та класифікація ферментів
- •6. Використання ферментів у харчових технологіях
- •1. Класифікація вітамінів, їх біологічна роль
- •2. Будова вітамінів та їх добова потреба
- •3.Антивітаміни.Гормони
- •Тема 7. Основні поняття динамічної біохімії. Вільна енергія. Механізм дихального ланцюга
- •1. Динамічна біохімія. Вільна енерпя
- •(Окислення, відновлення, гідроліз, фосфорилювання таін.)
- •2. Біологічне окиснення. Тканинне дихання. Дихальний ланцюг
- •3. Окиснювальне фосфорилювання
- •Теми 8-9. Вуглеводи та їх обмін
- •1. Вуглеводи, їх функції
- •2. Класифікація вуглеводів
- •3. Характеристика основних представників вуглеводів
- •4. Перетравлювання та всмоктування вуглеводів в організмі людини
- •5. Взаємоперетворення моносахаридів в організмі
- •6. Анаеробне перетворення вуглеводів -хімізм гліколізу
- •7. Аеробне перетворення вуглеводів. Цикл кребса
- •8. Поняття про пентозний цикл перетворення вуглеводів
- •9. Біосинтез вуглеводів в організмі
- •9. Фотосинтез. Синтез оліго- та полісахаридів
- •25 – 30 Г/добу
- •Теми 10 -11. Ліпіди та їх обмін
- •1. Функції ліпідів в організмі
- •2. Класифікація ліпідів
- •3. Хімічна природа простих та складних ліпідів
- •4.Перетворення ліпідів у шлунково-кишковому тракті
- •5. Внутрішньоклітинний обмін ліпідів
- •6. Біосинтез ліпідів
- •Модуль 3 Тема 12. Білковий обмін
- •1. Перетворення білкових речовин у шлунково-кишковому тракті
- •2. Катаболізм білкових речовин в організмі. Хімізм перетворень
- •4. Синтез білків
- •Тема 13. Взаємозв'язок обмінних процесів
- •1. Взаємозв'язок основних видів обміну речовин
- •2. Ключові метаболіти - ланки переходу вуглеводного, білкового та ліпідного обмінів
- •2.Боєчко ф. Ф. Біологічна хімія. - к.: Вища шк., 1995. - 538 с.
- •3.Филиппович ю.Б. Основн биохимии. -м.: Висш. Шк., 1985. -503с.
- •4.Комов в.П., Шведова в.Н. Биохимия: Учеб. Для вузов. - м.: Дрофа, 2006. - 638с. Для студ Тмя та Тмо
Модуль 3 Тема 12. Білковий обмін
План
1.Перетравлювання білкових речовин у шлунково- кишковому тракті.
2. Катаболізм білкових речовин в організмі. Хімізм перетворень амінокислот.
3 .Детоксикація аміаку в організмі людини.
4. Синтез білків.
Література: [1,2,3,4, 6, 8].
Нові поняття, терміни: перетравлювання білків, гідроліз, пепсин, трипсин, ентерокіназа, карбоксипептидази, амінопептидази, хімозин, хімотрипсин, трансляція, дезамінування, декарбоксилювання, переамінування, азотний баланс, ген, триплети, кодон, антикодон, цистрон, комплементарність, рекогніція, ініціація, елонгація, термінація, процесінг, інтрон, білкова недостатність.
1. Перетворення білкових речовин у шлунково-кишковому тракті
Основним шляхом перетворення білків їжі є їх гідроліз (перетравлювання) до амінокислот.
В організмі постійно відбувається катаболізм і анаболізм білків.
Засвоєння білків залежить від кулінарної обробки, активності протеолітичних ферментів, амінокислотного складу білків.
Біологічно повноцінними є білки раціону, із 100 г яких може бути синтезовано 100 г білків організму.
Закон мінімуму Лібіха: якщо співвідношення незамінних амінокислот у складі білків відрізняється від оптимального на 20 %, то всі інші амінокислоти будуть також використовуватися на 20 % менше.
Загальна схема перетворення білків і амінокислот у тваринному організмі.

! Динаміку балансом азоту обміну білків в організмі характеризують балансом азоту
Перетравлювання білків

Розщеплення
білків у
шлунку - до пептидів і, у незначній
кількості, до амінокислот.
Ферментн -
пепсин, хімозин (у дітей

Розщеплення
пептидів у
дванадцятипалій кишці -до
оліго-, дипептидів, вільних амінокислот.
Ферменти
панкреатичного
соку (ферменти підшлункової залози):
трипсин, хімотрипсин

Розщеплення
продуктів гідролізу білків у
тонкій
кишці - до амінокислот.
Ферменти
слизової
оболонки кишок: ентерокіназа,
карбоксипептидази,
амінопептидази
► Продукти гідролізу білка - амінокислоти всмоктуються в кінцевій частині дванадцятипалої і на початку тонкої клубової
кишок і попадають у кров, а звідти — до клітин різних органів і, насамперед, до печінки.
!! Амінокислоти, які не всмокталися в тонкій кишці, а потрапляють у товсту кишку, піддаються різним перетворенням під дією ферментів мікроорганізмів. Цей процес дістав назву гниття білків. При цьому найбільш поширене декарбоксилювання та деякі інші види перетворень, які призводять до утворення з амінокислот токсичних речовин: амінів, індолу, скатолу, фенолу, крезолу.

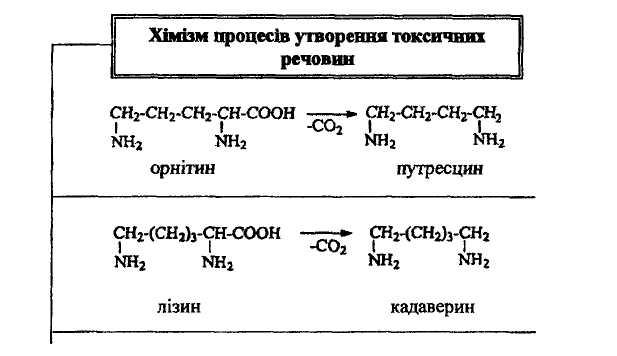

Токсичні продукти розкладу білків із товстої кишки частково всмоктуються у кров, попадають у печінку, де знешкоджуються.
2. Катаболізм білкових речовин в організмі. Хімізм перетворень
Амінокислоти до клітин надходять двома основними шляхами:
після перетравлювання
за рахунок реакцій переамінування з метаболітів вуглеводного та ліпідного обмінів
► Метаболічні перетворення амінокислот у клітинах організму відбуваються переважно як синтез білків і пептидів з
амінокислот. Крім того, ряд амінокислот є попередниками утворення сполук непептидної природи (пуринових і
піримідинових основ, біогенних амінів, нікотинової кислоти, порфіринів, в тому числі гема, тощо). Основним органом
метаболізму амінокислот є печінка.
Основні напрямки катаболізму вільних амінокислот реакції дезамінування
реакції декарбоксилювання
перетворення амінокислот за радикалом
Дезамінування амінокислот в живих організмах
► окиснювальне (утворюється кетокислота)
![]()
Є основним в організмі вищих тварин. Субстратом є глютамінова кислота:

► відновне - шляхом редукції під дією дегідрогеназ (утворюється насичена жирна кислота)

► гідролітичне - під дією відновних гідролаз (утворюється гідроксикислота)

►•внутрішньо-молекулярне - під дією відповідних ліаз (утворюється ненасичена кислота)
![]()
Дезамінування за 2 - 4 типами більш властиве грибам та рослинам
Біологічне окиснення амінокислот в організмі людини відбувається двома шляхами:
► пряме дезамінування (за хімізмом першої реакції)
► непряме, яке ще має назви трансдезамінування або переамінування (аміногрупа переноситься на кетокислоти)

Процес переамінування принципово ділиться на 2 етапи:
1) перенесення аміногруп з вільних амінокислот на кетокислоти, які є ключовими метаболітами (акцептори аміногруп - піруват, оксалоацетат, α-кетоглутарат). Реакції каталізуються відповідними - амінотрансферазами, кофакторами яких є похідна вітаміну В6 - піридоксальфосфат.
Мета першого етапу переамінування - зібрати аміногрупи вільних амінокислот, що підлягають біологічному окисненню, у амінокислоти одного типу (глутамінову кислоту).
2) процес окиснення лутамінової кислоти, який відбувається у мітохондріях під дією глутаматдегідрогенази.

Хімізм перетворення амінокислот за участю відповідних карбоксилаз
Декарбоксилювання



► Продуктами обміну амінокислот є карбонові кислоти, гідроксикислоти, кетокислоти, частина яких використовується під час синтезу нових речовин, а інша частина піддається р-окисненню, стисненню в трикарбоновому циклі Кребса до кінцевих продуктів - Н2О і СО2.
Аміни, що утворюються під час декарбоксилювання, мають високу біологічну активність, тому їх називають також біогенними амінами.
► Тканинними гормонами або нейрогормонами є серотонін, гістамін. Серотонін регулює функції нервової, серцево-судинної та м'язової систем, тиск крові. Бере участь у регуляції роботи органів дихання, травного каналу. Гістамін викликає секрецію соляної кислоти в шлунку, виявляє специфічну дію на нервові закінчення судин, зумовлюючи їх розширення і зниження тиску крові.
► γ-аміномасляна кислота відіграє важливу роль у функціональній діяльності центральної нервової системи.
3. МЕТОДИ ЗНЕШКОДЖЕННЯ АМІАКУ В ОРГАНІЗМІ людини
► Аміак, який утворюється як кінцевий продукт розщеплення амінокислот, є токсичною речовиною (шкідливо впливає на центральну нервову систему, порушує процеси тканинного дихання. Тому аміак миттєво нейтралізується з утворенням нетоксичних для організму сполук.
Одним із важливих методів знешкодження аміаку є взаємодія його з аспарагіновою і глутаміновою кислотами:
Схема перетворення аміаку
► синтез глутаміну та аспарагіну
► синтез амінокислот
► синтез сечовини (є основним шляхом для людини)
► синтез креатину
► утворення амонійних солей

► При взаємодії аспарагінової та глутамінової кислот з аміаком утворюються відповідні аміди. Обидві реакції відбуваються за участю енергії АТФ. Аспарагінова і глутамінова кислоти у клітинах зв'язують аміак.
Аміак у складі аспарагіну і глутаміну надходить у печінку, де з нього синтезується сечовина, яка є кінцевим продуктом азотистого обміну уреотелічних тварин (більшості хребетних).
!! Синтез сечовини - ферментативний процес, який здійснюється із затратою енергії АТФ.
Орнітиновий цикл - синтез сечовини

Орнітин знову може вступати в реакцію з карбамоїлфосфатом. Цикл повторюється. Більшість ферментів орнітинового циклу знаходяться в мітохондріях клітин печінки. Сечовина виділяється з клітин печінки в кров, переноситься в нирки і виділяється з організму з сечею.
