
Клиническая аллергология_учебное пособие_2007
.pdfхимические соединения, такие как изоцианаты, ангидриды, хром, никель, формальдегид и другие, а также некоторые лекарственные средства выступают в качестве гаптенов, способных связываться с белками и вызывать образование IgEантител.
Аллергены обычно не имеют совсем или имеют очень низкую токсичность (исключение составляют компоненты ядов некоторых насекомых), но могут спровоцировать развитие патологической реакции из-за их способности индуцировать IgE-опосредованный иммунный ответ, а после повторного попадания в организм вызвать IgE-зависимые и/или T-лимфоцитзависимые реакции гиперчувствительности.
Аллергены имеют названия в соответствии с рекомендациями ВОЗ (1994) и Комиссии по спецификации аллергенов при международном союзе иммунологов. Названия включают первые три буквы из названия рода и первую букву (или первые две буквы) из названия разновидности, к которой принадлежит аллерген, плюс арабская цифра для обозначения структурно идентичных аллергенов различной разновидности. Например, структурно подобные аллергены (антиген 5) от двух разновидностей ос Vespula – V. vulgaris и V. Vidua – обозначены Ves v 5 и Ves vi 5 соответственно. Четыре дополнительных числа могут быть использованы для идентификации варианта аллергена (изоаллергена). Например, из Ambrosia artemisiifolia получены четыре изоаллергена, два из которых являются вариантами первого и обозначаются Amb 1.01, Amb 1.0101 и Amb 1.0102, Amb 1.02.
Доза аллергена, необходимая для развития сенсибилизации и индукции клинических проявлений аллергического заболевания у атопика чрезвычайно мала. Установлено, что для формирования респираторного аллергоза предрасположенному к аллергии человеку достаточно ингалировать всего несколько микрограмм пыльцы в год.
Почему некоторые антигены являются аллергенами, а другие нет? К сожалению, в этом вопросе нет ясности, однако проводимые в настоящее время исследования структуры аллергенов, их идентификация и клонирование расширили наши представления о свойствах аллергенов и причинах их аллергенности.
Причины аллергенности
Антигенная мимикрия аллергенов с ферментами паразитов
Характер иммунных ответов на паразитарную инвазию (рисунок 2) и на многие безвредные антигены окружающей среды практически идентичен. Это поддерживает широко известное представление о том, что нежелательные IgEопосредованные иммунные ответы – это неудачный результат иммунной реакции на безопасные по существу аллергены, так, как будто они представляют паразита.
Многие из аллергенов – ферменты, поэтому предполагается, что способность
11

вызывать сильные ответы Th2-типа на ферменты развилась под давлением естественного отбора, который «поддерживал» развитие адекватного иммунного противопаразитарного ответа. Ферменты необходимы паразитам для успешного проникновения через тканевые барьеры организма и перемещения в межклеточном пространстве. В результате ферменты стали своего рода визитной карточкой паразитарной инфекции. Следствием этого явилось распространение IgE-опосредованного ответа на схожие с паразитарными, но "безвредные" ферменты, производимые растениями, насекомыми и животными.
LTC4, PAF,
простогландины, провоспалительные цитокины
Тромбоцит Эозинофил Макрофаг
Гельминт |
|
Тучная клетка |
|
|
|
Медиаторы, вызывающие вазодилятацию повышающие сосудистую проницаемость, стимулирующие секрецию слизи
Рисунок 2. В ответ на паразитарную инвазию происходит переключение иммунного ответа на Th2–тип, стимулируется выработка IgE, который армирует макрофаги и, возможно, эозинофилы, способствует дегрануляции тучных клеток с развитием местной воспалительной реакции.
Аллергены способны стимулировать продукцию IL-4 или IL-13
Установлено, что выделяемые паразитами ферменты и функционально схожие с ними, но безвредные аллергены другой природы, могут вызывать развитие ответов Th2-типа, непосредственно стимулируя синтез IL-4 или IL-13 тучными клетками, базофилами, T-лимфоцитами или другими клетками – потенциальными источниками этих цитокинов (рисунок 3).
12

Der p 1 способен «удалять» CD23 с поверхности В-лимфоцитов
Описаны другие механизмы, повышающие аллергенность. Например, Der p 1, протеолитически активный аллерген домашнего клеща Dermatophagoides pteronyssinus, способен «удалять» молекулы CD23 (FcεRII) с поверхности В- лимфоцитов. Вследствие этого В-лимфоциты утрачивают способность отвечать на сигнал, угнетающий выработку IgE, который возникает при связывании циркулирующих молекул IgE с FcεRII.
IL-4, IL-13
Аллерген
Рисунок 3. Аллерген напрямую воздействует на тучную клетку, стимулируя продукцию цитокинов, способствующих переключению иммунного ответа (преимущественной активации Th2-лимфоцитов).
Аллергены могут непосредственно взаимодействовать с рецепторами на антигенпрезентирующих клетках
Олигосахаридные цепи некоторых гликопротеиновых аллергенов могут непосредственно взаимодействовать с лектиновыми рецепторами на антигенпрезентирующих клетках. Таким образом, аллерген аккумулируется на поверхности клетки, и презентация его В-лимфоцитам усиливается.
Клиническая классификация аллергенов
Существует множество классификаций аллергенов. Мы приводим одну из них, основанную на особенностях их происхождения и способа попадания в организм. Выделяют следующие группы аллергенов:
Ингаляционные (аэроаллергены) – растительного и животного происхождения.
Пищевые.
Инсектные.
Лекарственные.
Инфекционные.
Промышленные.
13
Аэроаллергены
Воздушные аллергены представляют собой довольно крупные частицы (диаметр 2–60 мкм) сложного строения (пыльца, плесневые грибы, водоросли, микроклещи, частицы насекомых и растений, эпидермис животных и т. д.), которые могут вызывать аллергические реакции при попадании в дыхательные пути (перечень растительных аэроаллергенов, распространенных в Беларуси представлен в приложении 4). Собственно аллергеном является не вся частица, а лишь некоторые входящие в ее состав вещества, как правило, белки или гликопротеины с молекулярной массой 10–40 кД. Большинство из них способно длительно существовать в окружающей среде, не утрачивая аллергенности. Они хорошо растворимы в водной среде, что позволяет им быстро распространяться в слизи и других биологических жидкостях.
Углеводороды, промышленная пыль, неорганические кристаллы и газообразные вещества (хлор, сероводород, пары формальдегида и бензина, древесный и табачный дым, продукты сгорания органических веществ, дизельного топлива) сами по себе не иммуногенны. Однако они повышают чувствительность дыхательных путей к аллергенам, могут служить причиной развития гиперреактивности и, вероятно, оказывают влияние на течение аллергических заболеваний за счет непосредственного токсического воздействия на различные звенья иммунной системы.
Антигенность воздушных аллергенов определяется их размером, формой и химическим строением. Клинические проявления аллергии часто связаны со спецификой аэроаллергена. Например, пыльцевые аллергены типично связаны с аллергическим ринитом, а аллергены из фрагментов тараканов, клещей, а также из шерсти, перхоти и слюны кошек в большей степени являются фактором риска развития бронхиальной астмы.
Пищевые аллергены
Аллергия может возникнуть практически к любому пищевому продукту, однако более чем в 90% случаев развитие пищевой аллергии вызывают яйца, коровье молоко, пшеница, кукуруза, арахис, лесные орехи, рыба, ракообразные, моллюски. Аллергические реакции на пищевые аллергены могут протекать в любой форме и даже вызвать фатальную анафилаксию.
Пищевые аллергены обычно имеют молекулярную массу 10–70 кД, они относительно устойчивы к температурной денатурации, вывариванию, кислотному гидролизу и протеолизу. Часть из них обладает антипротеолитической активностью (например, рыбные аллергены). Однако, есть «приятные» исключения: например, большинство аллергенов из свежих фруктов и овощей термолабильны.
Трудности в установлении причины пищевой аллергии связаны с тем, что нередко наблюдаются перекрестные аллергические реакции между разными
14
продуктами, а также пищевыми и аэроаллергенами. Наиболее часто перекрестные реакции наблюдаются на продукты, представленные в таблице 1.
Пищевые красители также вызывают аллергические или сходные с ними реакции. Чаще всего их вызывает желтый краситель тартразин, который присутствует в продуктах и фармацевтических препаратах (входит в состав оболочки таблеток), имеющих оранжевый или желтый цвет. Ароматизаторы и консерванты, например глутамат натрия, нитриты, нитраты, бензоат натрия, сульфиты также часто вызывают аллергические реакции. Больше всего их содержат вина, пиво, ликеры, наливки, фруктовые соки и безалкогольные напитки, смеси для выпечки, колбасный фарш, маринады и соления, консервы, сыры (перечень пищевых добавок, используемых в пищевой промышленности, приведен в приложении 3).
Таблица 1. Продукты, дающие перекрестные аллергические реакции
Яблоко |
Картофель, морковь, пыльца березы |
Морковь |
Яблоко, пыльца березы, рожь, пшеница, авокадо, ананас |
Пшеница |
Рожь, ячмень, овес, кукуруза, дикие злаки, пыльца злаков |
Треска |
Угорь, скумбрия, форель, тунец, окунь, камбала, пикша |
Коровье молоко |
Козье молоко, кобылье молоко |
Яйцо |
Лизоцим, аэроаллергены птиц (пух, перхоть и т.д.) |
Чеснок |
Лук, аспарагус |
Мед |
Пыльца растений |
Бобы |
Соя, арахис, чечевица, фенхель |
Персики |
Абрикосы, сливы, бананы |
Креветки |
Крабы, омары, речные раки, домашний клещ |
Реакции на пищу также могут быть обусловлены прямыми биологическими эффектами ее компонентов (неаллергическая гиперчувствительность), например, гистамина (содержится в некоторых сортах рыбы), кофеина и теобромина (входят в состав многих тонизирующих напитков), растительных лектинов, содержащихся во многих фруктах и ягодах, например в клубнике. Эти вещества, связываясь с соответствующими рецепторами на тучных клетках, могут вызывать их дегрануляцию.
Яды насекомых
Содержат аллергены, многие из которых являются ферментами, способными стимулировать IgE-ассоциированные ответы у людей даже при отсутствии атопии. Укусы разновидностей Hymenoptera (пчелы, шершни и т.д.) – одна из наиболее частых причин анафилаксии. Это объясняется тем, что внутрикожно и/или подкожно вводятся относительно большие количества яда (приблизительно 50 мкг). Это сравнимо со средней дозой пыльцевых аллергенов вдыхаемых человеком ежегодно. Кроме того, аллергены разных видов Hymenoptera вызывают перекрестную сенсибилизацию.
15
Фармацевтические препараты
Аллергенные свойства лекарственных средств (ЛС) в значительной мере зависят от их химического строения, молекулярной массы и сложности молекулы. Сыворотки, химопапаин, стрептокиназа, аспарагиназа, инсулин относятся к полноценным антигенам. У веществ с молекулярной массой менее 4 кД иммуногенность низкая или отсутствует вовсе. Большинство ЛС – это простые органические вещества с молекулярной массой менее 1 кД, побочные эффекты на прием и введение таких лекарств часто обусловлены неаллергической гиперчувствительностью (аспириновая триада, реакции на введение рентгеноконтрастных веществ и т.д.). Некоторые ЛС являются гаптенами и приобретают иммуногенность только после связывания с макромолекулярными носителями, в качестве которых выступают белки организма, чаще альбумин, причем гаптенами часто являются не сами ЛС, а их метаболиты. Это создает определенные трудности в диагностике лекарственной аллергии при верификации причинно значимого фактора. Кожные пробы и другие лабораторные тесты, которые проводят с неизменёнными ЛС, как правило, дают отрицательные результаты.
Появление специфических AT выявлено у большинства больных, принимавших пенициллин и инсулин, но обычно это не сопровождается аллергическими реакциями или снижением эффективности указанных ЛС.
Механизмы, обуславливающие предрасположенность к аллергическим реакциям
Специфический аллерген по определению не вызывает аллергические реакции у большинства людей. Однако отдельные индивидуумы (атопики) имеют предрасположенность к развитию сильных IgE-опосредованных ответов, причем, могут давать их на множество различных аллергенов. С чем же связан риск развития аллергических реакций? Считается, что предрасположенность к аллергическим реакциям обусловлена особенностями организма и определяется:
склонностью к Th2-зависимым реакциям, приводящим к повышенной продукции IgE,
рестриктированностью иммунного ответа на аллергены системой HLA (DP и DR),
особенностями расположения генов, кодирующих медиаторы и рецепторы, ответственные за развитие аллергических реакций.
Причины повышенной продукции IgE
В 1921 Prausnitz и Kustner продемонстрировали, что введение сыворотки, полученной у больного с аллергией к рыбе, под кожу индивидууму, не имеющему аллергии, приводит к развитию у последнего сенсибилизации. Через 24 часа после
16

внутривенного введения рыбного антигена у сенсибилизированного возникает аллергическая реакция на участке кожи, куда ранее была введена сыворотка больного. Сывороточный фактор, ответственный за передачу аллергии, был назван реагином.
В 1966 году Ишизака установил, что реагины – это иммуноглобулины нового, неизвестного до того времени класса, названные впоследствии IgE (рисунок 4).
Константный фрагмент (Fc)
Антигенсвязывающий фрагмент (Fab)
Fc
Рисунок 4. Строение молекулы IgE
Концентрация IgE в сыворотке крови здорового взрослого человека составляет 87–350 нг/мл, тогда как у лиц с атопическими заболеваниями она может быть на несколько порядков выше. IgE практически отсутствует у новорожденных, с 2–3 месяцев его концентрация постепенно возрастает, но у здоровых годовалых детей содержание IgE не превышает 40 нг/мл и только к 10 годам жизни приближается к уровню взрослых. В секретах содержание IgE примерно в 10 раз выше, чем в сыворотке крови; особенно много его в молозиве. Даже в моче оно выше, чем в крови. Установлено, что бóльшая часть IgE секретируется в лимфоидной ткани, ассоциированной со слизистыми оболочками. Сывороточный IgE имеет короткий срок полужизни, измеряемый несколькими сутками. В результатах лабораторного обследования концентрация IgE приводится либо в весовых единицах (нг/мл), либо в единицах активности (МЕ/мл); 1 МЕ равна 2,42 нг.
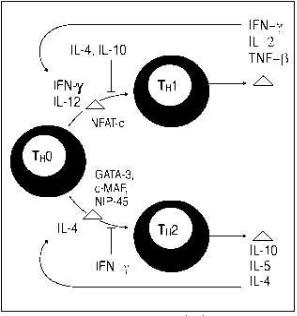
Индукция синтеза IgE обеспечивается цитокинами, продуцируемыми CD4+ лимфоцитами (Th). Эти лимфоциты подразделяются на Th1 и Th2 на основании профиля цитокинов, которые они производят. Th1 являются главным источником IL-2, IFN-γ и TNF- , т.е. цитокинов, имеющих большое значение в развитии клеточного компонента иммунного ответа. Th2 секретируют IL-4, IL-5, IL-6, IL-10 и IL-13, которые важны для развития гуморальных реакций, в том числе IgEопосредованных (рисунок 5).
Большинство иммунных болезней трудно классифицировать в зависимости от преобладающего типа реакции (Th1 или Th2), но при аллергических заболеваниях, также как и при IgE-ассоциированном противопаразитарном ответе явно преобладают Th2-зависимые реакции.
Почему наивные Т-лимфоциты (Th0) превращаются в Th2 не до конца понятно, однако известно, что способствует этому ряд факторов:
17
тип антигенпрезентирующей клетки – В-лимфоцит,
высокое количество антигена,
низкая «активность» презентации антигена наивной Т-клетке,
микроокружение слизистых,
повышенная концентрация цитокинов, вырабатываемых Th2 и низкое содержание продуктов, секретируемых Th1.
Рисунок 5. Сигналы, регулирующие образование Th1 и Th2
B-лимфоциты усваивают, обрабатывают аллерген и представляют его в комплексе с молекулами MHC II класса Th2-клеткам. Th2-клетки, распознавшие комплекс пептид–MHC-II активируются и обеспечивают B-клетки двумя критическими для синтеза IgE сигналами:
первый – секреция IL-4 (и/или 13) активированными Th2;
второй – взаимодействие CD40L, экспрессированных на поверхности Th2, и CD40, экспрессированных на поверхности B-клеток.
То, что В-лимфоцит играет основную роль в презентации аллергенов в первую очередь обусловлено тем, что аллергены обладают высокой растворимостью. При контакте со слизистой они быстро растворяются в слизи, легко диффундируют в межклеточную среду и быстро накапливаются в высокой концентрации, а захват и презентация растворимых антигенов является прерогативой В-лимфоцитов.
Среди многих факторов, под влиянием которых на ранней стадии иммунного ответа осуществляется индуцированная аллергеном дифференцировка Th0 в Th2, основным является IL-4. Наличие в среде этого цитокина в дебюте процесса
18

дифференцировки является необходимым условием. Клеточный источник этого «раннего IL-4» пока не ясен, но, возможно, им являются T-клетки с фенотипом CD1+CD4+. Было показано, что эти клетки сразу после активации in vivo начинают производить большие количества IL-4. Другие потенциальные кандидаты – тучная клетка, базофил и эозинофил.
IL-4 вырабатывается активированными T-лимфоцитами, тучными клетками, базофилами, имеет много сходных биологических свойств с IL-13. Эти цитокины индуцируют активацию B-клеток, обеспечивают переключение синтеза иммуноглобулинов с класса M на IgE и стимулируют продукцию последнего. Переключение происходит через промежуточную фазу – продукцию IgG4. Производство IgG4 и IgE подчиненно одинаковым регулирующим сигналам, таким образом, изменение их уровня обычно происходит параллельно.
Стимулируют синтез IgE IL-5, IL-6, IL-9, TNF-α и MIP-1α (макрофагальный воспалительный протеин). Подавляют его синтез, по крайней мере, при некоторых обстоятельствах IFN-γ, IFN-α, IL-8, IL-10, IL-12 и трансформирующий фактор роста-β.
Хотя и IL-4, и IL-13 могут стимулировать транскрипцию генов, кодирующих IgE, но продукция зрелого mRNA и IgE B-клетками требует физического взаимодействия с другими клетками. Это реализуется при взаимодействии CD40 на B-клетках с его лигандом CD40L, который экспрессируется на активированных T-лимфоцитах, а также некоторых других клетках: базофилах, эозинофилах, тучных клетках. Последние в результате активации аллергеном могут экспрессировать CD40L и производить IL-13 и IL-4 и теоретически способны «подменять» T-клетки в развитии IgE-ассоциированных иммунных реакций (рисунок 6). Такие эффекты наблюдаются в тканях, избыточно обеспеченных тучными клетками, базофилами и эозинофилами. Вероятно, по этой причине микроокружение слизистых является идеальной средой, поддерживающей IgEответ.
В-лимфоцит
Тучная клетка |
|
В-лимфоцит |
|
|
|
Рисунок 6. Активированные тучные клетки продуцируют IL-4 и экспрессируют CD40L, что позволяет им стимулировать продукцию IgE.
19
Нарушать соотношение Th1/Th2 в сторону преобладания Th2 и таким образом способствовать IgE-ответу, могут некоторые вирусные антигены. Так, например, известно, что при инфицировании респираторно-синцитиальным вирусом образуются IgE-антитела, специфичные к антигенам данного вируса. Вероятно, свойством респираторно-синцитиального вируса подавлять активность Th1 объясняется высокая заболеваемость бронхиальной астмой среди лиц перенесших на первом году жизни бронхиолит респираторно-синцитиальной этиологии.
С другой стороны установлено, что конституционно повышенная экспрессия Toll-подобных рецепторов (Toll-like receptors – TLR) 2 и 4 типов на лейкоцитах «препятствует» возникновению аллергических заболеваний. Связывание этих рецепторов с гликопротеинами и липополисахаридами, являющимися компонентами стенок соответственно Гр+ и Гр– бактерий, вызывает активацию транскрипционного фактора NF- , который запускает синтез ряда цитокинов и в первую очередь интерферонов. Таким образом, у лиц с повышенной экспрессией TLR 2 и 4 типов контакты с бактериальной инфекцией (а эти контакты происходят постоянно) способствуют подавлению активности Th2 и уменьшают вероятность возникновения IgE-опосредованных реакций.
Рестриктированность иммунного ответа на аллергена по DP и DR
Антигенные фрагменты аллергенов, как и фрагменты любых других экзоантигенов, представляются рецептору T-клетки в составе с молекулами главного комплекса гистосовместимости класса II (MHC-II). Было установлено, что гены в пределах региона HLA-D короткого плеча 6-й хромосомы связаны с антигенспецифическим IgE-ответом. Доказано, что иммунные ответы на многие клинически важные аллергены (райграсс, клещи, амброзия и т.д.) рестриктированы по DP и DR.
Таким образом, презентация этих аллергенов и соответственно продукция специфических IgE возможна только у лиц, имеющих соответственный набор аллельных вариантов генов HLA.
Генный контроль продукции IgE
Общий сывороточный IgE представляет собой совокупность антигенспецифических иммуноглобулинов. Высокий уровень общего IgE тесно ассоциирован с выраженностью клинических проявлений аллергического заболевания. Близнецовый метод свидетельствует, что концентрация IgE находится под жестким контролем генетических факторов. Генетическое картирование позволило показать, что многие гены, кодирующие факторы, имеющие значение в патогенезе аллергических заболеваний, сосредоточены на ограниченной области 5 хромосомы (регион q3l–33). В этом регионе в тесном
20
