
- •Электродные потенциалы
- •1. Понятие об электродных потенциалах
- •2. Водородный электрод. Газовые электроды.
- •3. Стандартные электродные потенциалы. Ряд напряжений
- •4. Потенциалы окислительно-восстановительных реакций
- •5. Измерение стандартных электродных потенциалов
- •6. Теория гальванических элементов; явления поляризации и деполяризации
- •Если цинк погружён в 1 м раствор сульфата цинка, а медь — в
- •7. Анодное окисление и катодное восстановление. Явления перенапряжения.
- •8. Последовательность разряда ионов
- •9. Законы Фарадея
- •Рассмотрим несколько примеров электролиза
- •11. Аккумуляторы
- •Коррозия металлов и борьба с ней
- •13. Типы коррозии металлов
- •14. Факторы, определяющие интенсивность коррозии металлов
- •15. Методы защиты металлов от коррозии
7. Анодное окисление и катодное восстановление. Явления перенапряжения.
Одностороннее движение ионов при прохождении электрического тока (подаваемого от внешнего источника) через электролит, сопровождающееся разрядом положительных ионов на катоде (процесс восстановления) и отрицательных ионов на аноде (процесс окисления), называется электролизом. В результате электролиза на электродах выделяются продукты окисления и восстановления, которые могут вступать в реакции с окружающей средой (вторичные процессы при электролизе).
Для осуществления электролиза к отрицательному полюсу внешнего источника постоянного тока присоединяют катод, к положительному полюсу — анод и погружают их в раствор или расплав электролита. В большинстве случаев электроды бывают металлические, но применяются и неметаллические, проводящие ток электроды, например, графитовые
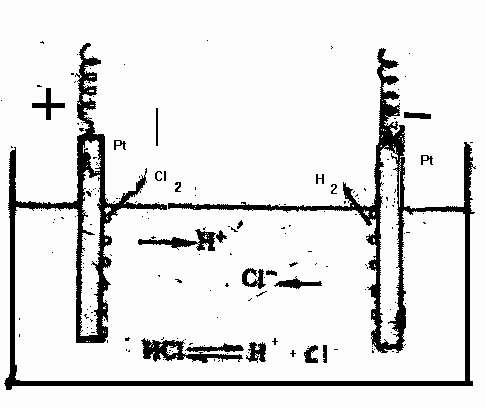
Рис. 6. Схема электролиза раствора НСl
Металлические аноды могут быть растворимыми (при электролизе они посылают в раствор свои ионы) и нерастворимыми (служат только для передачи электронов)
Рассмотрим схему электролиза раствора хлористого водорода с платиновыми нерастворимыми электродами (рис. 8).
На катоде идет процесс восстановления:
2Н+ +2е-=Н2;
образующийся водород выделяется в виде газа.
На аноде идет процесс окисления :
2Сl- = С12 + 2e-
выделяется газообразный хлор.
Катодное перенапряжение – это дополнительное напряжение, прикладываемое к катоду, при этом потенциал анода смещается далее в отрицательную сторону, а анодное – к аноду, при этом потенциал анода смещается далее в положительную сторону. Потенциал электрода, через который пропускается ток, Еi отличается от потенциала того же электрода без тока Е0. В общем случае, когда на электроде могут протекать несколько реакций, например на катоде с водным раствором электролита может протекать разряд ионов металла и разряд ионов водорода, разность потенциалов Еi – Е0 называют поляризацией. Перенапряжение затрудняет протекание электродного процесса и вызвано
Если же при электролизе на электроде протекает только одна реакция, например разряд ионов металла на катоде то величина Еi – Е0 равна перенапряжению η и в этом случае величина поляризации и перенапряжения совпадают. Перенапряжение на катоде, например, обусловлено тем, что переход гидратированного иона из водного раствора на катод связан с затратами энергии, (отсюда –перенапряжение, то есть, смещение напряжения на катоде в отрицательную сторону) на перенос ионов металла из раствора к поверхности катода; на разряд катионов с протеканием тех или иных химических процессов нарпример.ь дегидратации ионов. на внедрение образовавшихся атомов металла в кристаллическую решётку катодного отложения.
Перенапряжение, как катодное, так и анодное, так и анодное, зависит от материала электродов, состояния их поверхности, от природы разряжающихся на электроде ионов и на единицу площади поверхности электрода (плотность тока) Особенно большое значение имеет катодное перенапряжение выделения водорода. на платине оно близко к нулю. в то время как на других электродах имеет значительную величину. Напряжение разложения – общее напряжение, прилагаемое к электролитической ячейке, напряжение внешнего источника электричества, при котором начинается электролиз.
