
- •30.Материальный баланс массообмена.
- •31.Местные гидравлические сопротивления. Виды и конструкции запорных устройств.
- •32.Механическое перемешивание жидких сред. Конструкции мешалок и основы их расчета.
- •33.Многокорпусное выпаривание: материальный и тепловой баланс.
- •34. Мокрая и инерционная очистка газовых неоднородных систем.Конструкция аппаратов.
- •35.Молекулярный механизм переноса субстанции,элементарные законы переноса различных субстанций.
- •36. Образование и движение капель и газовых пузырей
- •37. Объемные коэффициенты масоотдачи и массопередачи.
- •38.Однокорпусное выпаривание: материальный и тепловой балансы.
- •39.Определение числа массообменных тарелок с помощю кинетической кривой.
- •40.Осаждение твердых частиц в поле центробежных сил. Циклоны и осадительные центрифуги.
- •41 Осевые и вихревые насосы.
- •42. Основное уравнение центробежных машин.
- •43.Основные рабочие параметры насосов.
- •44.Основне характеристики центробежных насосов.
- •45.Основы динамики потоков жидкость – жидкость
- •46. Особые случаи ректификации.
- •47.Параллельное и последовательное соединение двух центробежных насосов.
- •48. Перегонка жидкостей, равновесие в системе пар-жижкость
- •49. Перемешивание, виды перемешивания, интенсивность и эффективность перемешивания.
- •50.Периодическая ректификация. Виды.
- •51.Пленочное движение жидкости.
- •52.Пленочные массообменные и выпарные аппараты.
- •53. Подобие гидродинамических процессов
- •Подобие массообменных процессов.
- •56 Подобие тепловых процессов.
- •56.Полезная разность температур многокорпусной выпарной установке и ее распределение по корпусам.
- •57.Понятие теоретической тарелки. Эффктивность тарелки по Мерфи.
- •58.Поршневые насосы:конструкции и схемы установки.
- •59. Примеры применения в технике уравнения Паскаля (гидростатика) и Бернулли.
- •60.Проблемы масштабного перехода для промышленных аппаратов. Понятие сопряженного моделирования.
- •61. Процесс абсорбции:общие понятия, равновесие при абсорбции.
- •Равновесие при абсорбции. Закон Генри.
- •62.Процессы жидкостной экстракции
- •63.Процессы простой перегонки, основные виды.
- •64. Процессы сжатия газа в идеальной компрессорной машине. Мощность компрессора.
- •65.Псевдо и гидротранспорт зернистых материалов, понятие и основные виды. Гидродинамика зернистого слоя
- •66. Псевдоожижженый слой, скорость начала псевдоожижжения
- •Режим псевдоожижения
- •Скорость осаждения (витания)
- •67.Работа центробежного насоса на сеть, регулирование подачи центробежного насоса.
- •69Разделение неоднородных систем в поле центробежных сил:конструкции аппаратов.
- •70. Разделение неоднородных систем в поле сил тяжести. Конструкции аппаратов гравитационного разделения.
- •71.Расчет скорости осаждения и уноса.
- •72.Регенеративные и смесительные теплообменники
- •73.Ректификация:схема установок непрерывной и периодической ректификации
- •74. Сжатие и перемещение газов. Классификация компр.Машин
- •75Тепловой баланс в ректификационной колонне.
- •76. Тепловые депрессии в выпарных аппаратах.
- •77.Теплоносители : понятие виды и сферы применения.
- •78) Теплообмен при кипении жидкости
- •79) Теплообмен при конденсации паров
- •80.Теплообмен с телами сложной формы.
- •81.Технологический расчет аппаратов с непрерывным контактом фаз
- •82Технологический расчет аппарата со ступенчатым контактом фаз.
- •83.Турбулентное движение жидкости по трубам.Формула Дарси-Вейсбаха Режимы движения жидкости
- •Определение гидравлических сопротивлений в прямых трубах (определение путевых потерь)
- •Турбулентный механизм.
- •85.Урощенные модели массоотдачи Упрощенные модели массоотдачи.
- •Уравнения Бернулли
- •Физический (энергетический) смысл уравнения Бернулли
- •Уравнение Бернулли для потока реальной (вязкой) жидкости
- •88.Уравнение конвективного переноса импульса (уравнение Навье-Стокса)
- •89.Уравнение конвективного переноса теплоты (уравнение Фурье-Киргоффа)
- •–Уравнение Фурье-Кирхгофа.
- •90.Фазовые равновесия при массобмене
- •2.3.1.Математическое моделирование.
- •2.3.2 Физическое моделирование.
- •2.3.2.1 Теория подобия.
- •92.Фильтрование в поле центробежныз сил конструкции центрифуг.
- •93/ Число и высота единиц переноса
61. Процесс абсорбции:общие понятия, равновесие при абсорбции.
Абсорбцией называется процесс поглощения газов или паров из газовых или парогазовых смесей жидким поглотителем – абсорбентом. Если поглощаемый газ – абсорбтив – химически не взаимодействует с абсорбентом, то такая абсорбция физическая, если же абсорбтив образует с абсорбентом химическое соединение, то такой процесс называется хемосорбцией. Физическая абсорбция обратима, выделение поглощаемого газа из раствора – десорбция. Сочетание абсорбции и десорбции позволяют многократно использовать поглотитель и выделять поглощённый газ в чистом виде.
Абсорбция применяется:
— для получения готового продукта (абсорбция SO3 в производстве серной кислоты, абсорбция HCl, оксидов азота водой в производстве азотной кислоты);
— для выделения ценных компонентов из газовых смесей (абсорбция бензола из коксового газа и др.), при этом абсорбцию проводят в сочетании с десорбцией;
— для очистки газовых выбросов от вредных примесей;
— для осушки газов.
Равновесие при абсорбции. Закон Генри.
Система
состоит из трёх компонентов (распределяемое
вещество и два распределяющих вещества)
и двух фаз – жидкой и газовой. Для
абсорбции переменными являются Т, р,
концентрация компонента А в газовой и
жидкой фазах. Следовательно, в состоянии
равновесия при Т=const
и постоянном общем давлении зависимость
между парциальным давлением газа А или
его концентрацией и составом жидкой
фазы однозначна. Эта зависимость
выражается законом Генри: парциальное
давление
 растворённого газа пропорционально
его мольной доле
растворённого газа пропорционально
его мольной доле в растворе:
в растворе:
 (где
(где
 - парциальное давление поглощаемого
газа над раствором, находящегося в
равновесии, при концентрации раствора
- парциальное давление поглощаемого
газа над раствором, находящегося в
равновесии, при концентрации раствора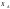 ,
Е – константа Генри. Е не зависит от
общего давления в системе, но зависит
от природы абсорбента и поглощаемого
газа, а также от Т.
,
Е – константа Генри. Е не зависит от
общего давления в системе, но зависит
от природы абсорбента и поглощаемого
газа, а также от Т.

Для
идеальных растворов зависимость
равновесных концентраций от давления
изображается прямой, т.к.

Чем
больше Т, тем меньше растворимость.
 - равновесная концентрация газа в
растворе, т.е. растворимость.
- равновесная концентрация газа в
растворе, т.е. растворимость.
Если
 –
мольная доля извлекаемого компонента
А в газовой смеси и р – общее давление
в системе, то парциальное давление
–
мольная доля извлекаемого компонента
А в газовой смеси и р – общее давление
в системе, то парциальное давление ,
по закону Дальтона, можно записать:
,
по закону Дальтона, можно записать:
Тогда,
подставив значение
 в (5.72) получим
в (5.72) получим
Итак
для закона Генри имеем
Здесь
 - коэффициент распределения, или
константа фазового равновесия.
Величинаm
уменьшается с увеличением р и снижения
Т. Таким образом, растворимость газа в
жидкости растёт с ростом давления и
снижения Т.
- коэффициент распределения, или
константа фазового равновесия.
Величинаm
уменьшается с увеличением р и снижения
Т. Таким образом, растворимость газа в
жидкости растёт с ростом давления и
снижения Т.
Когда в равновесии с жидкостью находятся смесь газов, закону Генри может следовать каждый из компонентов смеси в отдельности.
Закон Генри справедлив только для идеальных газов, а также к сильно разбавленным растворам. Для хорошо растворимых газов, при больших концентрациях их в растворе, растворимость меньше, чем по закону Генри. Для систем, не подчиняющихся закону Генри, m является величиной переменной и линия равновесия представляет собой кривую, которую строят обычно по опытным данным.
При
больших давлениях (МПа и выше) изменение
объёма жидкости вследствие растворения
в ней газа соизмеримо с изменением
объёма газа, тогда

 -
фугитивность (летучесть) поглощаемого
газа, выраженная в единицах давления
(расчет этой величины приводится в
специальной литературе).
-
фугитивность (летучесть) поглощаемого
газа, выраженная в единицах давления
(расчет этой величины приводится в
специальной литературе).
Обычно для расчетов используют не абсолютные, а относительные концентрации, когда концентрации выражаются в килограммах компонента по отношению к килограммам носителя.
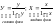
Закон
Генри запишется
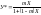
Следовательно,
линия равновесия в системе газ –
жидкость в координатах X
и Y
изображается кривой линией. При малых
концентрациях х в жидкости, т.е. в случае
сильно разбавленных растворов, величиной
 можно пренебречь. Тогда уравнение
упрощается и принимает вид:
можно пренебречь. Тогда уравнение
упрощается и принимает вид:

В случае абсорбции многокомпонентных смесей парциальное давление каждого компонента в газовой смеси зависит не только от его концентрации в растворе, но и от концентрации в растворе других компонентов, т.е. является функцией большого числа переменных. Поэтому в подобных случаях, равновесные зависимости основываются на опытных данных.
