
Кишкун А.А
.pdf
532 ■ Глава 9
Функциональное состояние
гипоталамо-гипофизарной системы
Существует тесная взаимосвязь между нервной и эндокринной системами. Единство нервной и гуморальной регуляции в организме обеспечивается тесной анатомической и функциональной связью гипофиза
игипоталамуса. Гипоталамус — высший вегетативный центр, координирующий функции различных систем для удовлетворения потребностей всего организма. Он играет ведущую роль в поддержании оптимального уровня обмена веществ (белкового, углеводного, жирового, водного и минерального) и энергии, в регуляции теплового баланса организма, функций пищеварительной, сердечно-сосудистой, выделительной, дыхательной и эндокринной систем. Под контролем гипоталамуса находятся такие железы внутренней секреции, как гипофиз, щитовидная железа, половые железы, надпочечники, поджелудочная железа. Гипоталамус имеет обширные анатомические и функциональные связи с другими структурами головного мозга.
Регуляция секреции тропных гормонов гипофиза осуществляется выделением гипоталамических нейрогормонов. Гипоталамус образует специфические медиаторы — рилизинг-гормоны, которые по сосудам портальной системы гипоталамуса-гипофиза поступают в гипофиз и, воздействуя непосредственно на его клетки, стимулируют или тормозят секрецию гормо-
нов. Сеть кровеносных капилляров, относящихся к портальной системе гипоталамус−гипофиз, образует вены, которые проходят по ножке гипофиза, а затем разделяются на вторичную капиллярную сеть в передней доле гипофиза. Гормоны гипоталамуса и гипофиза относятся к белковым
ипептидным гормонам.
Гормоны гипоталамуса
Стимуляцию секреции тропинов аденогипофиза осуществляют следующие гормоны гипоталамуса (рис. 9-1):
■кортикотропин-рилизинг гормон (КРГ);
■тиреотропин-рилизинг гормон (ТРГ);
■гонадотропин-рилизинг гормон (ГРГ);
■пролактин-рилизинг гормон (ПРГ);
■соматотропин-рилизинг гормон (СТРГ);
■меланотропин-рилизинг гормон.
Блокаторы секреции гипофизарных гормонов включают:
■соматостатин;
■гонадотропин-рилизингингибирующий гормон (ГРИГ);
■пролактин-рилизингингибирующий гормон (ПРИГ);
■меланостатин.
Биосинтез указанных выше нейрогормонов осуществляется не только в гипоталамусе, например, соматостатин образуют D-клетки островков поджелудочной железы и слизистой оболочки кишечника, а также церебральные нейросекреторные клетки. ТРГ образуется, кроме гипоталамуса, и в других отделах ЦНС. Помимо названных гормонов, в гипоталамусе ещё синтезируется АДГ, окситоцин и нейрофизин, которые мигрируют вдоль


534 ■ Глава 9
Рис. 9-1. Гормоны гипоталамуса, гипофиза и эндокринных желёз

Гормональные исследования ■ 535

536 ■ Глава 9
■Местные нарушения синтеза гормонов, изменение их свойств и реакции клеток на действие гормонов в гипоталамусе и гипофизе.
■Патологические изменения рецепторов гормонов клеток гипофиза.
■Расстройства функций периферических желёз внутренней секреции
и их рецепторов.
■ Патологическая резистентность (ареактивность) клеток-мишеней к действию гормонов.
Основной причины гипоталамо-гипофизарных заболеваний — нарушение взаимосвязи ЦНС, гипоталамуса, гипофиза и периферических желёз внутренней секреции. Для выбора эффективных методов лечения необходимо установить, на каком уровне произошло расстройство взаимосвязи в системе гормональной регуляции.
Соматотропная функция гипофиза
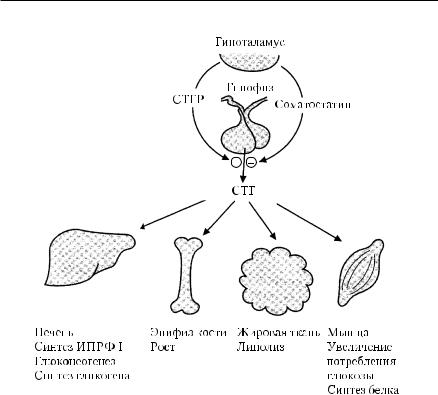
СТГ — пептид, выделяемый передней долей гипофиза и состоящий из 191 аминокислоты. Суточная продукция СТГ составляет приблизительно 500 мкг. СТГ стимулирует синтез белка, процессы митоза клеток и усиливает липолиз. Период полувыведения СТГ у взрослых составляет 25 мин. Инактивация гормона в крови осуществляется путём гидролиза. По сравнению с другими гормонами СТГ присутствует в гипофизе в наибольшем количестве (5−15 мг/г ткани). Главная функция СТГ — стимуляция роста организма. СТГ способствует синтезу белка и, взаимодействуя с инсулином, стимулирует поступление аминокислот в клетки. Он также влияет на поглощение и окисление глюкозы жировой тканью, мышцами и печенью. СТГ увеличивает чувствительность адипоцитов к липолитическому действию катехоламинов и снижает чувствительность их к липогенному действию инсулина. Эти эффекты ведут к выходу жирных кислот и глицерина из жировой ткани в кровь, с последующим их метаболизмом в печени. СТГ снижает эстерификацию жирных кислот, тем самым уменьшает синтез ТГ. Современные данные позволяют предполагать, что СТГ может уменьшать потребление глюкозы жировой тканью и мышцами путём пострецепторного ингибирования действия инсулина (рис. 9-2). СТГ увеличивает транспорт аминокислот в мышцу, создавая запасы субстрата для синтеза белка. Через отдельный механизм СТГ увеличивает синтез ДНК и РНК.
СТГ стимулирует рост клеток как непосредственно, так и опосредованно, через ИПФР I и II. Основные биологические эффекты СТГ обеспечивает ИПФР I.
Секреция СТГ в норме происходит неравномерно. В течение большей части суток его концентрация в крови здоровых людей очень низка. За сутки происходит 5−9 дискретных выбросов гормона. Низкий исходный уровень секреции и пульсирующий характер выбросов значительно затрудняют оценку результатов определения концентрации СТГ в крови. В таких случаях используют специальные провокационные тесты.
Регуляция секреции СТГ главным образом осуществляется двумя пептидами гипоталамуса: СТРГ, который стимулирует образование СТГ, и соматостатином, обладающим противоположным действием. В регуляции секреции СТГ участвует и ИПФР I. Увеличение концентрации в крови ИПФР I подавляет транскрипцию генов СТГ в соматотрофах гипофиза по принципу обратной отрицательной связи.
Гормональные исследования ■ 537
Рис. 9-2. Основные метаболические эффекты СТГ
Основные нарушения соматотропной функции гипофиза представлены избыточной или недостаточной продукцией СТГ. Гигантизм и акромегалия — нейроэндокринные заболевания, обусловленные хронической гиперпродукцией СТГ соматотрофами передней доли гипофиза. Избыточная продукция СТГ в период остеогенеза до закрытия эпифизов приводит к гигантизму. После закрытия эпифизов гиперсекреция СТГ служит причиной акромегалии. Гипофизарный гигантизм наблюдают редко, он возникает в молодом возрасте. Акромегалия возникает в основном в возрасте 30−50 лет (средняя частота — 40−70 случаев на 1 млн населения).
Развитие гипофизарного нанизма (карликовости) в подавляющем большинстве случаев связано с недостаточностью соматотропной функции передней доли гипофиза, вплоть до полного её выпадения. Нарушение продукции СТГ гипофизом чаще всего (приблизительно в 70% случаев) обусловлено первичным поражением гипоталамуса. Врождённые аплазию и гипоплазию гипофиза выявляют очень редко. Любые деструктивные изменения в гипоталамо-гипофизарной области могут привести к остановке роста. Чаще всего они обусловлены краниофарингиомами, герминомами

538 ■ Глава 9
ЦНС и другими опухолями гипоталамической области, туберкулёзом, саркоидозом, токсоплазмозом и аневризмами сосудов головного мозга.
Известны формы нанизма, преимущественно наследственно обусловленые, при которых образование и секреция СТГ не нарушены. В частности, у детей с синдромом Ларона присутствуют все признаки гипопитуитаризма, однако концентрация СТГ в крови повышена на фоне сниженного содержания ИПФР I. Основной дефект обусловлен неспособностью СТГ стимулировать выработку ИПФР I.
У многих больных гипопитуитаризмом не удаётся обнаружить очевидного структурного повреждения гипоталамуса или гипофиза; в таких случаях патология чаще обусловлена функциональными дефектами гипоталамуса. Недостаточность СТГ может быть как изолированной, так и сочетаться с недостаточностью других гормонов гипофиза.
СОМАТОТРОПНЫЙ ГОРМОН В СЫВОРОТКЕ КРОВИ
Суточный ритм секреции СТГ с пиками его концентрации выше 6 нг/мл через 1−3 ч после засыпания независимо от времени суток формируется к 3 мес после рождения. Среднесуточная концентрация СТГ повышается в период полового созревания, снижается после 60 лет; к этому же времени исчезают суточные ритмы. Половых различий в секреции СТГ не выявлено. Референтные величины концентрации СТГ в сыворотке крови представлены в табл. 9-1.
Таблица 9-1. Референтные величины концентрации СТГ в сыворотке крови
Возраст |
СТГ, нг/мл |
|
|
Кровь из пуповины |
8−40 |
Новорождённые |
10−40 |
Дети |
1−10 |
Взрослые: |
|
Мужчины |
0−4,0 |
Женщины |
0−18,0 |
Старше 60 лет: |
|
Мужчины |
1−9,0 |
Женщины |
1−16 |
Повышение концентрации СТГ в сыворотке крови наблюдают при акромегалии (у 80% больных — более 10 нг/мл) и гигантизме, которые чаще связаны с СТГ-продуцирующей аденомой гипофиза. Основной метод лабораторной диагностики гигантизма и акромегалии — определение концентрации СТГ в сыворотке крови натощак (подсчитывают среднее значение 3-кратного определения в течение 2−3 дней с перерывами 1−2 дня). Обычно концентрация СТГ в крови у больных в 2−100 раз выше нормы (иногда достигает 400 нг/мл). При близких к нормальным показателях содержания СТГ в крови натощак (у 30−53% больных) для подтверждения диагноза и установления фазы заболевания (активная или неактивная) необходимо исследовать суточный ритм секреции СТГ (в активную фазу превышает нормальные значения в 2−100 раз и более), а также провести ряд

Гормональные исследования ■ 539
физиологических и фармакологических тестов. Для уточнения диагноза содержание СТГ в сыворотке исследуют с интервалом 1−2 мес. При акромегалии определение СТГ в сыворотке крови в динамике заболевания необходимо для оценки эффективности консервативной терапии и радикальности хирургического лечения. Медикаментозная терапия акромегалии считается адекватной в случае, если концентрация СТГ не превышает 10 нг/мл. Эффективная гаммаили протонотерапия приводит к нормализации концентрации СТГ в крови. Результат гамматерапии оценивают не ранее чем через 2 мес, а протонотерапии — через 4 мес по окончании лечения. Радикально проведённая операция также способствует нормализации содержания СТГ в течение нескольких дней. Полноту удаления соматотропиномы оценивают с помощью глюкозотолерантного теста с исследованием содержания СТГ в сыворотке крови натощак, а также через 1 и 2 ч после приёма глюкозы. Снижение концентрации СТГ в ходе теста до 2,5 нг/мл и ниже свидетельствует о радикальности проведённой аденомэктомии.
Пониженное выделение СТГ в период роста приводит к карликовости. При гипофизарном нанизме секреция СТГ снижена, суточный ритм секреции не прослеживается. Если в пробе, взятой натощак, содержание СТГ превышает 10 нг/мл, его недостаточность может быть исключена. При более низких показателях необходимы дополнительные исследования. Проводят различные диагностические пробы, поскольку нижняя граница нормальной концентрации СТГ в крови близка к пределу чувствительности существующих лабораторных методов её определения.
Совсем недавно была выделена в самостоятельную нозологическую форму недостаточность СТГ у взрослых. Клинически недостаточность СТГ у взрослых проявляется увеличением массы тела вследствие прироста жировой ткани, снижением количества жидкости в организме (в основном за счёт экстрацеллюлярной) и минеральной плотности костей. В крови выявляют повышение концентрации ЛПОНП, ЛПНП, ТГ и снижение ЛПВП (нормализация их уровня — важный критерий оценки эффективности заместительной терапии у таких больных). Концентрацию ИПФР I
всыворотке крови в качестве критерия недостаточности СТГ у взрослых не используют из-за значительной вариабельности референтных величин.
Концентрация СТГ в крови может снижаться у детей с первичным гипотиреозом. Успешное лечение гипотиреоза приводит к её нормализации. Заболевания и состояния, при которых может изменяться содержание СТГ
вкрови, представлены в табл. 9-2.
ИНСУЛИНОПОДОБНЫЙ ФАКТОР РОСТА I В СЫВОРОТКЕ КРОВИ
Основной фактор, определяющий концентрацию ИПФР I в сыворотке крови, — возраст. Концентрация ИПФР I в крови возрастает с очень низких показателей (20−60 нг/мл) при рождении и достигает пиковых значений (600−1100 нг/мл) в период половой зрелости. Уже во второй декаде жизни человека уровень ИПФР I начинает быстро снижаться, достигая средних значений (350 нг/мл) в возрасте 20 лет, а затем снижается более медленно с каждой декадой. В 60 лет концентрация ИПФР I в крови составляет не более 50% таковой в возрасте 20 лет. Суточные колебания концентрации ИПФР I в крови не выявлены. Референтные величины содержания ИПФР I в сыворотке крови представлены в табл. 9-3 [Тиц Н., 1997].

540 ■ Глава 9
Таблица 9-2. Состояния, влияющие на концентрацию СТГ в крови
Увеличение концентрации |
Снижение концентрации |
|
|
Акромегалия и гигантизм |
Гипофизарная карликовость |
Голодание, стресс, алкоголизм |
Гиперкортицизм |
ХПН |
Тучность |
Посттравматические и постопераци- |
Химиотерапия, радиотерапия |
онные состояния |
|
Порфирия, гипергликемия |
Оперативные вмешательства |
Эктопическая продукция опухолями |
Синдром Иценко−Кушинга |
желудка, лёгких |
|
Гиперпитуитаризм |
Факторы, вызывающие гипергликемию |
Физическая нагрузка |
Гипопитуитаризм |
АКТГ, вазопрессин, эстрогены, |
Анэнцефалия у плода |
норадреналин, дофамин, серотонин, |
Прогестерон, ГК, фенотиазины, сома- |
клонидин, пропранолол, бромокрип- |
тостатин, глюкоза |
тин, аргинин, инсулин, витамин РР, |
|
амфетамин |
|
Таблица 9-3. Референтные величины концентрации ИПФР I в сыворотке крови |
|
Возраст, годы |
Пол |
ИПФР I, нг/мл |
|
|
|
|
|
1−3 |
Мужской |
31−160 |
|
|
Женский |
11−206 |
|
3−7 |
Мужской |
16−288 |
|
|
Женский |
70−316 |
|
7−11 |
Мужской |
136−385 |
|
|
Женский |
123−396 |
|
11−12 |
Мужской |
136−440 |
|
|
Женский |
191−462 |
|
13−14 |
Мужской |
165−616 |
|
|
Женский |
286−660 |
|
15−18 |
Мужской |
134−836 |
|
|
Женский |
152−660 |
|
18−25 |
Мужской |
202−433 |
|
|
Женский |
231−550 |
|
26−85 |
Мужской |
135−449 |
|
Женский |
135−449 |
||
|
Концентрация ИПФР I в крови зависит от СТГ, а также от T4. Низкий уровень ИПФР I выявляют у пациентов с тяжёлой недостаточностью T4. Проведение заместительной терапии препаратами левотироксина натрия приводит к нормализации концентрации ИПФР I в сыворотке крови.
Ещё один фактор, определяющий концентрацию ИПФР I в крови, — состояние питания. Адекватное белково-энергетическое обеспечение организма — важнейшее условие поддержания нормальной концентрации ИПФР I в крови как у детей, так и у взрослых. У детей с выраженной

Гормональные исследования ■ 541
энергетической и белковой недостаточностью концентрация ИПФР I в крови снижена, но легко поддаётся коррекции при нормализации питания. Другие катаболические нарушения, такие как печёночная недостаточность, воспалительные заболевания кишечника или почечная недостаточность, также ассоциируются с низким содержанием ИПФР I в крови.
В клинической практике исследование ИПФР I имеет важное значение для оценки соматотропной функции гипофиза.
При акромегалии концентрация ИПФР I в крови постоянно увеличена и поэтому считается более достоверным критерием акромегалии, чем содержание СТГ. Средняя концентрация ИПФР I в сыворотке крови у пациентов с акромегалией приблизительно в 7 раз превышает нормальную возрастную величину. Чувствительность и специфичность исследования ИПФР I для диагностики акромегалии у пациентов старше 20 лет превышает 97%. Степень повышения концентрации ИПФР I в сыворотке крови коррелирует с активностью заболевания и ростом мягких тканей. Определение содержания ИПФР I в сыворотке крови используют для мониторинга эффективности лечения, так как оно хорошо коррелирует с остаточной секрецией СТГ.
Критериями излечения акромегалии считают следующие лабораторные показатели:
■концентрация СТГ в крови натощак ниже 5 нг/мл;
■концентрация СТГ в крови ниже 2 нг/мл при проведении ПТТГ;
■концентрация ИПФР I в крови в пределах нормальных величин.
Функциональное состояние гипоталамо- гипофизарно-надпочечниковой системы
Гипоталамус, передняя доля гипофиза и кора надпочечников функционально объединены в гипоталамо-гипофизарно-надпочечниковую систему.
Надпочечник состоит из коры и мозговой части, выполняющих различные функции. Гистологически в коре надпочечников взрослого человека различают три слоя. Периферическую зону называют клубочковой, за ней идёт пучковая (наиболее широкая средняя зона коры надпочечника) и сетчатая. Клубочковая зона секретирует только альдостерон. Два других слоя — пучковая и сетчатая зоны — образуют функциональный комплекс, секретирующий основную массу гормонов коры надпочечников (ГК и андрогены).
Впучковойзонекорынадпочечниковпрегненолон,синтезированныйизХС, преобразуется в 17α-оксипрегненолон, служащий предшественником кортизола, андрогенов и эстрогенов. В процессе синтеза из 17α-оксипрегнено- лона образуется 17α-оксипрогестерон, который последовательно гидроксилируется в кортизол.
К продуктам секреции пучковой и сетчатой зон относятся стероиды, обладающие андрогенной активностью: дегидроэпиандростерон (ДГЭА), дегидроэпиандростерона сульфат (ДГЭАС), андростендион (и его 11β-ана- лог) и тестостерон. Все они образуются из 17α-оксипрегненолона.
Продукция надпочечниковых ГК и андрогенов регулируется гипоталамогипофизарной системой. В гипоталамусе вырабатывается КРГ, попадающий через портальные сосуды в переднюю долю гипофиза, где он стиму-
