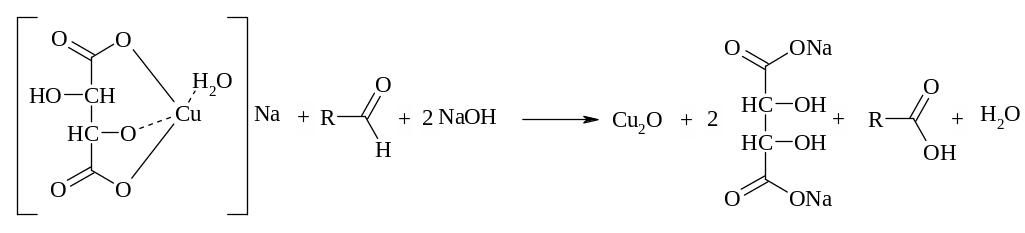- •Тема 2. Качественные и количественные реакции функциональных групп Оглавление
- •Окисление хромовой смесью (качественная реакция позволяет различить первичные и вторичные спирты)
- •Реакция с ванилином (обнаружение первичных спиртов)
- •Реакция с n-бромметилфталимидом
- •Реакция с 8-оксихинолинатом ванадия
- •Обнаружение метанола
- •Обнаружение этанола
- •Обнаружение пропанола и бутанола
- •Определение фурфурилового спирта
- •Обнаружение многоатомных спиртов
- •Обнаружение пентаэритрита
- •Количественное определение гидроксильных групп.
- •Определение гидроксильных групп по методу Чугаева –Церевитинова
- •Открытие формальдегида Реакция с аммиаком
- •Реакция с пирогаллолом
- •Реакция конденсации формальдегида с резорцином.
- •Реакция с β-нафтолом
- •Реакция с хромотроповой кислотой (1,8-диоксинафталин-3,6-дисульфокислотой)
- •Реакция с трихлоридом сурьмы.
- •Реакция с раствором 5-метилрезорцина.
- •Количественное определение альдегидов.
- •Многоосновные кислоты.
- •Обнаружение терефталевой кислоты
- •Проба на себациновую кислоту.
- •Определение кислотного числа.
- •Определение числа омыления и эфирного числа
- •2.5 Определение аминов Обнаружение анилина
- •Открытие мочевины
- •Количественное определение карбамида и меламина
- •Количественное определение азота.
Обнаружение пентаэритрита
При нагревании нелетучих многоатомных спиртов с карбамидом (мочевиной) выделяется аммиак, который можно обнаружить в газовой фазе с помощью реактива Несслера или кислотно-основной индикаторнойбумаги.

Приготовление реактива Несслера6 к 50 г иодида калия в 35мл воды добавляют насыщенный рвствор HgCl2 до тех пор пока не появится осадок, затем дрбавляют 400мл 9н раствора гадроксида натрия или калия. Полученный раствор доводят до 1л водой, дают отстоятся и декантируют.
Выполнение анализа:
Небольшой объем исследуемого раствора выпаривают в пробирке досуха , прибавляют несколько мл раствора мочевины и тщательно перемешивают. Затем пробирку помещают в баню с температурой 130 °С, отверстие пробирки накрывают фильтровальной бумагой смоченной реактивом Несслера, о положительной реакции свидетельствует появление бурого пятна.
Количественное определение гидроксильных групп.
Число гидроксильных групп проще всего определять методом получения соответствующих эфиров. Эфиры получают путем ацетилирования уксуснфм ангидридом в пиридине, затем эфир омыляют раствором щелочи и оттитровывают ее избыток. Расчет числа ОН-групп в испытуемом веществе проводится на основании следующих реакций:
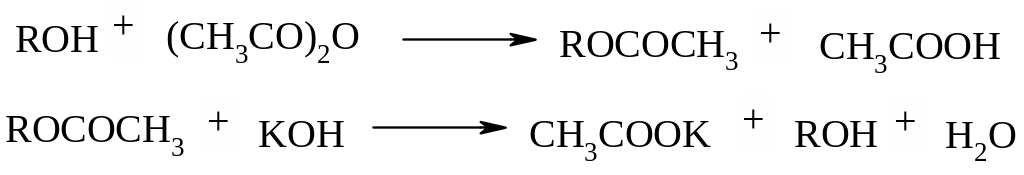
Ацетилированные продукты на каждый гидроксил освобождают 1 молекулу уксусной кислоты.
Выполнение анализа:
В колбу помещают 1г испытуемого продукта, приливают 3 мл уксусного ангидрида и нагревают с обратным холодильником 2-3 часа, затем продукт реакции переносят в стакан и под тягой кипятят с 500мл воды в течении 30 мин (для удаления избытка ангидрида). Продукт экстрагируется эфиром и промывается до отрицательной реакции промывных вод на кислоту. Эфирный раствор сушат над Na2SO4. Эфир отгоняют, остаток высушивают до постоянного веса.
Навеску ацетилированного продукта 0,2г помещают в круглодонную колбу (1л) и растворяют в 5 мл спирта, затем из бюретки отмеряют точно 20 мл 0,2н спиртового раствора КОН и нагревают на кипящей бане с обратным холодильником 2-3 часа. Параллельно проводят контрольный опыт с 5 мл спирта и 20мл 0,2н спиртового раствора КОН.
После охлаждения содержимое обеих колб титруют 0,1н раствором соляной кислоты и определяют количество свободной щелочи по формуле:
где, a –мл соляной кислоты, пошедшие на титрование в холостом опыте, b –мл соляной кислоты в табочем опыте, THCl –титр соляной кислоты по КОН, m –масса навески.
Определение гидроксильных групп по методу Чугаева –Церевитинова
Метод основан на реакции метилмагнийбромида со спиртами (или соединениями, содержащими активный водород с образованием метана по реакции:)
![]()
Измеряя объем выделившегося метана, можно определить количество атомов активного водорода.
Применение алюмогидрида лития основано на реакции:
![]()
В обоих случаях 1 атом активного водорода равен 1 молекуле газа.
Преимущества и недостатки методов.
Реакция с метилмагнийиодидом идет медленно и часто для ее завершения необходимо поднимать температуру, тогда как алюмогидрид лития реагирует пратически мгновенно и при низких температурах, даже с пространственно затрудненными соединениями.
Методы похожи по технике работы, аппаратурному оформлению, точности результатов. При работе с алюмогидридом лития следует помнить:
-он является сильным восстановителем, некоторые вещества не имеющие активного водорода, приобретают его, например:
-алюмогидрид лития очень чувствителен к влаге и реагирует с кислородом воздуха с выделением газа
Реакция с метилмагнийиодидом
Получение метилмагнийиодида
Берут 100г перегнанного над натрием диизоамилового эфира, 4,8г магния, 35,5г сухого иодистого метила и кристаллического иода. Если через некоторое время реакция не началась, смесь слабо нагревают. По окончании реакции смесь нагревают еще 2 часа с обратным холодильником на сильнокипящей водяной бане, затем с низходящим холодильником отгоняют избыток иодистого метила.
Полученный раствор метилмагнийиодида можно сохранять в хорошо закупоренной залитой парафином склянке 3-4 недели без изменений.
Определение гидроксильных групп проводят в приборе:
Где в сосуде А происходит реакция, его закрепляют на штативе в вертикальном положении, через воронку 1 вводят 0,1-0,2г вещества из пробирки, и около 15 мл растворителя. Затем сосуд А устанавливают наклонно и в сосуд С с помощью воронки 2 вносят 5 мл метилмагнийиодида в растворе, затем закрывают сосуд А пробкой и соединяют с измерительным прибором. Измерительный прибор редставляет собой градуированную трубку В, соединенную с воронкой М, наполненной ртутью, и воронкой К с двухходовым краном. Трубка В установлена в гильзе Г наполненной водой. Для поддержания температуры применяют термостатирование, через 10 мин устанавливается постоянная температура. В течение этого времени давление в А падает. Для того чтобы вновь получить атмосферное давление, на момент открывают двухходовой кран К. затем при помощи К трубку В соединяют с внешним воздухом, после этого поднимают воронку М, до тех пор пока ртуть не вытеснит весь воздух из В, поворачивают кран на 90°, опускают воронку М и закрепляют на лапке штатива.
После этого смешивают метилмагнийиодид с раствором, и поворачивают кран, чтобы соединить А и В. При сильном взбалтывании происходит сильное выделение газа из А и ртуть в В начинает опускаться. Как только ртуть начнет медленно падать и объем газа перестанет увеличиваться А помещают в термостат для принятия первоначальной температуры (5-7мин). При этом происходит сокращение объема газа, который замеряют при постоянной температуре и используют для расчета количества ОН-групп по формуле:

где, 0,000719 –вес 1мл метана при 0 °С и 760 мм.рт.ст.;
16 –молекулярный вес метана;
17 –относительный вес ОН-группы;
V –объем метана образовавшийся и приведенный к 0 °С и 760 мм.рт.ст. и выраженный в мл;
S –вес вещества в г.
Данный метод позволяет открывать ОН-группы в стероидных соединениях, в которых другими методами это сделать невозможно.
2.2. Обнаружение альдегидов
Традиционно альдегиды определяют с реактивом Толленса по реакции серебрянного зеркала, и реактивом Фелинга.
Реакцию на альдегиды дают многие полимеры: продукты конденсации с альдегидами полиспиртов, аминов, амидов, продукты конденсации альдегидов с поливинилацеталем.
Разложение полимера:
Исследуемый полимер (5г) помещают в пробирку из тугоплавкого стекла и закрывают отверстие пробкой с газоотводной трубкой, конец которой опускают во вторую пробирку наполненную на ½ водой. Пробирку с полимером нагревают в пламени горелки до обугливания полимера, протдукты разложения отгоняются в пробирку с водой.
Реакция серебрянного зеркала.
Приготовление реактива Толленса: 0,5мл 10%-ного раствора нитрата серебра смешивают с 0,2мл 40%-ного раствора едкого натра, выпавший осадок гидроксида серебра растворяют избытком аммиака.
Анализ продуктов разложения:
К раствору полученному при разложении полимера приливают раствор Толленса, и слегка нагревают, в случае положительной реакции на стенках выпадает серебро по реакции:
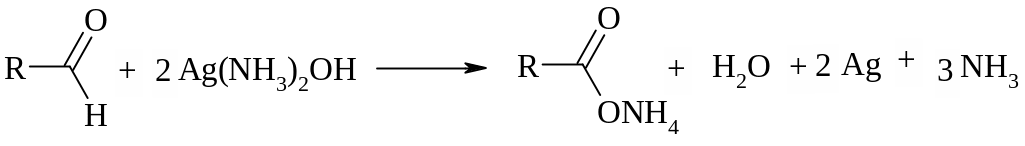
Реакция с реактивом Фелинга:
Приготовление реактива:
6,93 г чистого сульфата меди растворяют в воде в мерной колбе на 100мл и доводят водой до метки. Отдельно растворяют 14г едкого натра, 35г сегнетовой соли (натриево-калиевая соль винной кислоты или натрий-калий тартрат обычно кристаллогидрат *4 Н2О) в 50 мл воды и также доводят раствор до 100мл. оба раствора смешивают.
Проведение анализа:
К водному раствору продуктов разложения полимера добавляют Фелингову жидкость, выпадение красного осадка закиси меди свидетельствует о положительной реакции: