
- •Введение и краткая история биохимии. Роль и место биохимии в системе естественных наук. Значение биохимии для промышленности, сельского хозяйства и медицины.
- •Структура клетки и биохимическая характеристика отдельных субклеточных компонентов.
- •Аминокислотный состав белков. Классификация аминокислот. Протеиногенные и непротеиногенные аминокислоты.
- •Физико-химические свойства аминокислот. Кислотно-основные свойства аминокислот. Амфотерность. Изоэлектрическая точка. Буферные свойства.
- •Реакции на аминогруппу и карбоксильную группу. Реакции на отдельные аминокислоты.
- •8.Структурная организация белков. Первичная, вторичная, третичная и четвертичная структура белков.
- •Четвертичная структура
- •9. Структура пептидной связи. Элементы вторичной структуры: альфа-спирал и бета-структура. Домены в структуры белка, их функциональная роль.
- •10. Методы изучения структуры белка. Физико-химические свойства белков. Методы оценки размеров и формы белковых молекул. Денатурация и ренатурация белка.
- •13. Физико-химические свойства белков: молекулярная масса, кислотно-основные свойства белков. Заряд белковой молекулы, изоэлектрическая точка. Буферные свойства белков.
- •14. Растворимость, коллоидные свойства, денатурация и оптические свойства белков.
- •17. Скорость химических реакций и сущность явления катализа.Теоретические основы и особенности ферментативного катализа. Термодинамические и кинетические характеристики ферментативного катализа.
- •18. Классификация и номенклатура ферментов. Химическая природа ферментов, их функциональные группы. Активный и аллостерический центры.
- •33. Переаминирование аминокислот, его механизм, биологическое значение. Процессы дезаминирования и декарбоксилирования аминокислот.
- •34. Образование аммиака. Транспорт аммиака. Восстановительное аминирование. Амиды и их физиологическое значение.
- •35. Особенности обмена отдельных аминокислот и их роль в образовании важнейших биологически активных веществ.
- •37. Азотистые небелковые вещества (биогенные амины), их синтез, распад и биологическая роль. Нарушения структуры и обмена белков. Наследственные заболевания.
- •38. Алкалоиды, их роль у растений и значение в медицине.
- •39. Углеводы и их биологическая роль, классификация и номенклатура.
- •41. Анаэробный и аэробный распад углеводов. Энергетическая характеристика аэробной и анаэробной фазы углеводного обмена.
- •42. Гликолиз. Спиртовое брожение.
- •49. Цепь переноса водорода и электронов (дыхательная цепь).
- •50. Над и надф-зависимые дегидрогеназы.
- •51. Флавиновые ферменты, убихинон, цитохромы и цитохромоксидаза.
- •52. Окислительное фосфорилирование в дыхательной цепи. Представление о механизмах сопряжения окисления и фосфорилирования в дыхательной цепи.
- •53. Митохондрии, структура и энергетические функции. Трансмембранный потенциал ионов водорода как форма запасания энергии.
- •55. Жирные кислоты, их классификация и номенклатура. Простагландины.
Четвертичная структура
Встречается не у всех белков, а только у тех, которые состоят из двух или более полипептидных цепей. Каждая такая цепь называется СУБЪЕДИНИЦЕЙ данной молекулы (или ПРОТОМЕРОМ). Поэтому белки, обладающие четвертичной структурой, называют ОЛИГОМЕРНЫМИ белками. В состав белковой молекулы могут входить одинаковые или разные субъединицы. Например, молекула гемоглобина «А» состоит из двух субъединиц одного типа и двух субъединиц другого типа, то есть является тетрамером. Фиксируются четвертичные структуры белков всеми типами слабых связей, а иногда еще и дисульфидными связями.
9. Структура пептидной связи. Элементы вторичной структуры: альфа-спирал и бета-структура. Домены в структуры белка, их функциональная роль.
ЕЛКИ, высокомол. природные полимеры, построенные из остатков аминокислот, соединенных амидной (пептидной) связью —СО—NH—. Каждый БЕЛКИ характеризуется специфический аминокислотной последовательностью и индивидуальной пространств, структурой (конформацией). На долю БЕЛКИ приходится не менее 50% сухой массы органическое соединение животной клетки. Функционирование БЕЛКИ лежит в основе важнейших процессов жизнедеятельности организма. Обмен веществ (пищеварение, дыхание и др.), мышечное сокращение, нервная проводимость и жизнь клетки в целом неразрывно связаны с активностью ферментов - высокоспецифический катализаторов биохимический реакций, являющихся белками. Основу костной и соединительной тканей, шерсти, роговых образований составляют структурные БЕЛКИ (см., например, Коллаген). Они же формируют остов клеточных органелл (митохондрий, мембран и др.).
Аминокислоты способны соединяться между собой связями, которые называются пептидными, при этом образуется полимерная молекула. Если количество аминокислот не превышает 10, то новое соединение называется пептид; если от 10 до 40 аминокислот – полипептид, если более 40 аминокислот – белок.
Пептидная
связь –это связь между α-карбоксильной
группой одной аминокислоты и α-аминогруппой
другой аминокислоты.
![]() При необходимости назвать пептид ко
всем названиям аминокислот добавляют
суффикс "-ил", только последняя
аминокислота сохраняет свое название
неизменным.Например, аланил-серил-триптофан
или γ-глутаминил-цистеинил-глицин
(по-другому называемый глутатион).
При необходимости назвать пептид ко
всем названиям аминокислот добавляют
суффикс "-ил", только последняя
аминокислота сохраняет свое название
неизменным.Например, аланил-серил-триптофан
или γ-глутаминил-цистеинил-глицин
(по-другому называемый глутатион).
К
свойствам пептидной связи относятся:1.
Копланарность
![]() Все атомы, входящие в пептидную группу
находятся в одной плоскости, при этом
атомы "Н" и "О" расположены по
разные стороны от пептидной связи.
2.Транс-положение заместителей
Все атомы, входящие в пептидную группу
находятся в одной плоскости, при этом
атомы "Н" и "О" расположены по
разные стороны от пептидной связи.
2.Транс-положение заместителей![]() Радикалы аминокислот по отношению к
оси C-N связи находятся по "разные"
стороны, в транс-положении.3. Две
равнозначные формы
Радикалы аминокислот по отношению к
оси C-N связи находятся по "разные"
стороны, в транс-положении.3. Две
равнозначные формы
![]() Пептидная связь имеет кетоформу и
енольную форму.4. Способность к образованию
водородных связей.
Пептидная связь имеет кетоформу и
енольную форму.4. Способность к образованию
водородных связей.
 Атомы углерода и азота, входящие в
пептидную связь обладают способностью
образовывать две водородные связи с
другими пептидными группами. 5. Пептидная
связь имеет частично характер двойной
связи.
Атомы углерода и азота, входящие в
пептидную связь обладают способностью
образовывать две водородные связи с
другими пептидными группами. 5. Пептидная
связь имеет частично характер двойной
связи.
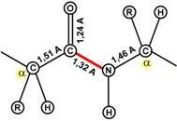 Длина пептидной связи меньше, чем
одинарной связи, она является жесткой
структурой, и вращение вокруг нее
затруднено. Но так как, кроме пептидной,
в белке есть и другие связи, цепочка
аминокислот способна вращаться вокруг
основной оси, что придает белкам различную
конформацию (пространственное расположение
атомов).
Длина пептидной связи меньше, чем
одинарной связи, она является жесткой
структурой, и вращение вокруг нее
затруднено. Но так как, кроме пептидной,
в белке есть и другие связи, цепочка
аминокислот способна вращаться вокруг
основной оси, что придает белкам различную
конформацию (пространственное расположение
атомов).
Вторичная структура - это пространственная организация стержня полипептидной цепи. Существуют 3 главнейших типа вторичной структуры:
1) Альфа-спираль - имеет определенные характеристики: ширину, расстояние между двумя витками спирали. Для белков характерна правозакрученная спираль. В этой спирали на 10 витков приходится 36 аминокислотных остатков. У всех пептидов, уложенных в такую спираль, эта спираль абсолютно одинакова. Фиксируется альфа-спираль с помощью водородных связей между NH-группами одного витка спирали и С=О группами соседнего витка. Эти водородные связи расположены параллельно оси спирали и многократно повторяются, поэтому прочно удерживают спиралеобразную структуру. Более того, удерживают в несколько напряженном состоянии (как сжатую пружину).
Бета-складчатая структура - или структура складчатого листа. Фиксируется также водородными связями между С=О и NH-группами. Фиксирует два участка полипептидной цепи. Эти цепи могут быть параллельны или антипараллельны. Если такие связи образуются в пределах одного пептида, то они всегда антипараллельны, а если между разными полипептидами, то параллельны.
3) Нерегулярная структура - тип вторичной структуры, в котором расположение различных участков полипептидной цепи относительно друг друга не имеет регулярного (постоянного) характера, поэтому нерегулярные структуры могут иметь различную конформацию.
Доме́н белка́ — элемент третичной структуры белка, представляющий собой достаточно стабильную и независимую подструктуру белка, чей фолдинг проходит независимо от остальных частей. Многие домены встречаются не только в белках, отвечающих одному гену или даже семейству генов, но и в совершенно разных белках. Достаточно часто им присваивают отдельные названия, так как их присутствие непосредственно влияет на выполняемые белком биологической функции. К примеру, Ca2+-связывающий домен кальмодулина или четыре домена глобина из которых составлен гемоглобин. Так как домены бывают достаточно консервативны и стабильны, с помощью генной инженерии можно «пришить» к одному из белков домен, принадлежащий другому (создав таким образом белок-химеру). В состав домена обычно входит несколько вторичных структур.
