
- •49. Суммарная кривая изменения потенциальной энергии взаимодействия двух молекул или других частиц от расстояния между ними.
- •50. Виды специфических взаимодействий между молекулами.
- •51. Понятие о реактивном поле.
- •52. Сущность физической, химической и физико - химической теорий образования растворов.
- •53. Полиэдрическое строение жидкостей и их растворов, влияние изменения параметров на структуру жидкостей и растворов.
- •54. Понятие об ассоциации и сольватации. Первичные и вторичные сольватные оболочки. Положительная и отрицательная сольватация.
- •55. В каких единицах выражаются концентрации. Методы пересчета одних концентраций в другие.
- •I. Расчет состава по количеству взятого в расчет
- •2. Расчет состава раствора по количеству растворителя
- •56. Аналитическое выражение и физический смысл парциальны мольных величин. Методы их экспериментального и расчетного определения.
51. Понятие о реактивном поле.
Реактивное поле возникает в смеси полярных и неполярных молекул, например, таких как углеводороды и нафтеновые кислоты смолистые соединения и жидкие углеводороды и др. В смесях нефтяных углеводородов полярные молекулы воздействуют полем определенной симметрии (симметрия поля определяется симметрией вакантных молекулярных орбиталей) и напряженности Н на молекулы углеводородов. Это поле возбуждает молекулярные орбитали, содержащие электроны, разделяя заряды, что обусловливает появление (наведение) диполя такой же симметрии и, возможно, несколько меньшей напряженности поля H1. Молекула с индуцированным диполем в свою очередь воздействует своим полем на полярную молекулу, изменяя ее электромагнитное поле, то есть возбуждает в ней реактивное (ответное) поле.
Возникновение реактивного поля приводит к повышению энергии взаимодействия двух частиц, что отражается в создании прочных сольватных оболочек в смеси полярных и неполярных жидкостей у молекул полярного типа. Создание прочных первичных сольватных оболочек упрочняет структуру элементарных пространственных объединений разнородных молекул, то есть полиэдров, что отражается в свойствах растворов полярных и неполярных жидкостей.
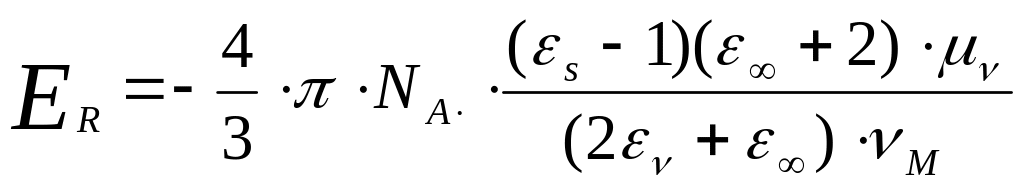
где знак минус определяет притяжение молекул;
![]() - статическая
электрическая проницаемость;
- статическая
электрическая проницаемость;
![]() -
диэлектрическая
проницаемость, обусловленная электронной
и атомной поляризуемостью полярных
молекул;
-
диэлектрическая
проницаемость, обусловленная электронной
и атомной поляризуемостью полярных
молекул;
![]() -
число
Авогадро;
-
число
Авогадро;
![]() - объем,
занимаемый I
молем полярного вещества в изотропной
падкости;
- объем,
занимаемый I
молем полярного вещества в изотропной
падкости;
![]() -
дипольный
момент;
-
дипольный
момент;
![]() - энергия
I
моля полярного вещества в растворе.
- энергия
I
моля полярного вещества в растворе.
Из формулы видно, что величина энергии реактивного доля возрастает с повышением дипольного момента и числа молекул в смеси и с уменьшением мольного объема полярных молекул. При разделении смеси полярных и неполярных молекул на составляющие ректификацией необходимо уменьшать величину реактивного поля, а при экстракции, наоборот, повышать его величину.
52. Сущность физической, химической и физико - химической теорий образования растворов.
Химическая
теория
растворов развивалась Д.И.Менделеевым,
который рассматривал растворы как смеси
непрочных химических соединений молекул
растворенного вещества с молекулами
растворителя. Эти представления
основывались на экспериментальной
зависимости плотности водно-спиртовых
растворов от состава и на зависимости
первой производной от плотности
спиртового раствора по числу моль спирта
![]() в
зависимости от состава раствора.
в
зависимости от состава раствора.
Развитием теории Д.И.Менделеева является полиэдрическая теория образования растворов, согласно которой в жидкости из однородных и разнородных молекул создаются элементарные пространственные группы-полиэдры. Однако химическая теория не может объяснить механизм образования идеальных растворов, отклонения в свойствах реальных растворов от свойств идеальных растворов и др.
Для объяснения свойств идеальных растворов с изменением их состава била предложена физическая теория (В.Ф.Алексеев - 1870--1880 гг.) и была проложена в работах Вант-Гоффа, Аррениуса и др. Согласно этой теории, процесс растворения одного вещества в другом является результатом простого распределения молекул по объему тепловым движением, при этом между взаимодействующими молекулами проявляются только слабые MМB. В результате простого перемешивания молекул веществ процесс растворения при создании идеальных растворов не сопровождается тепловым эффектом. Идеальными свойствами обладают также разбавленные растворы. Идеальными свойствами в любых пределах изменения концентрации растворов обладают смеси веществ с близкими по свойствам молекулами: н-гептан-н-гексан, оптические изомеры.
Общая теория растворов в настоящее время не создана, хотя проводятся широкие научные исследования методами квантовой химии, статистической термодинамики, кристаллохимии, различными физико-химическими методами анализа Д.И.Менделеев указывал, что образование растворов может рассматриваться с двух сторон: с физической и химической, и в растворах виднее, чем где-либо, насколько эти стороны естествознания сближены между собою. В учении о растворах широко используются представления о полиэдрической их структуре и развиваются аналитические методы, связывающие структуру, состав и свойства растворов.
