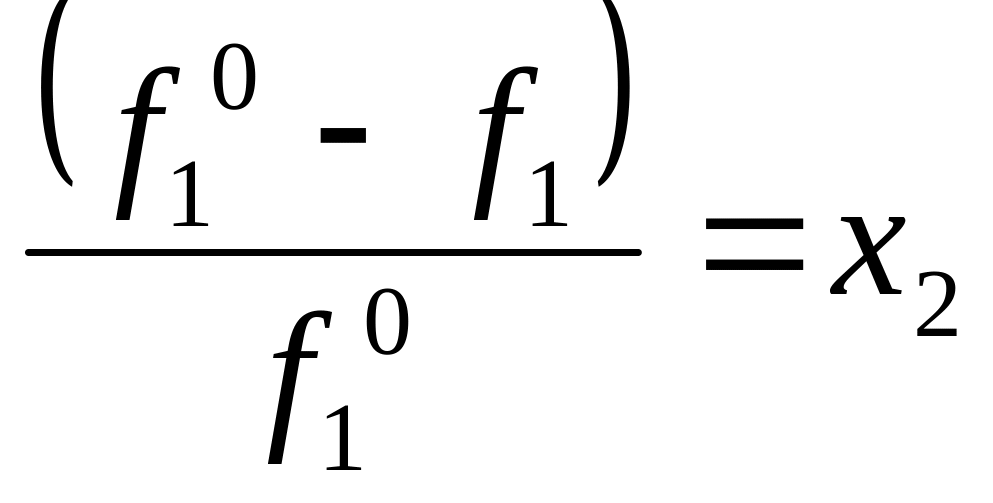- •57. Вывод уравнения Гиббса-Дюгема. Их применение к расчету термодинамических свойств.
- •58. Понятие об активности и коэффициенте активности. Симметричная и несимметричная нормировка стандартного состояния.
- •Основные виды растворов неэлектролитов и электролитов. Влияние различных факторов на растворимость твердых тел.
- •60. Уравнение расчета растворимости твердых тел в жидкости как функция температуры.
- •61. Уравнение зависимости растворимости твердых тел от давления.
- •62. Закон Рауля. Аналитическое выражение, физический смысл понижения давления насыщенных паров над раствором. Следствие из закона Рауля.
- •Диаграмм состояния воды и водного раствора электролита и неэлектролита.
- •Термодинамический вывод уравнения закона Рауля .
Диаграмм состояния воды и водного раствора электролита и неэлектролита.
П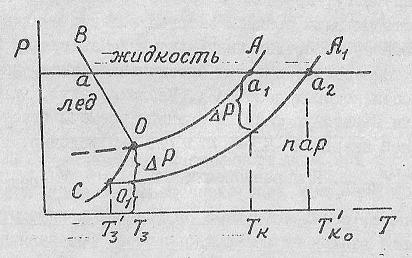 оле
этой диаграммы для чистой воды разделяется
кривыми ОА, ОВ и ОС на три области,
отражающие отражающие гомогенные
системы. Кривая ОА характеризует
равновесие в системе жидкость-пар
оле
этой диаграммы для чистой воды разделяется
кривыми ОА, ОВ и ОС на три области,
отражающие отражающие гомогенные
системы. Кривая ОА характеризует
равновесие в системе жидкость-пар
(f=1-2+2=1), ОВ - лед-жидкость (f=1), ОС - лед-пар (f=1). В точке 0 система трехфазна и имеет нулевое число степеней свободы
f=1-3+2=0.Кривые
ОА, ОВ и ОС описываются уравнениями
Клаузиуса-Клапейронав таком виде.
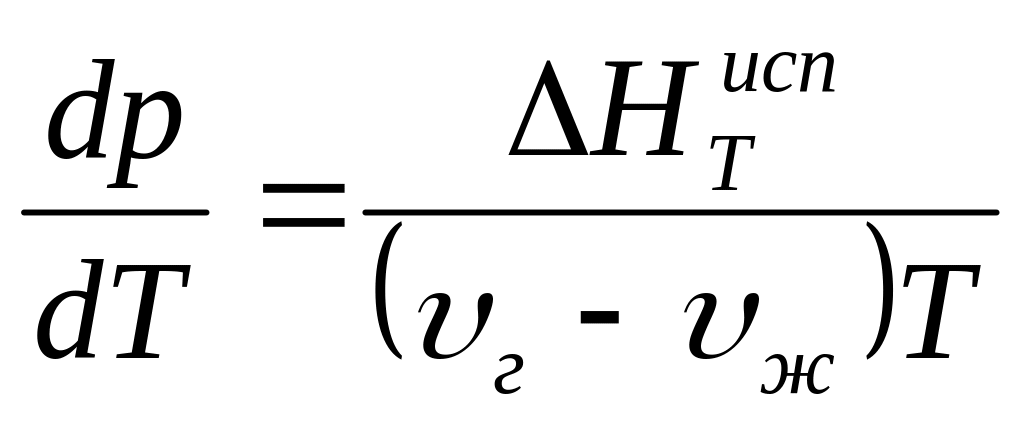
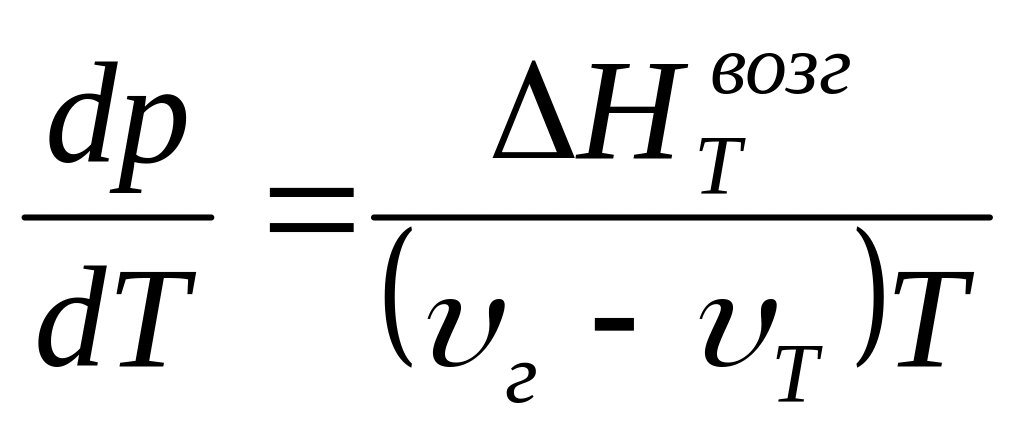
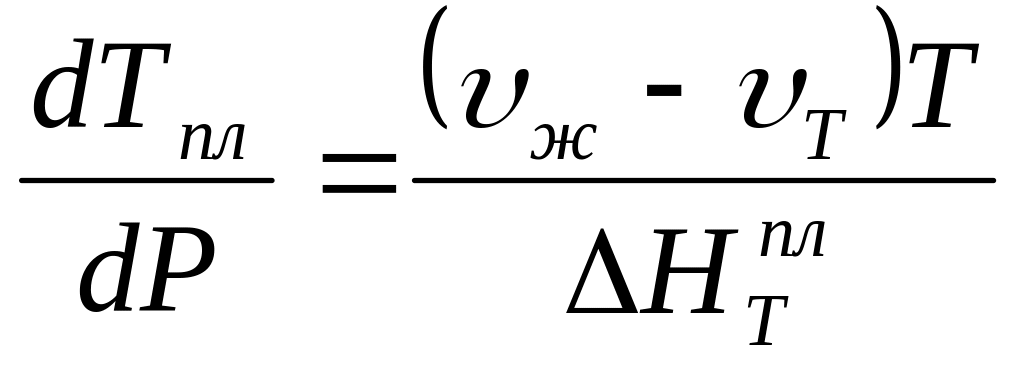
где ∆НТ – теплоты фазовых переходов,
υГ,υЖ,υТ –мольные обемы.
Кривая ОВ располагается под отрицательным углом наклона, так как υЖ<υТВ.
Растворение неэлектролитов в воде (сахар) снижает давление насыщенного пара над раствором при всех температурах (см. кривую О1А1)
Для определения температуры кипения чистой воды и раствора проведем изобару внешнего давления Рвнеш. Тогда точка а1 определяет Ткип чистой воды, а точка а2- Ткип раствора. Известно что жидкость закипает когда внутреннее давление жидкости равно внешнему давлению. Из рис. Видно , что ∆Рнас над раствором ниже, чем над чистой водой на величину ∆Р, поэтому для закипания раствора и для выравнивания давления над раствором с внешним давлением нужно повысить температуру до Тк.
Растворитель замерзает при условии, что давление над жидкостью становиться равным давлению над льдом. Этому условию соответствует точка 0. Над раствором давление ниже, чем над чистой жидкостью на ∆Р. Раствор замерзает, когда давление над ним равно давлению над льдом в растворе. Этому условию соответствует точка О1. Из рис. 40 следует, что раствор замерзает при более низкой температуре, чем чистая вода.
Термодинамический вывод уравнения закона Рауля .
При равновесии химический потенциал вещества одинаков во всех существующих фазах. Очевидно, хим. Потенциал компонента жидкого раствора μi(Ж) будет равен химическому потенциалу пара этого компонента μi(П) над раствором:
μi(Ж)= μi(П)
Подставляем уравнения химических потенциалов идеальных растворов
![]() =
=![]() (1)
(1)
Давление пара вещества над чистым растворителем равно Р0i, поэтому при хi=1 (чистое вещество) уравнение переходит в
![]() =
=![]() (2)
(2)
Подстановка соотношения (2) в (1) дает
![]()
Откуда после небольших упрощений получается уравнение р1=р01х1
Если раствор состоит из 2-х летучих компонентов. А пар обладает свойствами идеального газа, то закон Рауля будет справедлив как для р-ля, так и для растворенного вещества: р1=р01х1 (3)
Р2=р02х2 (4)
Общее давление равно сумме парциальных давлений пара отдельных компонентов:
Р=Р02+(Р01-Р02)х1 (5)
Из уравнений 3-5 следует, что парциальные давления пара р-ля и растворенного вещества, а также общее давление пара над идеальным раствором линейно зависят от состава раствора.
-пар при ↑Т пара не является идеальным, поэтому нужно вводить коэффициент фугитивности.
fi= f0ix2
-при ↑р в р-ре жидкостей для 2-го компонента справаведлив закон Генри :
х2=k ∙pB к-константа Генри
если паровая фаза обладает идеальными свойствами, тогда
к=I/p0B
и закон Генри записывается в такой форме:
pB=p0Bх2
Обобщенный закон Рауля для реальных растворов