
- •1. Предмет, методы и объекты изучения дисциплины «Технология материалов».
- •Механические и технологич св-ва км.
- •4. Кристаллические решетки металлов и их основные типы.
- •5. Дефекты кристаллических решеток. Их влияние на свойства металлов.
- •6. Кристаллизация металлов. Полиморфизм металлов.
- •7. Понятия металлических сплавов. Сплавом называют результат сплавления двух или более компонентов. Компоненты - это химически индивидуальные вещества образовывающие сплав.
- •8. Цветные металлы и сплавы на и их основе. Маркировка.
- •9.Сплавы на основе титана. Их свойства и маркировка.
- •10. Сплавы на основе алюминия. Их свойства и маркировка.
- •11. Сплавы на основе меди. Их свойства и маркировка.
- •12. Правило отрезков для диаграмм состояния.
- •4. Цементит – характеристика дана выше (в компонентах железоуглеродистых сплавов).
- •1 4. Диаграмма состояния железо-цементит. Эвтектические и эвтектоидные превращения
- •15. Диаграмма состояния железо-цементит. Кривые охлаждения сплавах железа с углеродом.
- •16. Термическая обработка сталей. Виды термической обработки.
- •17. Отжиг и нормализация сталей.
- •18. Закалка сталей.
- •19.Отпуск закаленных сталей.
- •20. Химико-термическая обработка сталей.
- •21. Композиционные материалы. Классификация км.
- •22. Композиционные материалы. Способы получения км.
- •23. Порошковая металлургия. Формование и спекание порошков.
- •1. Получение порошков
- •24. Свойства и области применения порошковых материалов.
- •2.1 Химические свойства
- •2.2 Физические свойства
- •25. Неметаллические материалы. Полимеры.
- •26. Пластмассы. Состав и классификация.
- •28. Чугуны. Их структура и свойства.
- •29. Классификация чугунов. Маркировка. Области применения
- •30. Подготовка сырьевых материалов (производство чугуна).
- •31. Основные химические процессы производства чугуна.
- •32. Доменное производство чугуна.
- •33. Внедоменное производство железа.
- •34. Влияние химического состава на свойства чугунов.
- •35. Конвертерный способ производства стали.
- •36. Производство стали в мартеновской печи
- •38. Разливка стали.
- •40. Строение стального слитка.
- •Маркировка легированных сталей
- •45. Инструментальные стали. Конструкционные стали. Области применения.
- •46. Производство меди.
- •47. Производство алюминия.
- •48. Производство титана.
- •49. Характеристика литейного производства. Преимущества и недостатки.
- •50. Классификация литых заготовок.
- •52. Формовочные и стержневые смеси.
- •53. Изготовление литейных форм.
- •54. Приемы ручной формовки.
- •55. Литейное производство. Изготовление стержней.
- •58. Литье по выплавляемым моделям. Литье в металлические формы.
- •59. Центробежное литье. Литье под давлением.
- •60. Литейное производство. Дефекты отливок и способы их устранения.
- •61. Обработка металлов давлением. Классификация процессов.
- •63. Обработка металлов давлением. Прессование.
- •64. Обработка металлов давлением. Волочение.
- •65. Обработка металлов давлением. Ковка.
- •66. Обработка металлов давлением. Штамповка.
- •67. Обработка металлов давлением. Горячая объемная штамповка (гош).
- •68. Обработка металлов давлением. Холодная штамповка.
- •69. Обработка металлов давлением. Листовая штамповка.
- •70. Сварочное производство. Виды сварки.
- •71. Сварочное производство. Ручная электродуговая сварка.
- •72. Сварочное производство. Автоматическая дуговая сварка под флюсом.
- •73. Контактная сварка. Газовая сварка.
- •74. Особые способы сварки: диффузионная, сварка трением, сварка взрывом.
- •75. Виды сварных соединений и швов. Термические процессы в сварочном производстве (наплавка, пайка).
- •76. Обработка металлов резанием. Классификация движений в металлорежущих станках.
- •77. Классификация металлорежущих станков.
- •78. Механическая обработка. Точение.
- •79. Механическая обработка. Сверление.
- •80. Механическая обработка. Протягивание.
- •81. Механическая обработка. Фрезерование.
- •82. Механическая обработка. Шлифование.
- •83. Финишная обработка поверхностей деталей.
11. Сплавы на основе меди. Их свойства и маркировка.
В разнообразных областях техники широко используются сплавы с использованием меди, самыми широко распространёнными из которых являются упоминавшиеся выше бронза и латунь. Оба сплава являются общими названиями для целого семейства материалов, в которые помимо олова и цинка могут входить никель, висмут и другие металлы. Например, в состав так называемого пушечного металла, который в XVI—XVIII вв. действительно использовался для изготовления артиллерийских орудий, входят все три основных металла — медь, олово, цинк; рецептура менялась от времени и места изготовления орудия. В наше время находит применение в военном деле в кумулятивных боеприпасах благодаря высокой пластичности, большое количество латуни идёт на изготовление оружейных гильз.
Для деталей машин используют сплавы меди с цинком, оловом, алюминием, кремнием и др. (а не чистую медь) из-за их большей прочности: 30-40 кгс/мм² у сплавов и 25-29 кгс/мм² у технически чистой меди. Медные сплавы (кроме бериллиевой бронзы и некоторых алюминиевых бронз) не принимают термической обработки, и их механические свойства и износостойкость определяются химическим составом и его влиянием на структуру. Модуль упругости медных сплавов (900-12000 кгс/мм² ниже, чем у стали). Основное преимущество медных сплавов — низкий коэффициент трения (что делает особенно рациональным применением их в парах скольжения), сочетающийся для многих сплавов с высокой пластичностью и хорошей стойкостью против коррозии в ряде агрессивных сред и хорошей электропроводностью. Величина коэффициента трения практически одинакова у всех медных сплавов, тогда как механические свойства и износостойкость, а также поведение в условиях коррозии зависят от состава сплавов, а следовательно, от структуры. Прочность выше у двухфазных сплавов, а пластичность у однофазных. Медноникелевые сплавы используются для чеканки разменной монеты[источник не указан 104 дня].
Медноникелевые сплавы, в том числе и так называемый «адмиралтейский» сплав, широко используются в судостроении и областях применения, связанных с возможностью агрессивного воздействия морской воды из-за образцовой коррозионной устойчивости.
Медь является важным компонентом твёрдых припоев — сплавов с температурой плавления 590—880 градусов Цельсия, обладающих хорошей адгезией к большинству металлов, и применяющихся для прочного соединения разнообразных металлических деталей, особенно, из разнородных металлов, от трубопроводной арматуры до жидкостных ракетных двигателей
12. Правило отрезков для диаграмм состояния.
Правило отрезков.
Посредством правила отрезков можно определить состав фаз в любой двухфазной области и количественное их соотношение. Правило отрезков состоит из двух частей. Первая часть: для того чтобы определить состав фаз через заданную точку в двухфазной области (точка соответствует конкретной температуре) проводят горизонтальную линию до пересечения с линиями, ограничивающими эту область. Проекция точек пересечения на ось концентрации даст нам состав фаз. Вторая часть: для того чтобы определить количество фаз через заданную точку проводят горизонтальную линию до пересечения с линией, ограничивающей эту область. Отрезки между заданной точкой и точками с соответствующим составом фаз обратно пропорциональны их количеству.
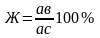
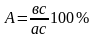
Правило фаз действует только в двухфазной области.
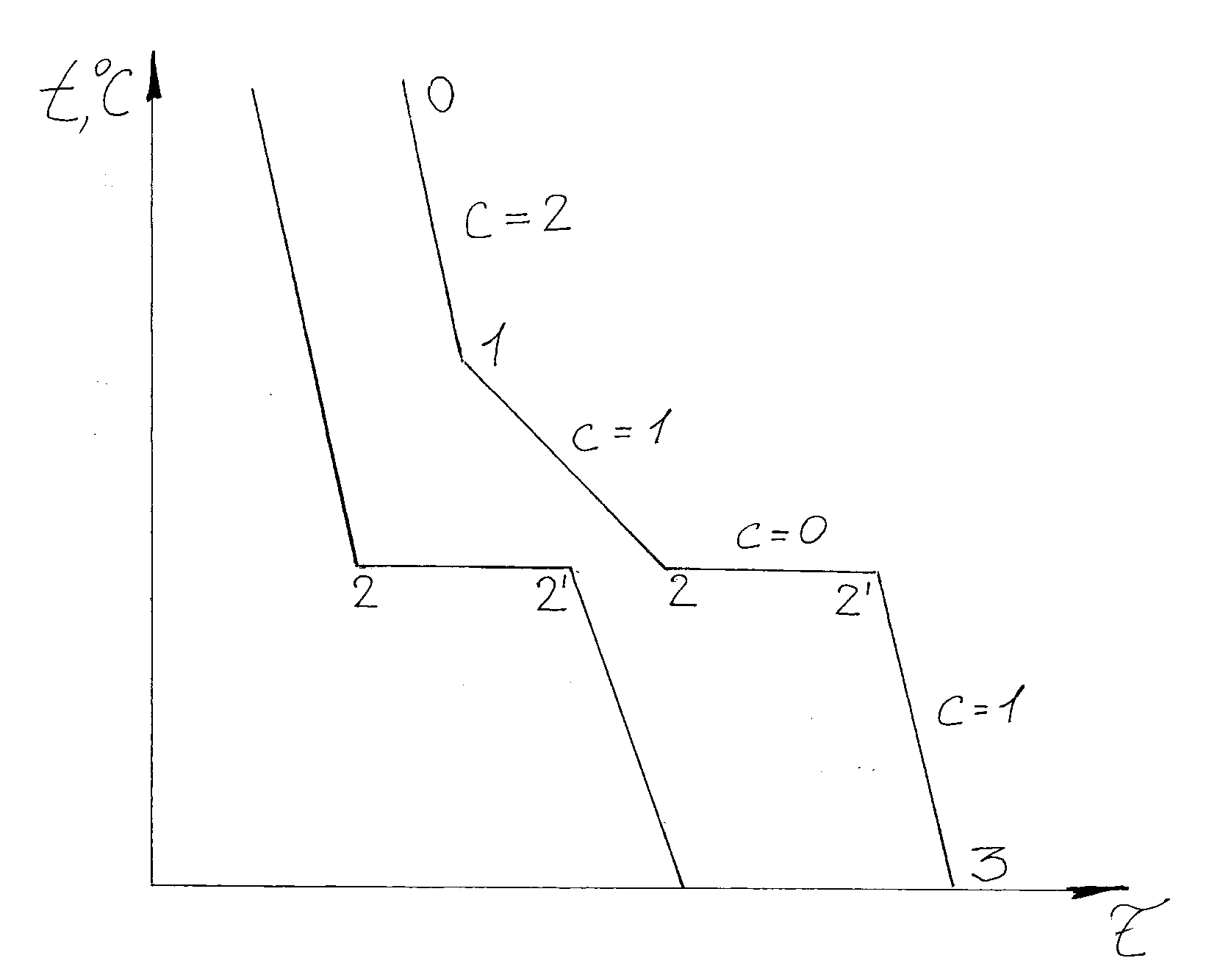
13. Компоненты и фазы в сплавах железа с углеродом.
Компонентами железоуглеродистых сплавов являются железо, углерод и цементит.
1. Железо – переходный металл серебристо-светлого цвета. Имеет высокую температуру плавления – 1539o С ± 5o С.
В твердом состоянии железо может находиться в двух модификациях. Полиморфные превращения происходят при температурах 911o С и 1392o С. При температуре ниже 911o С существует Feα с объемно-центрированной кубической решеткой. В интервале температур 911…1392o С устойчивым является Feγ с гранецентрированной кубической решеткой. Выше 1392o С железо имеет объемно-центрированную кубическую решетку и называется Feδ или высокотемпературное Feα. Высокотемпературная модификация Feα не представляет собой новой аллотропической формы. Критическую температуру 911oС превращения Feα <-> Feγ обозначают точкой A3, а температуру 1392o С превращения Feγ <-> Feδ - точкой А4.При температуре ниже 768o С железо ферромагнитно, а выше – парамагнитно. Точка Кюри железа 768o С обозначается А2.Структуры сталей. Структуры белого чугуна. Структуры сплавов. Структуры сталей и сплавов.Железо технической чистоты обладает невысокой твердостью (80 НВ) и прочностью (предел прочности – σв = 250МПа, предел текучести – σт = 120МПа) и высокими характеристиками пластичности (относительное удлинение – δ = 50%, а относительное сужение – ψ = 80%). Свойства могут изменяться в некоторых пределах в зависимости от величины зерна.Железо характеризуется высоким модулем упругости, наличие которого проявляется и в сплавах на его основе, обеспечивая высокую жесткость деталей из этих сплавов.Железо со многими элементами образует растворы: с металлами – растворы замещения, с углеродом, азотом и водородом – растворы внедрения.2. Углерод относится к неметаллам. Обладает полиморфным превращением, в зависимости от условий образования существует в форме графита с гексагональной кристаллической решеткой (температура плавления – 3500 0С, плотность – 2,5 г/см3) или в форме алмаза со сложной кубической решеткой с координационным числом равным четырем (температура плавления – 5000 0С).В сплавах железа с углеродом углерод находится в состоянии твердого раствора с железом и в виде химического соединения – цементита (Fe3C), а также в свободном состоянии в виде графита (в серых чугунах).3. Цементит (Fe3C) – химическое соединение железа с углеродом (карбид железа), содержит 6,67 % углерода.Аллотропических превращений не испытывает. Кристаллическая решетка цементита состоит из ряда октаэдров, оси которых наклонены друг к другу.Температура плавления цементита точно не установлена (1250, 1550o С). При низких температурах цементит слабо ферромагнитен, магнитные свойства теряет при температуре около 217o С.Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность. Такие свойства являются следствием сложного строения кристаллической решетки.
Цементит способен образовывать твердые растворы замещения. Атомы углерода могут замещаться атомами неметаллов: азотом, кислородом; атомы железа – металлами: марганцем, хромом, вольфрамом и др. Такой твердый раствор на базе решетки цементита называется легированным цементитом.Цементит – соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита. Этот процесс имеет важное практическое значение при структурообразовании чугунов.Фазами железоуглеродистых сплавов являются жидкая фаза, феррит, аустенит, цементит.1. Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы.2. Феррит (Ф) Feα (C) – твердый раствор внедрения углерода в α-железо.Феррит имеет переменную предельную растворимость углерода: минимальную – 0,006 % при комнатной температуре (точка Q), максимальную – 0,02 % при температуре 727o С ( точка P). Углерод располагается в дефектах решетки..При температуре выше 1392o С существует высокотемпературный феррит (δ) (Feδ (C), с предельной растворимостью углерода 0,1 % при температуре 1499o С (точка J)Свойства феррита близки к свойствам железа. Он мягок (твердость – 130 НВ, предел прочности – σв = 300МПа) и пластичен (относительное удлинение – δ = 30%), магнитен до 768o С.3. Аустенит (А) Feγ (С) – твердый раствор внедрения углерода в γ-железо.
Углерод занимает место в центре гранецентрированной кубической ячейки.
Аустенит имеет переменную предельную растворимость углерода: минимальную – 0,8 % при температуре 727o С (точка S), максимальную – 2,14 % при температуре 1147o С (точка Е).
Аустенит имеет твердость 200…250 НВ, пластичен (относительное удлинение – δ = 40..50%), парамагнитен.
При растворении в аустените других элементов могут изменяться свойства и температурные границы существования.
