
- •1. Види науково обґрунтованих класифікацій та номенклатури, що враховують як будову карбонового ланцюга, так і наявність у молекулі певних функціональних груп.
- •2. Ізомерія в органічних сполуках. Просторова будова органічних
- •2)Положения
- •3)Взаємного положення в кільці
- •1. Геометрична :
- •2. Оптична (дзеркальна)
- •3. Поворотна ізомерія ( конформація)
- •4. Динамічна ізомерія
- •4. Загальна характеристика хімічних реакцій біоорганічних сполук.
- •5. Характеристика нуклеофілів та електрофілів.
- •6. Багатоатомні спирти. Будова, номенклатура та ізомерія фенолів, амінів.
- •1. Радикальні заміщення біля насиченого атома Карбону (sr).
- •2. Електрофільне приєднання до ненасичених сполук (ae).
- •3. Електрофільне заміщення в ароматичних сполуках (se).
- •4. Вплив замісників на реакційну здатність аренів.
- •5. Вуглеводні . Алкани, алкени, арени .
- •6. Багатоатомні спирти. Будова, номенклатура та ізомерія фенолів, амінів. ( спрс ).
- •1.Феноли.
- •1.Реакції нуклеофільного приєднання (an) до оксосполук.
- •2.Вплив нуклеофілу на утворення з альдегідами і кетонами нових зв'язків: c-о, с-с, с- н, с- n.
- •3.Альдольна конденсація та її значення для подовження карбонового ланцюга.
- •4.Окиснення альдегідів і кетонів.
- •5. Медико-біологічне значення альдегідів і кетонів. ( спрс).
- •1.Класифікація карбонових кислот, окремі представники монокарбонових кислот.
- •2. Реакції нуклеофільного заміщення (sn) біля sp2- гібридизованого
- •3. Вищі жирні кислоти (вжк) як складові нейтральних ліпідів. Будова
- •5. Функціональні похідні карбонових кислот. ( спрс)
- •1. Хімічні властивості та біологічне значення гідрокси- та амінокислот.
- •1. Класифікація гідроксикислот:
- •2. Біологічне значення кетокислот та їх похідних. Кетонові тіла, діагностичне значення, їх визначення при цукровому діабеті.
- •3. Фенолокислоти та їх похідні. Використання саліцилової кислоти та її похідних у медицині (метилсаліцилат, салол, аспірин, саліцилати натрію) у вигляді лікарських засобів.
- •1. Класифікація амінокислот за будовою карбонового ланцюга, здатністю до синтезу в організмі та полярністю радикала.
- •2. Хімічні властивості а-амінокислот. Реакції поліконденсації з утворенням пептидів. Якісні реакції на α-амінокислоти, пептиди, білки.
- •1. Аліфатичні сполуки зі змішаними функціями
- •1. Класифікація вуглеводів. Таутомерні форми моносахаридів.
- •2. Утворення глікозидів, їхня роль у побудові оліго- та полісахаридів, нуклеозидів. Нуклеотидів та нуклеїнових кислот. Аскорбінова кислота як похідне гексоз, біологічна роль вітаміну с.
- •3. Класифікація дисахаридів за здатністю до окисно-відновних реакцій. Два типи зв'язків між залишками моносахаридів та їх вплив на реакційну здатність дисахаридів.
- •4. Будова, біологічна роль та застосування крохмалю, його складові.
- •5. Структура вуглеводів. (спрс).
- •1. Класифікація гетероциклів за розмірами циклу, кількістю та
- •2. Пятичленні гетероцикли з одним та двома гетероатомами та їхні
- •3. Бензпірол (індол) як складова триптофану та продуктів його перетворення — біологічно активних сполук (триптамін, серотонін) та токсичних речовин (скатол, індол) і продукти їхньою знешкодження.
- •4 Шестичленні гетероцикли з одним та двома гетероатомами -основа
- •5. Лікарські засоби на основі гетероциклічних сполук.( спрс).
- •1. П’ятічленні гетероциклічні сполуки з одним гетероатомом.
- •2. П’ятічленні гетероциклічні сполуки з двома гетероатомами.
- •3. Шестичленні гетероцикли з двома гетероатомами.
- •1. Нуклеозиди та нуклеотиди — продукти неповного гідролізу нуклеїнових кислот. ( спрс)
- •2. Нуклеїнові кислоти — полінуклеотиди, біополімери, що зберігають, передають спадкову інформацію та беруть участь у біосинтезі білка.
- •3. Вільні нуклеотидів (коферменти)— амф, адф, атф, над . Н. Будова та значення 3’,5'-ц-амф, його роль у дії гормонів на клітини.
1.Реакції нуклеофільного приєднання (an) до оксосполук.
Реакції нуклеофільного (багатого на електрони реагенту) приєднання до тригонального атома вуглецю AN .
Подвійний зв'язок в карбонільній групі поляризований, тому в карбонільній групі вуглець завжди несе частковий позитивний заряд, а кисень - негативний. Поява + заряду призводить до того, що характерними реакціями для карбонільних сполук є реакції нуклеофільного приєднання - AN . Альдегіди більш реакційоноздатні в реакціях - AN, чим кетони оскільки 2 радикали утрудняють підхід до
- С –
║
О
Хімічні властивості альдегідів і кетонів :
1) Реакції окислення;
2) Реакції відновлення;
3) Реакції дисмутації;
4) Реакції альдольної конденсації;
5) Реакції утворення ацеталів і напівацеталей;
6) Галоформниє реакції;
7) Реакції приєднання - відщеплення.
2.Вплив нуклеофілу на утворення з альдегідами і кетонами нових зв'язків: c-о, с-с, с- н, с- n.
Можливість нуклеофільної атаки визначається наявністю електронодефіцитного атома Карбону карбонільної групи. Загальна схема реакції нуклеофільного приєднання (AN) до карбонільної групи включає нуклеофільну атаку нуклеофілів по карбонільному атому Карбону (електрофільний центр) з подальшим приєднанням електрофілу до атому Оксигену.

За наведеним механізмом відбувається приєднання води, синильної кислоти, гідросульфіту натрію; спиртів; тіолів; амінів і їх похідних; гідридів металів.
Так, хлоралгідрат, утворений приєднанням води до трихлороцтового альдегіду (хлоралю), застосовується в медичній практиці як заспокійливий та протисудомний засіб. Приєднання синильної кислоти до альдегідної групи використовують для подовження карбонового ланцюга сахарів, а також для одержання кислот (ціан-гідридний синтез). Утворення напівацеталей реалізується при розчиненні глюкози чи її стереомерів у воді.
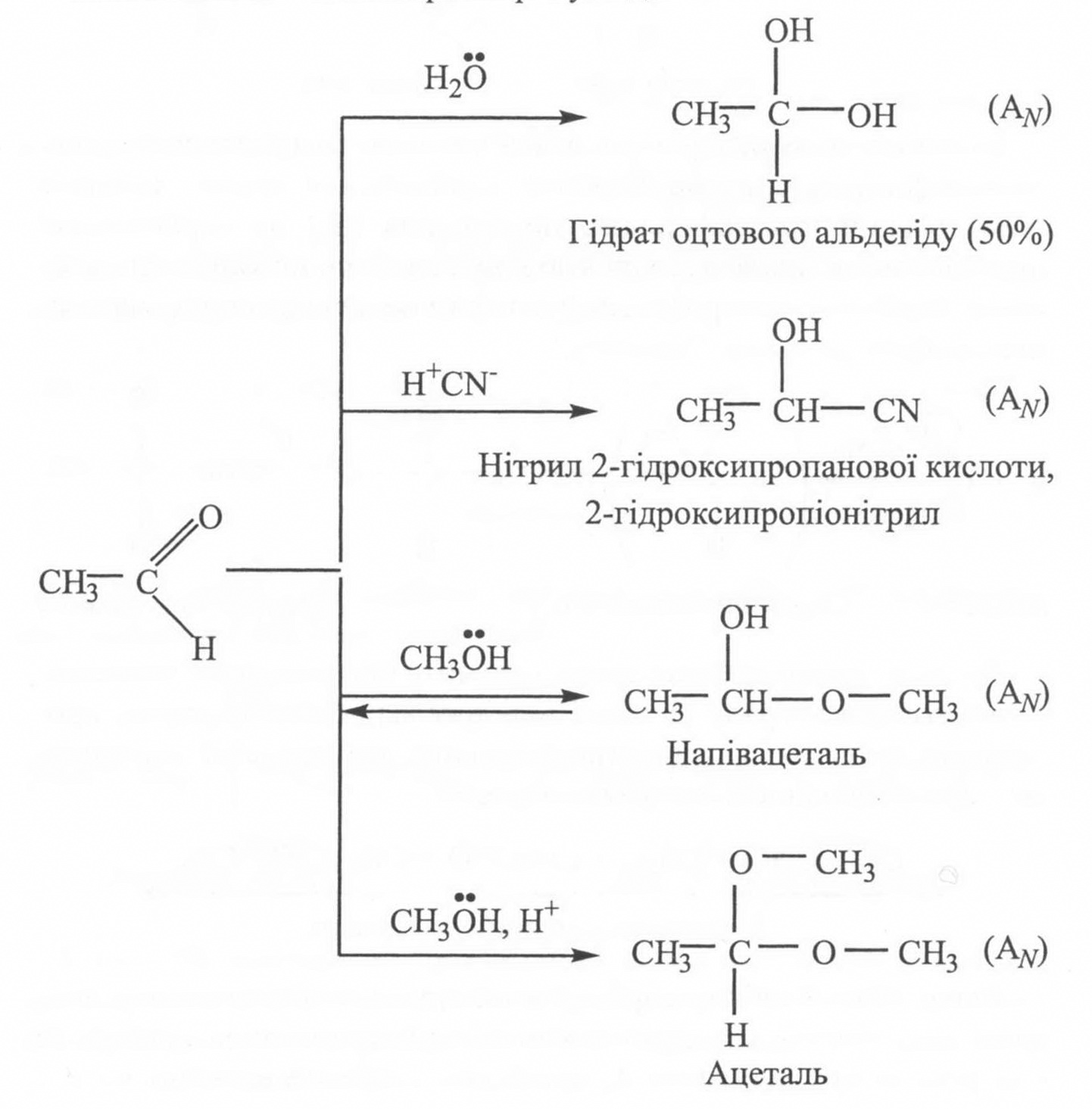
Як гідриди металів використовуютьLіН, NаН, КВН4, LіА1Н4. Як нуклеофіл виступає гідрид-іон (Н-).

3.Альдольна конденсація та її значення для подовження карбонового ланцюга.
Реакции альдольної конденсації. ( подовження ланцюга) Реакции протіка я к під впливом лугіг , так і під впливом кислот. Протікают за механізмом AN, .
1 стадія - утворення карбоаніона :
 О !_
O
О !_
O
 СН2 -
С + NaOH
→ H2O
+ Na+
+ CH2
– C
СН2 -
С + NaOH
→ H2O
+ Na+
+ CH2
– C
H Н H
Оцтовий альдегід карбоанион
2 стадія - нуклеофільна атака карбоаніоном позитивного зарядженого вуглецю карбонильной групи с образованием промежуточного соединения – алкоксидиона.
О
 О !_
О
|
О
О !_
О
|
О
СН3 - С + СН2 - С → [ СН3 - С - СН2 - С ]
Н Н | Н
карбоаніон Н
Оцтовий альдегід алкоксид - іон
3 стадія - алкоксид – іон в водному середовищу присоединяет Н+ из НОН с образованием соединения зі змішаними функціями - альдоля- и регенеруя каталізатор :
_
О ОН
| О | О _
СН3 - С - СН2 - С + НОН → СН3 - С - СН2 - С + ОН
| Н | Н
Н Н
Алкоксид – іон альдоль ( 3 – оксибуталь )
Значення цих реакцій : таким шляхом під впливом ферментів йде освіта :
А) лимонної кислоти в циклі трікарбонових кислот. Би) Утворення гексоз з двох фосфотріоз. У) Нейрамінової кислоти в нервових клітинах.
