
- •Глава 1. Общие вопросы отбора, консервирования и подготовки проб воды к анализу
- •Питьевая вода и вода для промышленных целей Требования, предъявляемые к воде
- •Питьевая вода
- •Вода для промышленных целей
- •Отбор проб воды и пробоподготовка их к анализу
- •Виды отбора проб
- •Виды проб
- •Оборудование для отбора проб воды
- •Отбор проб воды из различных источников
- •Консервирование проб
- •2.10. Определение цветности воды
- •1. Визуальное определение цветности
- •2. Фотоэлектроколориметрическое определение цветности
- •1. Приготовление растворов.
- •2. Приготовление имитационной шкалы цветности.
- •3. Выбор условий определения.
- •4. Построение градуировочного графика.
- •5. Определение цветности анализируемой воды.
- •2.12. Определение кислорода, растворенного в воде. Бпк
- •1. Калибрование кислородной склянки.
- •2. Определение растворенного кислорода.
- •3. Определение бпк
- •3.1. Определение нитритов в воде.
- •1. Приготовление основного раствора
- •2. Приготовление рабочего раствора № 1
- •3. Приготовление рабочего раствора № 2.
- •4. Приготовление серии стандартных растворов.
- •5. Подготовка пробы анализируемой воды.
- •6. Выбор условий определения
- •7. Построение градуированного графика
- •8. Определение концентрации нитритов в пробе
- •.6. Определение хлоридов в воде
- •1. Определение хлорид ионов в воде методом осаждения
- •2. Определение хлоридов в воде потенциометрическим методом анализа
- •1) Приготовление основного раствора.
- •2) Приготовление серии стандартных растворов.
- •3) Приготовление фонового раствора.
- •4) Измерение эдс стандартных растворов на приборе рН-340
- •5) Построение градуированного графика в координатах
- •6) Определение концентрации хлоридов в пробе воды.
- •7) Таблица результатов
- •3.7. Определение железа в воде
- •1. Приготовление основного раствора
- •2. Приготовление рабочего раствора
- •3. Приготовление серии стандартных растворов
- •4. Подготовка пробы анализируемой воды
- •5. Выбор условий определения
- •6. Построение градуировочного графика
- •7. Определение концентрации железа в пробе
- •3.8. Определение хрома в воде
- •1. Приготовление основного раствора
- •2. Приготовление рабочего раствора № 1
- •3. Приготовление рабочего раствора № 2
- •4. Приготовление серии стандартных растворов
- •5. Подготовка пробы анализируемой воды
- •6. Выбор условий определения
- •7. Построение градуировочного графика
- •8. Определение концентрации хрома в воде
- •3.10. Определение алюминия в воде
- •1. Приготовление основного раствора
- •2. Приготовление рабочего раствора
- •3. Приготовление серии стандартных растворов.
- •4. Подготовка пробы анализируемой воды.
- •5. Выбор условий определения
- •7. Построение градуированного графика
- •8. Определение концентрации алюминия в пробе
- •3.14. Определение кальция в воде
- •4.1. Определение фенолов в воде
- •Определение летучих с паром фенолов (определение относительно больших концентраций)
- •1. Приготовление основного раствора
- •2. Приготовление рабочего раствора
- •3. Приготовление серии стандартных растворов
- •4. Подготовка пробы анализируемой воды
- •5. Выбор условий определения
- •6. Построение градуированного графика.
- •7. Определение концентрации фенола в воде
1. Приготовление основного раствора
ЗАДАЧА. Сколько граммов нитрита натрия необходимо взять для приготовления 1 литра раствора с массовой концентрацией нитрит-ионов 100 мкг/мл?
Дано:
Сm (NO2) = 100,00 мкг/мл (мг/л)
М(NO2) = 46 г/моль
М( NaNO2) = 69 г/моль
V = 1000,00 мл
Вычислить массу навески mн .

(1) (2) (3)
Сколько г NO2 содержится в 1 литре раствора;
Сколько моль NO2 содержится в 1 литре раствора; столько же моль NaNO2 содержится в 1 литре раствора.
Сколько г NaNO2 содержится в 1 литре раствора.
Методика приготовления раствора.
0,1500 г х.ч. NaNO2 взвешивают на аналитических весах, количественно переносят в мерную колбу на 1 литр, добавляют 2 мл хлороформа, растворяют, объем доводят в мерной колбе до метки, закрывают пробкой, перемешивают.
2. Приготовление рабочего раствора № 1
ЗАДАЧА. В мерной колбе 500 мл приготовить рабочий раствор № 1 с массовой концентрацией нитрит - ионов 10 мкг/мл, из основного раствора с массовой концентрацией нитрит – ионов 100 кг/мл.
Дано:
Сm (NO2-)1 = 100,00 мкг/мл
Сm (NO2-)2 = 10,00 мкг/мл
Vм.к. = 500,00 мл
Вычислить объем основного раствора.
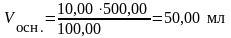
Методика приготовления рабочего раствора № 1
50,00 мл основного раствора отмеривают пипеткой, переносят в мерную колбу 500 мл, разбавляют дистиллированной водой до метки, закрывают пробкой, перемешивают.
3. Приготовление рабочего раствора № 2.
ЗАДАЧА. В мерной колбе 500 мл приготовить рабочий раствор с массовой концентрацией нитрит - ионов 0,5 мкг/мл из рабочего раствора №1 с массовой концентрацией нитрит - ионов 10 мкг/мл.
Дано:
Сm (NO2-)1 = 10,00 мкг/мл
Сm (NO2-)2 = 0, 50 мкг/мл
Vм.к. = 500,00 мл
Вычислить объем рабочего раствора № 1.

Методика приготовления рабочего раствора № 2
25,00 мл рабочего раствора № 1 отмеривают пипеткой, переносят в мерную колбу 500 мл, разбавляют дистиллированной водой до метки, закрывают пробкой, перемешивают.
4. Приготовление серии стандартных растворов.
В мерные колбы 50,00 мл по бюретке отмеривают рабочий раствор № 2: 0 мл; 1,00 мл; 2,00 мл; 5,00 мл; 10,00 мл; 15,00 мл; 20,00 мл; 25,00 мл; 30,00 мл. Объемы в мерных колбах доводят до метки дистиллированной водой. В каждую колбу с помощью пипеток добавляют 1,00 мл сульфаниловой кислоты (рН = 1,4). Дают постоять 3-10 мин., затем 1,00 мл раствора альфа-нафтиламина, 1,00 мл ацетата натрия (рН = 2 –2,5), закрывают пробкой, перемешивают.
Вычисление концентрации приготовленных стандартных растворов:







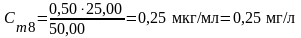

5. Подготовка пробы анализируемой воды.
50,00 мл анализируемой воды отмеривают мерной колбой, затем с помощью пипеток добавляют 1,00 мл раствора сульфаниловой кислоты (рН = 1,4). Дают постоять 3-10 мин., затем приливают 1,00 мл альфа- нафтиламина, 1,00 мл ацетата натрия (рН = 2-2,5). Закрывают пробкой, перемешивают.
Примечание.
При наличии в лаборатории реактива Грисса к 50,00 мл анализируемой воды добавляют 2,00 мл реактива Грисса, закрывают пробкой, перемешивают и через 30 мин. измеряют абсорбционность.
