
- •Глава 1. Общие вопросы отбора, консервирования и подготовки проб воды к анализу
- •Питьевая вода и вода для промышленных целей Требования, предъявляемые к воде
- •Питьевая вода
- •Вода для промышленных целей
- •Отбор проб воды и пробоподготовка их к анализу
- •Виды отбора проб
- •Виды проб
- •Оборудование для отбора проб воды
- •Отбор проб воды из различных источников
- •Консервирование проб
- •2.10. Определение цветности воды
- •1. Визуальное определение цветности
- •2. Фотоэлектроколориметрическое определение цветности
- •1. Приготовление растворов.
- •2. Приготовление имитационной шкалы цветности.
- •3. Выбор условий определения.
- •4. Построение градуировочного графика.
- •5. Определение цветности анализируемой воды.
- •2.12. Определение кислорода, растворенного в воде. Бпк
- •1. Калибрование кислородной склянки.
- •2. Определение растворенного кислорода.
- •3. Определение бпк
- •3.1. Определение нитритов в воде.
- •1. Приготовление основного раствора
- •2. Приготовление рабочего раствора № 1
- •3. Приготовление рабочего раствора № 2.
- •4. Приготовление серии стандартных растворов.
- •5. Подготовка пробы анализируемой воды.
- •6. Выбор условий определения
- •7. Построение градуированного графика
- •8. Определение концентрации нитритов в пробе
- •.6. Определение хлоридов в воде
- •1. Определение хлорид ионов в воде методом осаждения
- •2. Определение хлоридов в воде потенциометрическим методом анализа
- •1) Приготовление основного раствора.
- •2) Приготовление серии стандартных растворов.
- •3) Приготовление фонового раствора.
- •4) Измерение эдс стандартных растворов на приборе рН-340
- •5) Построение градуированного графика в координатах
- •6) Определение концентрации хлоридов в пробе воды.
- •7) Таблица результатов
- •3.7. Определение железа в воде
- •1. Приготовление основного раствора
- •2. Приготовление рабочего раствора
- •3. Приготовление серии стандартных растворов
- •4. Подготовка пробы анализируемой воды
- •5. Выбор условий определения
- •6. Построение градуировочного графика
- •7. Определение концентрации железа в пробе
- •3.8. Определение хрома в воде
- •1. Приготовление основного раствора
- •2. Приготовление рабочего раствора № 1
- •3. Приготовление рабочего раствора № 2
- •4. Приготовление серии стандартных растворов
- •5. Подготовка пробы анализируемой воды
- •6. Выбор условий определения
- •7. Построение градуировочного графика
- •8. Определение концентрации хрома в воде
- •3.10. Определение алюминия в воде
- •1. Приготовление основного раствора
- •2. Приготовление рабочего раствора
- •3. Приготовление серии стандартных растворов.
- •4. Подготовка пробы анализируемой воды.
- •5. Выбор условий определения
- •7. Построение градуированного графика
- •8. Определение концентрации алюминия в пробе
- •3.14. Определение кальция в воде
- •4.1. Определение фенолов в воде
- •Определение летучих с паром фенолов (определение относительно больших концентраций)
- •1. Приготовление основного раствора
- •2. Приготовление рабочего раствора
- •3. Приготовление серии стандартных растворов
- •4. Подготовка пробы анализируемой воды
- •5. Выбор условий определения
- •6. Построение градуированного графика.
- •7. Определение концентрации фенола в воде
1. Приготовление основного раствора
ЗАДАЧА. Сколько граммов дихромата калия необходимо взять для приготовления 1 литра раствора с массовой концентрацией хрома 1,00 мг/мл?
Дано: Сm(Сr6+) = 1,00 мг/мл (г/л)
М(Cr6+ ) = 52,00 г/моль
М(К2Сr2О7) = 294,185 г/моль
Vм.к. = 1000,00 мл
Вычислить массу навески mн ?

(1) (2) (3)
1) Сколько моль ионов Cr6+ содержится в 1 литре раствора;
2) Сколько моль дихромата калия содержится в 1 литре раствора;
3) Сколько г K2Cr2O7 содержится в 1 литре раствора.
Методика приготовления раствора
2,8287 г х.ч. К2Сr2О7 взвешивают на аналитических весах, количественно переносят в мерную колбу 1 литр, растворяют, объём в мерной колбе доводят дистиллированной водой до метки, закрывают пробкой, перемешивают.
2. Приготовление рабочего раствора № 1
ЗАДАЧА. В мерной колбе 500 мл приготовить рабочий раствор с массовой концентрацией хрома 0,05 мг/мл из основного раствора с массовой концентрацией хрома 1,00 мг/мл.
Дано: Сm(Сr6+)1 = 1,00 мг/мл
Сm(Cr6+)2 = 0,050 мг/мл
Vм.к. = 500,00 мл
Вычислить объём основного раствора.

Методика приготовления рабочего раствора № 1
25,00 мл основного раствора отмеривают пипеткой, переносят в мерную колбу 500 мл, разбавляют дистиллированной водой до метки, закрывают пробкой, перемешивают.
3. Приготовление рабочего раствора № 2
ЗАДАЧА. В мерной колбе 500 мл приготовить рабочий раствор с массовой концентрацией хрома 0,002 мг/мл из рабочего раствора № 1 с массовой концентрацией хрома 0,05 мг/мл.
Дано: Сm(Сr6+)1 = 0,050 мг/мл
Сm(Cr6+)2 = 0,0020 мг/мл
Vм.к. = 500,00 мл
Вычислить объём рабочего раствора № 1?

Методика приготовления рабочего раствора № 2
20,00 мл рабочего раствора № 1 отмеривают пипеткой, переносят в мерную колбу 500 мл, разбавляют дистиллированной водой до метки, закрывают пробкой, перемешивают.
4. Приготовление серии стандартных растворов
В мерные колбы 100,00 мл по бюретке отмеряют рабочий раствор № 2: 0 мл; 0,10 мл; 0,50 мл; 1,00 мл; 1,50 мл; 2,00 мл; 3,00 мл. В каждую мерную колбу добавляют дистиллированную воду до метки, затем с помощью пипеток добавляют 1 мл раствора Н2SO4, 0,3 мл Н3РО4, перемешивают; затем добавляют 2 мл раствора дифенилкарбазида и смесь снова перемешивают.
Вычисление концентрации приготовленных стандартных растворов:
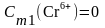
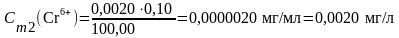


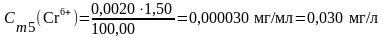


5. Подготовка пробы анализируемой воды
100,00 мл анализируемой воды отмеривают мерной колбой, затем с помощью пипеток добавляют 1 мл раствора Н2SO4, 0,3 мл Н3РО4, перемешивают; затем добавляют 2 мл раствора дифенилкарбазида и смесь снова перемешивают.
6. Выбор условий определения
Условия определения выбирают через 10 минут.
а) Выбор светофильтра. Для практического выбора светофильтра берут стандартный раствор максимальной концентрации. Измеряют абсорбционность (А) этого раствора на всех светофильтрах по отношению к холостому раствору. По полученным данным строят график в координатах: абсорбционность (А) - длина волны падающего света ().

Выбирают для анализа тот светофильтр, который дает максимальное значение абсорбционности (А). В данном случае - зеленый светофильтр.
б) Выбор кюветы. Для выбора кюветы (толщины поглощающего слоя) берут стандартный раствор максимальной концентрации. Измеряют абсорбционность (А) на выбранном светофильтре во всех кюветах по отношению к холостому раствору. Абсорбционность должна быть близкой к единице.
