
спектр и фотометр
.pdfэкспериментально относительно легко, так как его положение зависит от концентрации и температуры, причем при разведении сигнал смещается в область сильного поля. Кроме того, такой сигнал исчезает при растворении в D2О за счет водородного обмена.
Положение сигнала от протона группы СООН в карбоновых кислотах (δ 10-13 м.д.) более постоянно и меньше изменяется даже при сильном разведении достаточно характеристично.
Если на магнитное экранирование данного протона действуют одновременно две группировки, вызывающие смещение химического сдвига сигнала в область слабого поля, то это смещение будет, соответственно, ещё больше.
Таким образом, по величине химического сдвига может быть определено положение протона в органической молекуле. Однако сигналы от протонов, незначительно отличающиеся по химическому сдвигу, могут перекрываться полностью или частично. Так, незначительно различающиеся по положению метиленовые группы в ациклических цепях или циклических системах часто сливаются в один широкий сложный сигнал.
1.5.3. Совместное применение спектральных методов
Все рассмотренные выше спектральные методы дают определённую информацию о структуре вещества. Однако каждый из этих методов имеет определенные ограничения, и все они, применяемые по отдельности, в большинстве случаев не позволяют однозначно установить строение исследуемых соединений. Совместное применение методов неизмеримо расширяет их возможности, так как полученные каждым отдельным путем сведения уточняют и дополняют друг друга. Комбинация УФ-, ИК-, ЯМР 1Н- и масс-спектров в подавляющем большинстве случаев позволяет решать структурно-аналитические задачи, включая установление строения сложных природных соединений, при минимальных затратах вещества.
В особо сложных случаях, в частности при определении пространственных особенностей молекулы, приходится прибегать к данным рентгеноструктурного анализа, рассмотрение которого выходит за рамки данного учебного пособия.
Комплекс приёмов совместного использования спектральных данных довольно разнообразен и в сложных случаях представляет собой скорее искусство, чем науку. На тех элементарных примерах, которые рассматриваются ниже, даются лишь начальные общие навыки обращения со спектральным материалом.
Обычно, приступая к исследованию строения вещества, располагают так называемой «первичной информацией». Если вещество получено син-
61
тетическим путем, о многом говорит путь его синтеза. Необозримый круг возможных структур резко ограничивается данными элементного анализа или, в современном варианте, масс-спектрометрии высокого разрешения.
Иными словами, перед рассмотрением спектральных данных брут- то-формула вещества известна и, следовательно, известен «показатель ненасыщенности», а также набор гетероатомов, составляющих определенные функциональные группы.
Предложить типовую схему решения задач по установлению строения органических соединений не представляется возможным, ибо каждый раз последовательность логических заключений естественно, будет различной.
В простейших случаях может быть рекомендована следующая цепь размышлений:
а) извлечь из предварительных данных всю возможную информацию; б) получить из данных масс-спектра молекулярную массу вещества; его брутто-формула, при отсутствии данных масс-спектра высокого раз-
решения, может быть найдена из данных элементного анализа; в) по данным УФ-спектра определить наличие в молекуле системы со-
пряженных двойных связей, ароматического ядра и карбонильной группы; г) по данным ИК-спектра подтвердить выводы, полученные в пункте «в», и по характеристическим частотам колебаний определить присут-
ствующие в веществе функциональные группы; д) подтвердить по данным ЯМР 1Н спектров наличие в веществе обна-
руженных функциональных групп и попытаться определить расположение атомов водорода в молекуле;
е) рассматривая основные направления фрагментации в масс-спектре, определить основные структурные элементы молекулы;
ж) сформулировать предположение о структуре вещества (их может быть несколько);
з) повторно рассматривая ИК, ЯМР 1Н- и масс-спектры, проверить соответствие предполагаемой структуры соответствующей спектральной информации.
Итак, решайте предлагаемые Вам задачи, сверяясь с цифровым (в основном табличным) материалом, приведенным выше. Старайтесь научиться основную информацию из предлагаемых спектров (С=С, ароматическое ядро, С=О и т. д.) получить сразу, не заглядывая в таблицы. Ниже приводятся примеры комплексного использования спектральных данных для установления строения вещества.
Пример 1. Соединение С4Н8О2. УФ-спектр: λmax (в гексане) 207 нм
(lgε 1,84). Спектр ЯМР 1Н (δ, м. д.): 1,15 (триплет); 2,0 (синглет); 4,0 (ква-
62
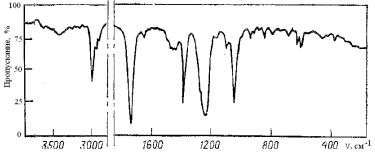
друплет); соотношение интенсивностей сигналов 3:3:2. Масс-спектр (m/z): 88(10).,73(12),70(6),61(15),45(10), 44(3), 43(100), 42(8), 29(20), 28(10), 27(9), 15(8). ИК-спектр: см. рисунок 29. Установите строение вещества.
Рис. 29. ИК-спектр этилового эфира уксусной кислоты
Решение. УФ-спектр вещества (обращает на себя внимание не только положение максимума, но и малая интенсивность поглощения) соответствует карбоновой кислоте или ее функциональному производному.
ИК-спектр показывает наличие в веществе карбонильной группы (1742 см-I), причем частота поглощения и наличие двух интенсивных полос в области νс-о (1054 и 1233 см-1) позволяют предлагать, что эта группа входит в состав сложноэфирной группировки. Прочие функциональные группы (в особенности гидроксильная) по данным ИК-спектра отсутствуют.
Спектр ЯМР 1Н не содержит сигналов от протона карбоксильной группы (в области δ 10-13 м. д.); следовательно, вещество является сложным эфиром.
Согласно брутто-формуле, в веществе отсутствуют кратные угле- род-углеродные связи и циклы, следовательно, вещество может иметь структуры: НСООС3Н7, СН3СООС2Н5, С2Н5СООСН3. При рассмотрении спектра ЯМР 1Н выявляется наличие характерной для этильной группы комбинации сигналов δ 1,15 м. д. (триплет, 3Н, два протона при соседнем С-атоме) и δ 4,00 м. д. (квадруплет, 2Н, три протона при соседнем С-ато- ме), причём химический сдвиг сигнала от метиленовой группы соответствует её положению при атоме кислорода. Синглетный сигнал δ 2,0 м. д. (3Н) легко идентифицируется как принадлежащий протонам метильной группы при карбонильной группе как по химическому сдвигу, так и по отсутствию спин-спинового взаимодействия (отсутствие протонов при соседнем углеродном атоме).
Таким образом, вещество является этиловым эфиром уксусной кислоты СН3СООС2Н5.
63
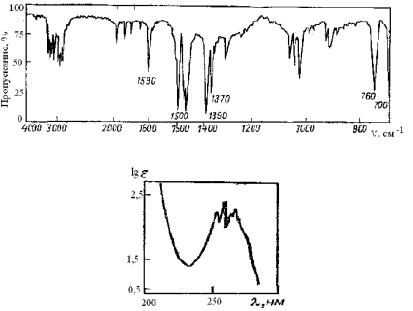
Пример 2. Жидкость C9HI2. Спектр ЯМР 1Н содержит дублет при δ 1.18 м. д., септет при δ 3,0 м. д. и синглет при δ 7,2 м. д.; соотношение интенсивностей сигналов 6:1:5. ИК- и УФ-спектры представлены на рисунках 30 и 31. Определите структуру вещества.
Рис. 30. ИК-спектр изопропилбензола
Рис. 31. УФ-спектр изопропил-бензола
Решение. УФ-спектр вещества имеет типичный для одноядерных аренов максимум с тонкой структурой при 262 нм. Согласно брутто-формуле вещество является углеводородом. Поглощение максимума (батохромный сдвиг на 7 нм по отношению к положению максимума в спектре бензола) хорошо согласуется с наличием в ядре одного алкильного заместителя. ИК-спектр вещества имеет типичный набор полос замещенного бензола (νС-С 1590, 1500; δС-Н 760 и 700 см-1; νСН – набор полос поглощения при ~3060 см-1). Наличие четырех полос поглощения в области 1650-2000 см-1 (см. рис. 30) является свидетельством в пользу того, что в бензольном ядре имеется один заместитель, т. е. соединение представляет собойпропилили изопропилбензол.
В спектре ЯМР 1Н содержатся три сигнала с соотношением интенсивностей 5:1:6. Протоны ароматической системы проявляются острым синглетом δ 7,2 м. д. (5Н), что дополнительно подтверждает наличие единственного алкильного заместителя в бензольном ядре. Заместителю принадлежат два сигнала: δ 1,18 м. д. (дублет, 6Н), и δ 3,0 м. д.
64
(7 компонентов, lН). Первый из сигналов соответствует двум эквивалентным метильным группам, имеющим единственный протон при соседнем углеродном атоме; единственный протон, дающий другой сигнал, имеет при соседних С-атомах 6 протонов (сигнал семикомпонентный). Следовательно, соединение является изопропилбензолом. С6Н5–СН(СН3)2.
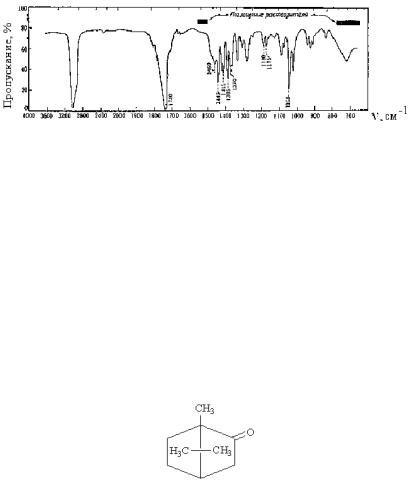
Пример 3. Определите структуру монотерпена С10Н16О. В спектре ЯМР 1Н имеются три синглетных сигналов метильной группы. ИК-спектр представлен на рисунке 32.
Рис. 32. ИК-спектр камфоры
Решение. Из данных ИК- и ЯМР-спектров вытекает, что степень ненасыщенности молекулы равна 3. Одна из степеней относится к пятичленному циклическому кетону. Из трех метильных групп, присоединенных к четвертичному углеродному атому (спектр ПМР), две составляют гем-диметильную группу (расщепление полос 1380, 1190 и 1175 см-1). Присутствует также активная метиленовая группа.
1740 см-1: Пятичленный циклический кетон (1745 см-1). 1460 и 1445 см-1: СН2 и СНз.
1415 см-1: Активная метиленовая группа. 1385 и 1370 см-1: гем-диметильная группа.
1190 и 1175 см-1: Две метильных группы, присоединенных к четвертичному углеродному атому (1215 и 1195 см-1).
1050 см-1: Алифатический кетон (1100 см-1).
Таким образом, представленные данные ИК- и ЯМР 1Н-спектров согласуются со структурой камфоры.
камфора
65
ЧАСТЬ 2. КОНТРОЛЬ КАЧЕСТВА ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ
СИСПОЛЬЗОВАНИЕМ МЕТОДОВ СПЕКТРОСКОПИИ
ИХРОМАТОГРАФИИ
Различные этапы исследования потенциальных лекарственных средств в соответствии с современными Правилами организации производства и контроля качества лекарственных средств (GLP или GMP) требуют привлечения определенного набора физических, химических и физико-химических методов.
На этапе синтеза новых соединений и изучения их фармакологической активности с помощью физических и химических методов устанав-
ливают физико-химические константы и степень чистоты.
При переходе к доклиническим и клиническим испытаниям происхо-
дит формирование нормативных документов (НД).
На этом этапе для испытаний подлинности обычно используют качественный функциональный анализ, определение температуры плавления, а также методы УФ-, ИК- и ЯМР-спектроскопии.
Для количественного определения биологически активного веще-
ства используют титриметрические методы, УФ-спектрофотометрию,
ГЖХ, ВЭЖХ и другие методы.
Биофармацевтические и фармакокинетические исследования
требуют применения высокочувствительных методов (УФ-спектрофо-
тометрия, флуориметрия, масс-спектро-метрия, радиохимические методы).
Этап перехода к промышленному производству сопровождается адаптацией разработанных методик оценки доброкачественности к условиям фармацевтического предприятия и проверки стабильности основных показателей качества на опытно-промышленных сериях лекарственных средств (ЛС).
Таким образом, аналитические методы широко применяются на всех стадиях разработки новых ЛС, включая синтетические, технологические, биофармацевтические, фармакокине-тические исследования.
Разработка НД на лекарственные вещества (ЛВ) и лекарственные формы (ЛФ) – это итог аналитических исследований, связанных с созданием ЛС.
Руководствуясь НД, провизор-аналитик осуществляет затем систематический контроль за качеством ЛС как в процессе их производства, так и при поступлении на аптечные базы (склады) и в аптеки.
66

В связи с тем, что различные методы спектроскопии подробно рассмотрены в I части данного учебного пособия, а методы хроматографического анализа ЛС широко представлены в ранее изданных нами учебных пособиях (А.З. Абышев, С.Н. Трусов, А.В. Ложкин «Лекарственные препараты антиангинального действия»,Санкт-Петербург, 2010, 140с и А.З. Абышев, С.Н. Трусов, Н.И. Котова, М.П. Блинова «Синтез, свойства и контроль качества витаминных препаратов и витаминоподобных веществ», Санкт-Петербург, 2010, 133с), в настоящем втором издании учебного пособия представляем некоторые варианты методов хроматографии, отсутствующих в вышеуказанных учебных пособиях. В качестве примера рассматриваем результаты анализа различных групп ЛС методами тонкослойной хроматографии (ТСХ), колоночной хроматографии (КХ), гель – хроматографии, высокоэффективной жидкостной хроматографии (ВЭЖХ), газовой жидкостной хроматографии (ГЖХ), вариант сочетания последней с масс-спектрометрией и др.
Ниже представлены некоторые варианты адсорбционной и гель-хро- матографии, отвечающие требованиям, предъявляемым GLP или GMP при разработке новых ЛС в лабораторных и промышленных условиях
(см. рис. 1, 2).
67

Рис. 3. Гель-хроматография в промышленных условиях
68

Рис. 4. Комбинированная гель-хроматография в промышленных условиях
Высокоэффективная жидкостная хроматография (ВЭЖХ) отлича-
ется от ГЖХ тем, что подвижной фазой служит не газ, а жидкость, причем она проходит через колонку наполненную сорбентом, с большой скоростью за счет значительного давления.
Поэтому ВЭЖХ позволяет разделять многокомпонентные смеси на индивидуальные вещества высокой степени чистоты. ВЭЖХ отличается высокой чувствительностью (до 10-6 г).
На разделение 10-15 компонентов затрачивается 20-30 мин.
Жидкостный хроматограф включает такие узлы, как дозатор, насос
высокого давления, высокоэффективную колонку, детектор с регистрирующим устройством.
Колонки изготавливают из нержавеющей стали, они имеют длину
10-25см, внутренний диаметр0,3-0,8сми плотно набиваются адсорбентом с размером частиц 5-10 мкм.
69

Вкачестве элюента используют различные углеводороды в сочетании
сэтанолом.
Детектором обычно служит спектрофотометр с переменной длиной волны (190-900 нм), но существуют также флуориметрические, элек-
трохимические и другие детекторы.
Подлинность испытуемых ЛВ подтверждают по времени выхода каждого компонента смеси из колонки, которое будет лабильно при одинаковых условиях проведения эксперимента.
Количественное содержание рассчитывается по площади пика,ко-
торая пропорциональна количеству ЛВ в пробе.
В настоящее время метод ВЭЖХ широко применяется при изучении фармакокинетики различных лекарственных веществ и их лекарственных форм.
Не давно данная методика была успешно апробирована в исследованиях клинической фармакокинетики антиангинального препарата амло-
дипина.
Хроматограмма реального образца плазмы крови человека на 10 день через 5 ч после приема препарата (1 таблетка, содержащая 5 мг активного вещества) и современный ВЭЖХ приведены на рисунках 5 и 6.
Рис. 5. Хроматограмм субстанции амлодипина
Далее представляем конкретные примеры ЛВ и их лекарственные формы, в контроле качества которых были использованы современные методы спектроскопии и хроматографии по следующим показателям:
1.Синтез (если он не описан в учебниках по фармацевтической химии или в других источниках) и определение чистоту и строения ЛВ;
2.Определение подлинности (идентификации) ЛВ;
3.Количественное определение;
4.Применение.
70
