
- •Московская Медицинская Академия им. И.М.Сеченова
- •Аттестационный лист студента
- •Основы количественного анализа. Способы выражения концентрации раствора.
- •Задания для самостоятельной работы
- •Основы количественного анализа.
- •Кислотно – основное титрование.
- •Дата_________ Лабораторная работа № ______
- •Определение массы гидроксида натрия в растворе
- •Расчеты:
- •Задания для самостоятельной работы
- •Химическая термодинамика. Энергетика химических реакций.
- •I начало термодинамики. Энтальпия. Закон Гесса. Дата_________ Лабораторная работа № ______ Определение стандартной энтальпии реакции нейтрализации.
- •Расчеты
- •Энтропия. Химическое равновесие. Задания для самостоятельной работы
- •Химическая кинетика. Дата_________ Лабораторная работа №________ Определение кинетических характеристик реакции окисления иодид-ионов пероксидом водорода.
- •Экспериментальные данные
- •Расчеты Вывод
- •Задания для самостоятельной работы
- •Расчеты
- •Экспериментальные данные
- •Расчеты:
- •Задания для самостоятельной работы
- •Теоретическое и экспериментальное определение рН. Дата_________ Лабораторная работа
- •Экспериментальные данные
- •Свойства буферных растворов. Дата_________ Лабораторная работа Свойства буферных растворов.
- •Экспериментальные данные
- •Расчет рН
- •Экспериментальные данные
- •Гетерогенные процессы. Дата_________ Лабораторная работа Гетерогенные равновесия в растворах электролитов
- •Расчет пс:
- •Расчет пс:
- •Дата_________ Лабораторная работа № _________ Построение изотермы адсорбции уксусной кислоты на угле.
- •Получение и устойчивость дисперсных систем. Дата_________ Лабораторная работа № ______
- •Адсорбция на подвижной и неподвижной границах раздела фаз. Получение и устойчивость дисперсных систем. Задания для самостоятельной работы
- •Ход работы:
- •Задания для самостоятельной работы
- •Дата_________ Лабораторная работа № _________
- •Задания для самостоятельной работы
- •Защита модуля 4 Механизмы реакций в органической химии
- •Биологически важные органические соединения неполимерного характера Дата_________ Лабораторная работа № _________ Свойства гетерофункциональных соединений.
- •Задания для самостоятельной работы
- •Выводы Задания для самостоятельной работы
- •Задания для самостоятельной работы
- •Строение и свойства аминокислот, пептидов и белков. Дата_________ Лабораторная работа № ________
- •Ход работы:
- •Занятие 29
- •Свойства растворов биополимеров
- •Дата_________ Лабораторная работа
- •Свойства растворов вмс. Определение изоэлектрической точки белка по степени набухания.
- •Дата_________ Лабораторная работа № _______ Строение и свойства углеводов
- •Дата_________ Лабораторная работа Нуклеиновые кислоты и их структурные компоненты
- •Дата_________ Лабораторная работа Изучение свойств липидов и их структурных компонентов
Расчеты:
Выводы:
Занятие 10 Коллигативные свойства растворов.
Задания для самостоятельной работы
1) Какую массу сахарозы надо растворить в 250 г воды, чтобы получить раствор, кипящий при 100,2оС. При какой температуре замерзает такой раствор?
2) Опишите поведение эритроцитов при 310К в растворе глюкозы с массовой долей 2%, плотность раствора 1,01 г/мл.
3) Раствор, содержащий уксусную кислоту массой 0,571 г в 100 г воды, замерзает при температуре –0,181оС. Вычислите изотонический коэффициент уксусной кислоты и осмотическое давление раствора при 298К (плотность раствора 1 г/мл).
4) К 150 мл раствора гидроксида калия с концентрацией 0,01 моль/л добавили 200 мл соляной кислоты с концентрацией 0,1 моль/л. Вычислите активность ионов водорода в полученном растворе.
Занятие 11
Теоретическое и экспериментальное определение рН. Дата_________ Лабораторная работа
Определение рН раствора фотоэлектроколориметрическим методом.
Цель работы. Научиться определять рН растворов с помощью фотоэлектроколориметрического метода.
Сущность работы. Метод основан на использовании кислотно-основных индикаторов, представляющих собой слабые кислоты или основания, изменяющие характер или интенсивность окраски в обратимых реакциях протонирования - депротонирования. У одноцветных индикаторов молекулярная форма бесцветна, а ионная - окрашена. Пример одноцветного индикатора –n-нитрофенол:
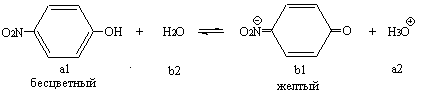
При прибавлении к водному раствору n-нитрофенола небольшого количества сильной кислоты сопряженное основание (Ind-) переходит в соответствующую бесцветную кислоту (HInd); интенсивность окраски уменьшается или она исчезает вовсе. Наоборот, прибавление небольшого количества сильного основания вызывает смещение равновесия в противоположном направлении: концентрация окрашенной формы индикатора (Ind-) возрастает, интенсивность окраски усиливается. Изменение соотношенияHIndиInd-сопровождается визуальными изменениями в определенном диапазоне значенийpH, что позволяет судить о положения равновесия и, следовательно, определятьpH:
pH= pKa+lg c(Ind-)/c(HInd),
где рКа- силовой показатель индикатора.
Сущность фотоэлектроколориметрического метода определения рН заключается в измерении оптической плотности (Ах) испытуемого раствора с индикатором и раствора, в котором добавленный индикатор полностью ионизирован и имеет максимальную интенсивность окраски, т.е. максимальную оптическую плотность (Аmax).
Ход работы.
1. На полоску универсальной индикаторной бумаги стеклянной палочкой наносят 1 каплю исследуемого раствора. Окраску индикаторной бумаги сравнивают со стандартной шкалой рН. Ориентировочное значение рН записывают в лабораторный журнал. Воспользовавшись табличными данными, выбирают одноцветный индикатор из серии Михаэлиса, зона перехода окраски которого включает ориентировочное значение рН.
2. За 15 мин до начала измерений фотоколориметр подключают к электросети, открывают крышку кюветного отделения и, нажимая кнопку “Сеть”, включают прибор, при этом загорается индикаторная лампа. Поворотом ручки “Светофильтры” устанавливают необходимый светофильтр. Ручку “Установка 100 грубо” переводят в крайнее левое положение.
3. После включения прибора готовят растворы для фотоколориметрирования. В первую пробирку с помощью пипетки отмеривают 9,0 мл исследуемого раствора, а во вторую пробирку добавляют из бюретки 9,0 мл раствора карбоната натрия. В обе пробирки добавляют точно (из бюретки) по 1,0 мл раствора выбранного индикатора. Содержимое пробирок хорошо перемешивают стеклянной палочкой.
4. Одну из кювет заполняют раствором из первой пробирки (кюветы можно брать только за те грани, через которые при работе фотоколориметра не проходит луч света), предварительно ополоснув ее этим раствором, а другую кювету- дистиллированной водой. Жидкости в кюветы наливают до метки. При необходимости внешние стенки кювет осушают фильтровальной бумагой.
5. Кювету с дистиллированной водой помещают в дальнее отделение кюветодержателя, а кювету с исследуемым раствором – в ближнее отделение. Рычаг смены кювет должен находиться в положении “1”. Крышку кюветного отделения закрывают и вращением ручек “Чувствительность”, “Установка 100 грубо” и “Установка 100 точно” устанавливают стрелку микроамперметра в положение “0” по нижней шкале “D”. Перемещают рычаг смены кювет в положение “2” и записывают полученное по нижней шкале значение оптической плотности в лабораторный журнал. Измерение повторяют.
6. После окончания измерения оптической плотности исследуемого раствора кювету с этим раствором извлекают из прибора, раствор выливают, кювету промывают дистиллированной водой, ополаскивают раствором из второй пробирки и заполняют этим же раствором. Кювету ставят в ближнее отделение и измеряют оптическую плотность щелочного раствора индикатора аналогично тому, как было описано выше.
