
- •1 Точка 1 семестр Методы объемного анализа.
- •Зависимость эквивалента вещества от реакции.
- •Понятие об эквиваленте. Объемные методы анализа. Методы расчета в объемном методе анализа.
- •Понятие об эквиваленте. Объемные методы анализа. Эквивалент простых и сложных веществ.
- •2 Точка 1 семестр Молекулярность и порядок реакций
- •Зависимость скорости реакции от концентраций реагирующих веществ.
- •Зависимость скорости реакции от температуры.
- •Гомогенный, гетерогенный и микрогетерогенный катализ.
- •Химическая термодинамика Первое начало термодинамики. Закон Гесса.
- •Химическая термодинамика. Основные термодинамические понятия.
- •Химическая термодинамика Второй закон термодинамики. Свободная энергия.
- •Принцип Ле-Шателье.
- •Костанта равновесия.
- •Химическая связь.
- •Современное представление о строении атома.
- •2 Точка 2 семестр
- •Комплексные соединения.
- •3 Точка 1 семестр Учения о растворах Теория электролитической диссоциации. Сильные и слабые электролиты.
- •Учение о растворах Коллигативные свойства растворов.
- •Учения о растворах Коллоидная химия
- •Учения о растворах. Буферные системы
- •Учения о растворах Ионное произведение воды и водородный показатель.
- •Учения о растворах Гидролиз солей.
- •Учения о растворах Способы выражения концентрации растворов.
- •3 Точка 2 семестр
Учения о растворах Гидролиз солей.
1. Задание {{ 304 }} ТЗ № 304
Среда кислая в водных растворах солей
- K2CO3
- KCl
+ CuCl2
+ Fe (NO3)3
- NaNO3
2. Задание {{ 305 }} ТЗ № 305
Кислые соли образуются при гидролизе солей
- NaCl
+ K2CO3
- AlCl3
+ Na3PO4
- KNO2
3. Задание {{ 306 }} ТЗ № 306
Щелочная среда в водных растворах солей
+ Na3PO4
+ K2СO3
+ Na2S
- NaCl
- KNO3
4. Задание {{ 307 }} ТЗ № 307
В водном растворе гидролизу подвергаются соли
- NaNO3
+ MgCl2
+ FeCl3
+ (NH4)2SO4
5. Задание {{ 308 }} ТЗ № 308
Нейтральная или близкая к нейтральной среда в водных растворах солей
+ KNO3
+ CH3COONH4
- Na2CO3
- CuCl2
6. Задание {{ 309 }} ТЗ № 309
Фенолфталеин малиновый в водных растворах солей
- KCl
+ K2CO3
+ KHCO3
- KNO3
- Cu(NO3)2
7. Задание {{ 310 }} ТЗ № 310
Основные соли образуются при гидролизе солей
- NH4NO3
+ CuCl2
- Na2CO3
+ Al(NO3)3
8. Задание {{ 311 }} ТЗ № 311
Гидролизу по катиону в водном растворе подвергаются соли
- NaCl
+ (NH4)2SO4
+ CuCl2
- K2CO3
9. Задание {{ 312 }} ТЗ № 312
Гидролизу по аниону в водном растворе подвергается соль
- AlCl3
+ Na2S
- (NH4)2S
- Al2S3
- CuCl2
10. Задание {{ 313 }} ТЗ № 313
В водном растворе и по катиону и по аниону гидролизуются соли
- NaNO3
+ CH3COONH4
+ (NH4)2CO3
- KCl
- CuCl2
11. Задание {{ 314 }} ТЗ № 314
Гидролиз хлорида алюминия можно усилить
+ повышением температуры
- увеличением концентрации соли
- подкислением раствора
+ подщелачиванием раствора
1 2.
Задание {{ 315 }} ТЗ № 315
2.
Задание {{ 315 }} ТЗ № 315
Равновесие реакции гидролиза S2- + HOH HS- + OH- можно сместить вправо, если
+ добавить кислоты
- добавить щелочи
- охладить раствор
+ нагреть раствор
+ добавить воды
13. Задание {{ 316 }} ТЗ № 316
Наиболее сильно гидролизу подвергается соль калия
- KNO3
+ K2S
- K2Se
- K2Te
- KCl
14. Задание {{ 317 }} ТЗ № 317
Концентрация гидроксидных ионов наибольшая в водном растворе соли
- NaNO3
+ Na2CO3
- CuSO4
- BaCl2
15. Задание {{ 318 }} ТЗ № 318
Подкисление раствора ослабляет гидролиз солей
+ CuSO4
- Na2CO3
- Na2S
+ NH4Cl
16. Задание {{ 319 }} ТЗ № 319
В водном растворе NaCl реакция среды
- кислая
- щелочная
+ нейтральная
17. Задание {{ 320 }} ТЗ № 320
В водном растворе Na2CO3 pH
+ >7
- <7
-
![]() 7
7
18. Задание {{ 321 }} ТЗ № 321
К щелочной среде приведет добавление к воде
- NaCl
- AlCl3
- HCl
+ K2CO3
- CO2
19. Задание {{ 322 }} ТЗ № 322
При растворении в воде слабощелочную реакцию дает
- H2S
- SO2
- CO2
+ NH3
- NaCl
20. Задание {{ 323 }} ТЗ № 323
Раствор нитрата железа (III) имеет реакцию среды
+ кислую
- щелочную
- нейтральную
21. Задание {{ 324 }} ТЗ № 324
Ослабить или прекратить гидролиз раствора хлорида аммония можно добавив немного
- KOH
- NaCl
+ HCl
- H2O
- KNO3
22. Задание {{ 325 }} ТЗ № 325
Чтобы ослабить или прекратить гидролиз раствора Na2СO3 необходимо добавить немного
+ KOH
- NaCl
- HCl
- H2O
- KNO3
23. Задание {{ 326 }} ТЗ № 326
В водном растворе (NH4)2S
+
pH![]() 7
7
- pH>7
- pH<7
24. Задание {{ 327 }} ТЗ № 327
В водном растворе CuCl2
-
pH![]() 7
7
- pH>7
+ pH<7
25. Задание {{ 328 }} ТЗ № 328
Щелочной раствор получают при растворении в воде
- SO2
- CO2
- CaCl2
+ K2SO3
- CuSO4
26. Задание {{ 329 }} ТЗ № 329
Гидролиз раствора FeCl3 усилится при добавлении
- NH4Cl
+ H2O
- HCl
- ZnCl2
- NaCl
27. Задание {{ 330 }} ТЗ № 330
Степень гидролиза можно рассчитать по формулам
+

-

-
h=![]()
+
N=
28. Задание {{ 331 }} ТЗ № 331
Лакмус синий в водном растворе
- KCl
+ K2SO3
- CuCl2
- NH4Cl
- HCl
29. Задание {{ 332 }} ТЗ № 332
Лакмус красный в водных растворах
- KCl
- K2SO3
+ CuCl2
+ NH4Cl
+ HCl
30. Задание {{ 333 }} ТЗ № 333
Лакмус фиолетовый в водном растворе
+ KCl
- K2SO3
- CuCl2
- NH4Cl
- HCl
31. Задание {{ 334 }} ТЗ № 334
Гидролиз Al2S3 протекает
- обратимо
+ необратимо
- ступенчато
32. Задание {{ 335 }} ТЗ № 335
Гидролизу не подвергаются соли
- CuSO4
+ NaCl
+ KNO3
- K2CO3
- (NH4)2S
33. Задание {{ 336 }} ТЗ № 336
Гидролиз хлорида меди усиливается при
- подкислении раствора
+ добавлении воды
+ нагревании раствора
+ подщелачивании раствора
34. Задание {{ 337 }} ТЗ № 337
Для солей образованных слабым основанием и слабой кислотой константа гидролиза рассчитывается по формуле
-
Кг =
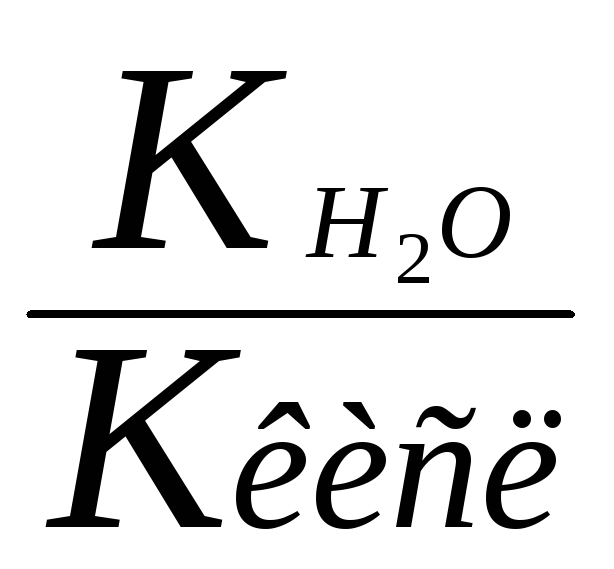
-
Кг =

+
Кг =

35. Задание {{ 338 }} ТЗ № 338
Для солей образованных слабым основанием и сильной кислотой константа гидролиза рассчитывается по формуле
-
Кг =

+
Кг =

-
Кг =
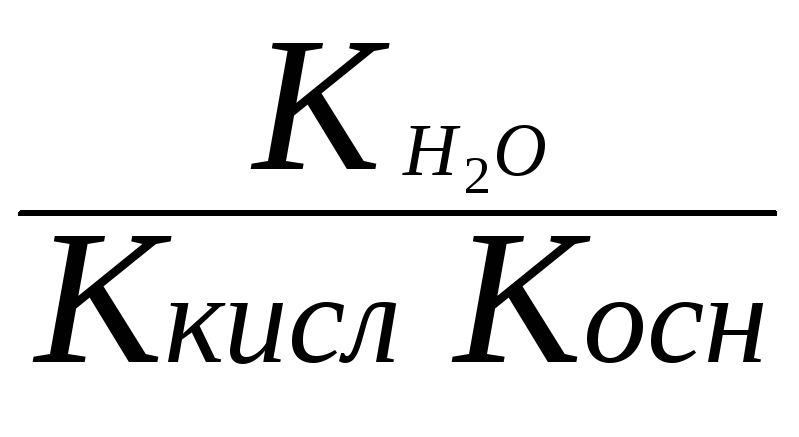
36. Задание {{ 339 }} ТЗ № 339
Для солей образованных сильным основанием и слабой кислотой константа гидролиза рассчитывается по формуле
+
Кг =

-
Кг =

-
Кг =

