
- •1 Точка 1 семестр Методы объемного анализа.
- •Зависимость эквивалента вещества от реакции.
- •Понятие об эквиваленте. Объемные методы анализа. Методы расчета в объемном методе анализа.
- •Понятие об эквиваленте. Объемные методы анализа. Эквивалент простых и сложных веществ.
- •2 Точка 1 семестр Молекулярность и порядок реакций
- •Зависимость скорости реакции от концентраций реагирующих веществ.
- •Зависимость скорости реакции от температуры.
- •Гомогенный, гетерогенный и микрогетерогенный катализ.
- •Химическая термодинамика Первое начало термодинамики. Закон Гесса.
- •Химическая термодинамика. Основные термодинамические понятия.
- •Химическая термодинамика Второй закон термодинамики. Свободная энергия.
- •Принцип Ле-Шателье.
- •Костанта равновесия.
- •Химическая связь.
- •Современное представление о строении атома.
- •2 Точка 2 семестр
- •Комплексные соединения.
- •3 Точка 1 семестр Учения о растворах Теория электролитической диссоциации. Сильные и слабые электролиты.
- •Учение о растворах Коллигативные свойства растворов.
- •Учения о растворах Коллоидная химия
- •Учения о растворах. Буферные системы
- •Учения о растворах Ионное произведение воды и водородный показатель.
- •Учения о растворах Гидролиз солей.
- •Учения о растворах Способы выражения концентрации растворов.
- •3 Точка 2 семестр
Костанта равновесия.
1. Задание {{ 515 }} ТЗ № 515
К онстанта
равновесия для реакции A+B
C+D
выражается формулой
онстанта
равновесия для реакции A+B
C+D
выражается формулой

-

-

-

2 .
Задание {{ 516 }} ТЗ № 516
.
Задание {{ 516 }} ТЗ № 516
Выражение константы равновесия для реакции N2 + O2 2NO
-
![]()

-

+
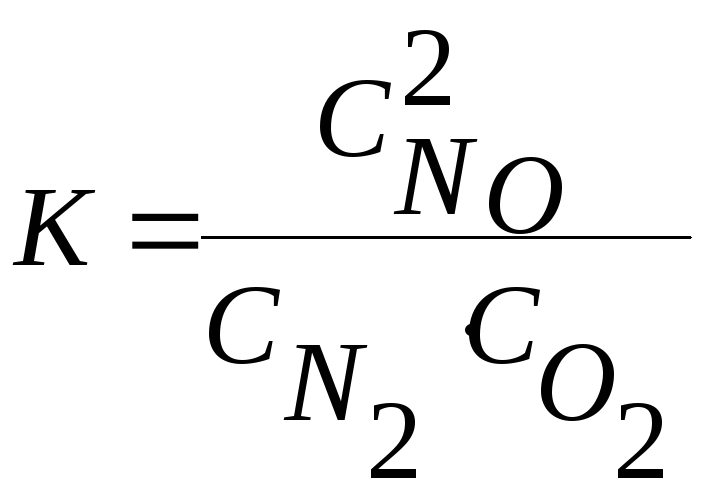
-

3. Задание {{ 517 }} ТЗ № 517
Р авновесие
реакции 2NO
+ O2
2NO2
при некоторой температуре установилось
при следующих концентрациях реагирующих
веществ: СNO=0,2,
авновесие
реакции 2NO
+ O2
2NO2
при некоторой температуре установилось
при следующих концентрациях реагирующих
веществ: СNO=0,2,
![]() =0,1
и
=0,1
и
![]() =0,1
моль/л. Константа равновесия этой
реакции равна
=0,1
моль/л. Константа равновесия этой
реакции равна
- 0,5
- 1
+ 2,5
- 5
4. Задание {{ 518 }} ТЗ № 518
Р авновесие
реакции 2NO
+ O2
2NO2
установилось при следующих концентрациях
веществ: СNO=0,2,
авновесие
реакции 2NO
+ O2
2NO2
установилось при следующих концентрациях
веществ: СNO=0,2,
![]() =0,1
и
=0,1
и
![]() =0,1
моль/л. Первоначальная концентрация
оксида азота (II)
равна
=0,1
моль/л. Первоначальная концентрация
оксида азота (II)
равна
- 0,1
- 0,2
+ 0,3
- 0,4
5. Задание {{ 519 }} ТЗ № 519
К онстанта
равновесия системы 2N2+O2
2N2O
равна 1,21. Равновесные концентрации
онстанта
равновесия системы 2N2+O2
2N2O
равна 1,21. Равновесные концентрации
![]() =0,72
и
=0,72
и
![]() =0,84
моль/л. Равновесная концентрация
=0,84
моль/л. Равновесная концентрация
![]() равна
(моль/л).
равна
(моль/л).
- 0,96
+ 1,12
- 2,24
- 3,36
6. Задание {{ 520 }} ТЗ № 520
К онстанта
равновесия реакции N2+3H2
2NH3
равна 0,1 при (400
онстанта
равновесия реакции N2+3H2
2NH3
равна 0,1 при (400![]() С).
Равновесные концентрации
С).
Равновесные концентрации
![]() =0,2
и
=0,2
и
![]() =0,08
моль/л. Равновесная концентрация азота
равна (моль/л)
=0,08
моль/л. Равновесная концентрация азота
равна (моль/л)
- 2
- 4
- 6
+ 8
7. Задание {{ 521 }} ТЗ № 521
К онстанта
равновесия термической диссоциации
N2O4
2NO2
равна 0,16. Равновесная концентрация NO2
равна 0,08 моль/л. Равновесная концентрация
N2O4
равна
онстанта
равновесия термической диссоциации
N2O4
2NO2
равна 0,16. Равновесная концентрация NO2
равна 0,08 моль/л. Равновесная концентрация
N2O4
равна
- 0,02
+ 0,04
- 0,06
- 0,08
8 .
Задание {{ 522 }} ТЗ № 522
.
Задание {{ 522 }} ТЗ № 522
Константа равновесия термической диссоциации N2O4 2NO2 равна 0,16. Равновесная концентрация NO2 равна 0,08 моль/л. Первоначальная концентрация N2O4 равна (моль/л)
- 0,02
- 0,04
- 0,06
+ 0,08
1 точка 2 семестр
Химическая связь.
1. Задание {{ 73 }} ТЗ № 73
Валентность азота в N2O5 равна
- 3
+ 4
- 5
- 2
2. Задание {{ 74 }} ТЗ № 74
Наиболее правильно отображает строение молекулы аммиака схема
-

+

-

-

3. Задание {{ 75 }} ТЗ № 75
Электронную конфигурацию благородного газа имеют частицы
+ Mg2+
+ S2-
- Fe2+
+ Ca2+
- P3+
4. Задание {{ 76 }} ТЗ № 76
Частицы Ar0, K+ и Cl- имеют одинаковые
- число протонов
- число нейтронов
+ число электронов
- массовое число
5. Задание {{ 77 }} ТЗ № 77
Наименьший радиус имеет ион
- Se2-
- Br -
- Rb+
+ Sr 2+
6. Задание {{ 78 }} ТЗ № 78
Валентные орбитали атома бора в молекуле BCl3 гибридизованы по типу
- sp3
- sp
+ sp2
- d2 sp3
7. Задание {{ 79 }} ТЗ № 79
Наибольший радиус имеет ион
- Ca2+
- K+
- F -
+ Cl -
8. Задание {{ 80 }} ТЗ № 80
Молекула хлорида бериллия имеет структуру
+ линейную
- плоскую
- тетраэдрическую
- октаэдрическую
9. Задание {{ 81 }} ТЗ № 81
Валентность азота в азотной кислоте
- 2
- 3
+ 4
- 5
10. Задание {{ 82 }} ТЗ № 82
Ковалентная связь, образованная по донорно-акценторному механизму имеется в веществе
- NaNO3
- NO
- KCl
+ NH4Cl
11. Задание {{ 83 }} ТЗ № 83
При
переходе
![]() имеет место превращение типа
имеет место превращение типа
- Испускание протона
- α - распад
+ электронный захват
- β - распад
12. Задание {{ 84 }} ТЗ № 84
Молекула метана имеет структуру
- линейную
- плоскую
+ тетраэдрическую
- октаэдрическую
13. Задание {{ 85 }} ТЗ № 85
При образовании молекулы HBr перекрываются орбитали типа
- p и p
+ s и p
- s и s
- d и p
14. Задание {{ 86 }} ТЗ № 86
π- связи имеют молекулы
+ CO
- Cl2
+ O2
+ H2SO4
15. Задание {{ 87 }} ТЗ № 87
В молекуле азота связь
+ тройная
+ ковалентная неполярная
+ очень прочная
- двойная
16. Задание {{ 88 }} ТЗ № 88
Валентность атома азота равна трем в молекулах
+ азота
+ аммиака
- азотной кислоты
+ азотистой кислоты
17. Задание {{ 89 }} ТЗ № 89
Связь образована тремя общими электронными парами в молекулах
- Cl2
- O2
+ N2
- CO
18. Задание {{ 90 }} ТЗ № 90
Валентность, равную номеру группы имеют элементы
+ углерод
- азот
+ фосфор
+ сера
- кислород
19. Задание {{ 91 }} ТЗ № 91
Высшая валентность равна четырем в атомах элементов
+ B
- P
+ N
- Cl
20. Задание {{ 92 }} ТЗ № 92
Число ковалентных полярных связей в ионе аммония равно
- 1
- 2
- 3
+ 4
22. Задание {{ 93 }} ТЗ № 93
При взаимодействии двух атомных р-орбиталей образуются связи типа
- s
+
![]()
- d
- π
23. Задание {{ 94 }} ТЗ № 94
Все
связи
![]() -
типа в молекулах
-
типа в молекулах
+ аммиака
+ этана
- азота
+ водорода
24. Задание {{ 95 }} ТЗ № 95
При взаимодействии двух атомных s-орбиталей образуется химическая связь типа
- s
+
![]()
- d
-
![]()
25. Задание {{ 99 }} ТЗ № 99
Молекулу воды правильно отображает схема
-

+

-

26. Задание {{ 100 }} ТЗ № 100
Ковалентную неполярную связь отображает формула
- NaCl
- HCl
+ Cl2
- NH3
27. Задание {{ 101 }} ТЗ № 101
В молекуле азота
-
1 π и 2![]() связи
связи
+
2
![]() и
1
и
1![]() связи
связи
-
3![]() связи
связи
-
3![]() связи
связи
28. Задание {{ 102 }} ТЗ № 102
Водородные связи образуются в жидком состоянии между молекулами
- фтора
+ фтороводорода
- водорода
+ воды
