
- •Введение в органическую химию
- •3. Изомерия органических веществ
- •4. Особенности углерод-углеродных связей
- •5. Электронные эффекты в органических молекулах
- •1.4. Номенклатура органических соединений
- •Алифатические углеводороды
- •1. Предельные углеводороды (алканы)
- •1.1. Номенклатура и изомерия алканов
- •1.2. Методы получения алканов.
- •1.3. Химические свойства алканов
- •1.4. Применение алканов
- •2. Этиленовые углеводороды (алкены)
- •2.1. Номенклатура и изомерия алкенов
- •2.2. Способы получения алкенов
- •2.3. Химические свойства алкенов
- •2.4. Применение алкенов
- •3. Диены
- •3.1. Электронное строение сопряженных диенов
- •3.2.Химические свойства сопряженных диенов
- •3.3. Применение сопряженных диенов
- •3.4. Получение диенов
- •4. Углеводороды с одной тройной связью (алкины)
- •4.1. Номенклатура и изомерия алкинов
- •4.2. Методы получения алкинов
- •4.3. Химические свойства алкинов
- •4.4. Применение ацетилена
- •Ароматические углеводороды
- •Спирты и фенолы
- •2. Изомерия и номенклатура спиртов
- •3. Методы получения спиртов:
- •7. Фенолы
- •Карбонильные соединения (альдегиды и кетоны)
- •1. Классификация карбонильных соединений
- •3. Методы получения альдегидов и кетонов
- •4. Физические свойства
- •5. Химические свойства
- •5.1. Реакции присоединения:
- •5.3. Реакции с участием атома водорода в α-положении
- •5.4. Окисление альдегидов и кетонов
- •Карбоновые кислоты
- •1. Классификация карбоновых кислот
- •2. Номенклатура и изомерия
- •4. Физические свойства
- •5. Химические свойства
- •7.1. Жиры
- •Оксикислоты. Оксокислоты
- •1. Оптическая изомерия
- •1.1. Оптически активные соединения с одним асимметрическим атомом углерода.
- •1.2. Проекционные формулы Фишера
- •1.3. Оптически активные соединения с несколькими
- •1.4. Генетические ряды
- •2. Оксикислоты
- •2.2. Физические и химические свойства
- •3.Оксокислоты
- •4. Ацетоуксусный эфир. Таутомерия
- •Углеводы
- •I. Моносахариды
- •3. Альдозы. Изомерия. Генетические ряды
- •4. Циклические формы моносахаридов. Таутомерия.
- •5. Кетозы
4. Ацетоуксусный эфир. Таутомерия
Строение ацетоуксусного эфира было предметом спора химиков в течение многих десятилетий. Одни рассматривали его как ацетоуксусный эфир(I), другие считали его эфиром 3-гидроксикротоновой кислоты (II):
O OH



 ||
O
|
O
||
O
|
O

 H3C−C−CH2−C
CH3−C
= CH−
C
H3C−C−CH2−C
CH3−C
= CH−
C
OC2H5 OC2H5
(I) (II)
Обе версии имели эспериментальное подтверждение. Так, подобно другим кетонам, ацетоуксусный эфир присоединяет циановодородную кислоту с образованием циангидрина:
H
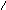
 3C−C−CH2−COOC2H5
+ HCN
H3C−C−CH2−COOC2H5
3C−C−CH2−COOC2H5
+ HCN
H3C−C−CH2−COOC2H5
||
O NC OH
Как непредельное соединение ацетоуксусный эфир присоединяет бром:
OH OH



 |
O
| O
|
O
| O


 H3C−C
= CH−C
+ Br2
CH3−C
− CH−
C
H3C−C
= CH−C
+ Br2
CH3−C
− CH−
C
OC2H5 | | OC2H5
Br Br
Кроме того, как спирт, имеющий гидроксил при атоме углерода с двойной связью (енол), ацетоуксусный эфир дает с хлоридом железа фиолетовое окрашивание.
Исследования показали, что ацетоуксусный эфир представляет собой смесь двух изомеров: кетонной (92,5 %) и енольной (7,5 %) форм. Оба изомера находятся в равновесии друг с другом. Прибавив к раствору ацетоуксусного эфира хлорид железа, заметим появление фиолетовой окраски, прибавляя затем по каплям бром, переведем енол в бромпроизводное – окраска исчезнет, однако со временем появится вновь, так как нарушенное равновесие восстановится и часть кетонной формы (I) перейдет в енольную (II).
Явление существования вещества в виде нескольких изомерных форм, легко переходящих друг в друга и находящихся в подвижном равновесии, называется таутомерией.
Чаще всего переход одной изомерной формы в другую связан с миграцией подвижного атома водорода:
| |
−C−C− −C=C− −C−N− −C=N−
|| | | || | |
O H OH O H OH
кетон енол лактам лактим
(кето-енольная таутомерия) (лактам-лактимная таутомерия)
