
- •Введение в органическую химию
- •3. Изомерия органических веществ
- •4. Особенности углерод-углеродных связей
- •5. Электронные эффекты в органических молекулах
- •1.4. Номенклатура органических соединений
- •Алифатические углеводороды
- •1. Предельные углеводороды (алканы)
- •1.1. Номенклатура и изомерия алканов
- •1.2. Методы получения алканов.
- •1.3. Химические свойства алканов
- •1.4. Применение алканов
- •2. Этиленовые углеводороды (алкены)
- •2.1. Номенклатура и изомерия алкенов
- •2.2. Способы получения алкенов
- •2.3. Химические свойства алкенов
- •2.4. Применение алкенов
- •3. Диены
- •3.1. Электронное строение сопряженных диенов
- •3.2.Химические свойства сопряженных диенов
- •3.3. Применение сопряженных диенов
- •3.4. Получение диенов
- •4. Углеводороды с одной тройной связью (алкины)
- •4.1. Номенклатура и изомерия алкинов
- •4.2. Методы получения алкинов
- •4.3. Химические свойства алкинов
- •4.4. Применение ацетилена
- •Ароматические углеводороды
- •Спирты и фенолы
- •2. Изомерия и номенклатура спиртов
- •3. Методы получения спиртов:
- •7. Фенолы
- •Карбонильные соединения (альдегиды и кетоны)
- •1. Классификация карбонильных соединений
- •3. Методы получения альдегидов и кетонов
- •4. Физические свойства
- •5. Химические свойства
- •5.1. Реакции присоединения:
- •5.3. Реакции с участием атома водорода в α-положении
- •5.4. Окисление альдегидов и кетонов
- •Карбоновые кислоты
- •1. Классификация карбоновых кислот
- •2. Номенклатура и изомерия
- •4. Физические свойства
- •5. Химические свойства
- •7.1. Жиры
- •Оксикислоты. Оксокислоты
- •1. Оптическая изомерия
- •1.1. Оптически активные соединения с одним асимметрическим атомом углерода.
- •1.2. Проекционные формулы Фишера
- •1.3. Оптически активные соединения с несколькими
- •1.4. Генетические ряды
- •2. Оксикислоты
- •2.2. Физические и химические свойства
- •3.Оксокислоты
- •4. Ацетоуксусный эфир. Таутомерия
- •Углеводы
- •I. Моносахариды
- •3. Альдозы. Изомерия. Генетические ряды
- •4. Циклические формы моносахаридов. Таутомерия.
- •5. Кетозы
5. Кетозы
Кетозы являются изомерами альдоз с тем же количеством углеродных атомов. Они имеют на один асимметрический центр меньше, чем альдозы, а следовательно, меньшее количество изомеров. Кетозы, как и альдозы, существуют в нескольких таутомерных формах:
 1CH2OH
1CH2OH


 2C
= O
2C
= O











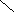


 6
O OH HO 3
*
H 6
O 1CH2OH
6
O OH HO 3
*
H 6
O 1CH2OH


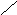
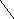


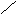

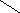
 5
HO 2
H 4
*
OH 5
HO 2
5
HO 2
H 4
*
OH 5
HO 2

 HO 4
3
1
CH2OH
H 5
*
OH HO 4
3
OH
HO 4
3
1
CH2OH
H 5
*
OH HO 4
3
OH
OH 6CH2OH OH
β-D-фруктопиранозаD-фруктоза α-D-фруктопираноза
Химические свойства моносахаридов
Моносахариды – бифункциональные соединения, поэтому их химические свойства обусловлены наличием в молекулах как карбонильных (в линейной форме), так и гидроксильных групп.
А. Реакции альдегидной группы.
1. Окисление
Альдегидная группа альдоз легко окисляется в карбоксильную даже такими слабыми окислителями, как аммиачный раствор оксида серебра или гидроксид меди(II):
NH3
H O−CH2−(CHOH)4−CH=O
+ Ag2O
HO−CH2−(CHOH)4−COOH
+ 2 Ag
O−CH2−(CHOH)4−CH=O
+ Ag2O
HO−CH2−(CHOH)4−COOH
+ 2 Ag
D-глюкоза глюконовая кислота
Глюконовая кислота относится к так называемым альдоновым кислотам. В более жестких условиях образуются сахарные кислоты:
[O]
H O−CH2−(CHOH)4−CH=O
HOOC−(CHOH)4−COOH
O−CH2−(CHOH)4−CH=O
HOOC−(CHOH)4−COOH
HNO3(к) глюкосахарная кислота
Альдоновые и сахарные кислоты из-за отсутствия карбонильной группы не способны к цикло-цепной таутомерии.
Фруктоза при окислении образует две кислоты: щавелевую и винную:
[O]
H OCH2−(CHOH)3−C−CH2OH
HOOC−COOH + HOOC−CH−CH−COOH
OCH2−(CHOH)3−C−CH2OH
HOOC−COOH + HOOC−CH−CH−COOH
|| щавелевая кислота | |
O OH OH
винная кислота
2. Восстановление
При восстановлении моносахариды превращаются в многоатомные спирты. Так, при восстановлении глюкозы образуется шестиатомный спирт – сорбит:
[H]
H O−CH2−(CHOH)4−CH=O
HO−CH2−(CHOH)4−CH2−OH
O−CH2−(CHOH)4−CH=O
HO−CH2−(CHOH)4−CH2−OH
сорбит
Б. Реакции гидроксильных групп.
1. С гидроксидом меди(II) без нагревания глюкоза реагирует как многоатомный спирт и образует раствор синего цвета.
2. Образование простых эфиров
Образование простых эфиров в первую очередь происходит по гидроксилу, связанному с С1 (гликозидный, или полуацетальный гидроксил); такие эфиры носят название гликозидов. Гликозиды – широко распространенные природные соединения.
6СН2ОН 6СН2ОН
| |

 5С
О 5С
О
5С
О 5С
О

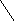

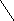 Н |
Н Н | Н
Н |
Н Н | Н
| Н | СН3ОН | Н |
 4С
1С
4С
1С
+ Н2О
4С
1С
4С
1С
+ Н2О
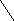

 | ОН Н
| | ОН Н |
| ОН Н
| | ОН Н |
НО | | ОН НО | | ОСН3

 3С
2С
3С
2С
3С
2С
3С
2С
| | | |
Н ОН Н ОН
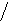 α – глюкоза
α – метилглюкозид
α – глюкоза
α – метилглюкозид
3. Образование сложных эфиров
При действии на глюкозу ангидридов кислот образуются сложные эфиры:
6СН2ОН 6СН2ОСОСН3
| |
Н
 5СН
О Н Н 5СН
О Н
5СН
О Н Н 5СН
О Н
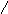


 |
| 5 СН3СООН
| |
|
| 5 СН3СООН
| |


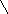
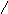 4С
ОН Н 1С
4С
ОСОСН3
Н 1С
+ 5 Н2О
4С
ОН Н 1С
4С
ОСОСН3
Н 1С
+ 5 Н2О
 | | |
| | |
| |
| | |
| | |
| |

 НО 3С
2С
ОН Н3СОСО
3С
2С
ОСОСН3
НО 3С
2С
ОН Н3СОСО
3С
2С
ОСОСН3
| | | |
Н ОН Н ОСОСН3
глюкоза пентаацетилглюкоза
Большое значение имеют сложные эфиры, образованные моносахаридами и ортофосфорной кислотой.
В. Реакции брожения
Важным свойством моносахаридов является их ферментативное брожение. Брожению подвергаются в основном гексозы. Молекулы глюкозы способны к расщеплению под действием различных микроорганизмов. Основные виды брожения:
а) спиртовое брожение
С 6Н12О6
2 С2Н5ОН
+ 2 СО2
6Н12О6
2 С2Н5ОН
+ 2 СО2
б) молочнокислое брожение
С 6Н12О6
2 СН3−СН(ОН)−СООН
6Н12О6
2 СН3−СН(ОН)−СООН
молочная кислота
в) маслянокислое брожение
С 6Н12О6
С3Н7−СООН
+ 2 СО2
+ 2 Н2
6Н12О6
С3Н7−СООН
+ 2 СО2
+ 2 Н2
масляная кислота
