
- •Введение в органическую химию
- •3. Изомерия органических веществ
- •4. Особенности углерод-углеродных связей
- •5. Электронные эффекты в органических молекулах
- •1.4. Номенклатура органических соединений
- •Алифатические углеводороды
- •1. Предельные углеводороды (алканы)
- •1.1. Номенклатура и изомерия алканов
- •1.2. Методы получения алканов.
- •1.3. Химические свойства алканов
- •1.4. Применение алканов
- •2. Этиленовые углеводороды (алкены)
- •2.1. Номенклатура и изомерия алкенов
- •2.2. Способы получения алкенов
- •2.3. Химические свойства алкенов
- •2.4. Применение алкенов
- •3. Диены
- •3.1. Электронное строение сопряженных диенов
- •3.2.Химические свойства сопряженных диенов
- •3.3. Применение сопряженных диенов
- •3.4. Получение диенов
- •4. Углеводороды с одной тройной связью (алкины)
- •4.1. Номенклатура и изомерия алкинов
- •4.2. Методы получения алкинов
- •4.3. Химические свойства алкинов
- •4.4. Применение ацетилена
- •Ароматические углеводороды
- •Спирты и фенолы
- •2. Изомерия и номенклатура спиртов
- •3. Методы получения спиртов:
- •7. Фенолы
- •Карбонильные соединения (альдегиды и кетоны)
- •1. Классификация карбонильных соединений
- •3. Методы получения альдегидов и кетонов
- •4. Физические свойства
- •5. Химические свойства
- •5.1. Реакции присоединения:
- •5.3. Реакции с участием атома водорода в α-положении
- •5.4. Окисление альдегидов и кетонов
- •Карбоновые кислоты
- •1. Классификация карбоновых кислот
- •2. Номенклатура и изомерия
- •4. Физические свойства
- •5. Химические свойства
- •7.1. Жиры
- •Оксикислоты. Оксокислоты
- •1. Оптическая изомерия
- •1.1. Оптически активные соединения с одним асимметрическим атомом углерода.
- •1.2. Проекционные формулы Фишера
- •1.3. Оптически активные соединения с несколькими
- •1.4. Генетические ряды
- •2. Оксикислоты
- •2.2. Физические и химические свойства
- •3.Оксокислоты
- •4. Ацетоуксусный эфир. Таутомерия
- •Углеводы
- •I. Моносахариды
- •3. Альдозы. Изомерия. Генетические ряды
- •4. Циклические формы моносахаридов. Таутомерия.
- •5. Кетозы
4. Циклические формы моносахаридов. Таутомерия.
Мутаротация
Альдозы проявляют далеко не все свойства, характерные для альдегидов. Так, они не дают реакции с фуксинсернистой кислотой и очень медленно реагируют с гидросульфитом натрия. В то же время наблюдается повышенная активность одной из гидроксильных групп, количество изомеров альдоз в два раза больше, чем предсказывает формула Фишера, кроме того, для альдоз характерно явление мутаротации – изменение угла вращения свежеприготовленных растворов.
Для объяснения этих противоречий в конце XIX в. была высказана мысль, что моносахариды могут существовать не только в линейной форме, но и в форме циклических внутренних полуацеталей, не содержащих карбонильной группы. В дальнейшем было доказано, что для моносахаридов характерна цикло-цепная таутомерия: в кристаллическом состоянии они имеют циклическое строение, а в растворах существуют в виде циклических и открытоцепных форм, находящихся в динамическом равновесии.
Образование циклических форм моносахаридов обусловлено взаимодействием альдегидной группы с гидроксилом, находящимся у С5, реже у С4-атома:
δ−


 δ+
O
H
δ+
O
H

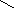
 C
C
C
C
 H
OH
(гликозидный
H
OH
(гликозидный
 δ−δ+
O
гидроксил)
δ−δ+
O
гидроксил)

 5(4)C
− O
− H
5(4)C
5(4)C
− O
− H
5(4)C
| H | H
Образовавшееся соединение – внутренний циклический полуацеталь. Поэтому циклические формы моноз называют полуацетальными.
В результате замыкания цикла в молекуле появляется новый асимметрический центр – это приводит к удвоению числа изомеров:








 HO−*C
− H CHO
H−*C−OH
HO−*C
− H CHO
H−*C−OH


 H *
OH H *
OH H *
OH
H *
OH H *
OH H *
OH








 HO *
H O HO *
H HO *
H O
HO *
H O HO *
H HO *
H O


 H *
OH H *
OH H *
OH
H *
OH H *
OH H *
OH


 H *
H *
OH H *
H *
H *
OH H *
CH2OH CH2OH CH2OH
β-D-глюкозаD-глюкоза α-D-глюкоза
Более наглядно строение циклических форм моносахаридов можно представить с помощью «перспективных» формул Хеуорса:
H
6СН2ОН | 6СН2ОН
| 1C=O |

 5С
О |
5С
О
5С
О |
5С
О

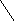
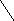
 Н |
Н H−2C−OH
Н | ОН
Н |
Н H−2C−OH
Н | ОН
|
Н | |
| Н |
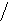
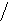
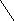



 4С
1С
HO−3C−H
4С
1С
4С
1С
HO−3C−H
4С
1С
| ОН Н | | | ОН Н |
НО | | ОН H−4C−OH НО | | Н

 3С
2С
|
3С
2С
3С
2С
|
3С
2С
| | H−5C−OH | |
Н ОН | Н ОН
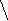 6CH2OH
6CH2OH
α –D- глюкопираноза линейная форма β – D-глюкопираноза
D−глюкозы
Группа −ОН при первом углеродном атоме в циклических формах называетя гликозидным гидроксилом. Он гораздо реакционноспособнее остальных гидроксильных групп, легко реагирует со спиртами или со второй молекулой моносахарида с образованием гликозидов.
Кристаллические формы α- и β-глюкозы вполне устойчивы, но в растворе каждая из них медленно превращается в равновесную смесь обеих форм:
Т.пл. = 146ºС Т.пл. = 149ºС
[α]D20= +113º [α]D20= +19º
 CHO
CHO


 CH2OH
H OH
CH2OH
CH2OH
H OH
CH2OH











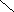


 O
HO H
O OH
O
HO H
O OH





 OH
H OH
OH
OH
H OH
OH

 HO
OH H OH HO
HO
OH H OH HO
OH CH2OH OH

 α-форма
β-форма
α-форма
β-форма
(36%) (0,024%) (64%)

равновесная смесь
[α]D20= +52º
Изменение угла вращения свежеприготовленных растворов сахаров, связанное с переходом одних таутомерных форм в другие до наступления состояния равновесия, называется мутаротацией.
