
- •Федеральное агентство по образованию
- •им. М. В. Ломоносова
- •И. А. Туторский
- •5. Адсорбция на границе раствора с газом
- •5.1. Поведение растворенных веществ на границе раствора с газом
- •5.2. Поверхностная активность
- •5.3. Поверхностно – инактивные вещества
- •5.4. Вывод адсорбционного уравнения Гиббса
- •5.5. Строение адсорбционного слоя ПАВ на границе раствора с газом
- •5.6. Уравнение состояния двумерного газа
- •5.7. Диаграммы состояния поверхностных пленок
- •5.8. Химические реакции в поверхностных пленках
- •5.9. Самоорганизованные монослои и пленки, перенесенные на твердую подложку с поверхности вода-воздух (пленки Ленгмюра –Блоджетт)
- •5.10. Двухсторонние пленки
- •5.11. Вид изотермы поверхностного натяжения. Уравнение Шишковского
- •5.12. Связь уравнений Ленгмюра и Гиббса с помощью уравнения Шишковского
- •5.13. Вывод уравнения Ленгмюра при совместном решении уравнений Гиббса и Шишковского
- •5.14. Правило Траубе
- •6. АДСОРБЦИЯ НА ГРАНИЦЕ РАЗДЕЛА ТВЕРДОЕ ТЕЛО – РАСТВОР
- •6.1. Введение
- •6.2. Правило вытеснения
- •6.3. Когезия и адгезия
- •6.4. Смачивание и растекание
- •6.5. Практическое значение смачивания
- •6.6. Правило выравнивания полярностей
- •6.7. Адсорбция полимеров из растворов на твердой поверхности
- •7. Коллоидные ПАВ
- •7.1. Введение
- •7.2. Производство и применение ПАВ
- •7.3. Биоразлагаемость и токсичность
- •Рис. 7.1. Биоразлагаемость анионных ПАВ. 1-тетрапропиленбензолсульфонат натрия, 2-линейный алкилбензолсульфонат, 3-алкилсульфат
- •7.4. Классификация и общая характеристика ПАВ
- •7.5. Свойства водных растворов ПАВ. Мицеллообразование
- •Рис. 7.3. Строение сферической мицеллы ПАВ в воде.
- •7.6. Влияние различных факторов на ККМ
- •7.6.1. Влияние длины углеводородного радикала
- •7.6.2. Влияние строения углеводородного радикала
- •7.6.3. Влияние добавок электролитов
- •7.6.4. Влияние полярных органических веществ
- •7.7. Термодинамика мицеллообразования в водной среде
- •7.8. Зависимость растворимости ПАВ в воде от температуры
- •7.9. Мицеллообразование в неводных средах
- •7.10. Оценка дифильных свойств ПАВ
- •7.11. Солюбилизация
- •7.12. Физико-химия моющего действия
- •7.13. Смеси ионных и неионных ПАВ
- •Содержание

WA 1 2 1 2 |
2 2 |
Wk (2) |
(6.7) |
т.е. работа адгезии в этом случае равна работе когезии менее полярной жидкости. Нарушение контакта жидкостей происходит по менее полярной фазе, взаимодействие в которой слабее, чем в полярной, т.е. наблюдается когезионный характер разрушения. На более полярной фазе остается адсорбированный слой менее полярной фазы.
Существует три теории адгезии: молекулярная (адсорбционная), электрическая и диффузионная. Молекулярная теория в качестве основной причины адгезии рассматривает силы Ван-дер-Ваальса. В электрической теории причиной адгезии считается контактная электризация. При контактировании фаз образуется плоский конденсатор, энергия которого определяет работу адгезии:
W a |
2 s2 h |
(6.8) |
|
|
|||
|
|
где Wa – работа адгезии, ρs – плотность поверхностного заряда, h – расстояние между обкладками, ε – диэлектрическая проницаемость.
Диффузионная теория адгезии разработана для полимерных адгезивов и в качестве причины адгезии рассматривает диффузии макромолекулы или ее сегмента в субстрат.
6.4. Смачивание и растекание
Под смачиванием понимают совокупность поверхностных явлений, происходящих на границе раздела трех контактирующих фаз, т.е. на линии трехфазного контакта. Оно зависит от взаимодействия молекул внутри каждой из фаз и между фазами и сопровождается убылью свободной энергии. При смачивании рассматриваются системы жидкость - газ - твердое тело или жидкость
40
равн |
наи отт |
(6.15) |
|
2 |
|||
|
|
Рис. 6.2. Определение равновесного угла смачивания.
При растекании жидкости с малым поверхностным натяжением по поверхности жидкости с большим поверхностным натяжением проявляется эффект Марангони, т.е. течение жидкости под действием градиента поверхностного натяжения, возникающего из-за локальных неоднородностей состава и температуры в разных участках межфазной поверхности. Жидкость течёт из области малых в область больших поверхностных натяжений вследствие самопроизвольного уменьшения поверхностной энергии Гиббса. При
ньютоновском |
течении |
напряжение |
сдвига |
P |
пропорционально |
|
градиенту поверхностного натяжения |
d / dx , |
где x |
- расстояние в |
|||
направлении |
движения |
жидкости, P d / dx . |
Для |
раствора ПАВ |
||
градиент поверхностного натяжения можно разложить на два множителя:
d d dc
dx dc dx
(6.16)
где первый множитель - поверхностная активность, а второй - градиент концентрации.
45
www.mitht.ru/e-library
неравенств, характеризующих растекание, называется коэффици-
ентом растекания по Гаркинсу:
f тг тж жг ; f WA Wk (6.13)
Установление термодинамического и механического равновесия в идеальном случае совпадает. В реальных условиях контактирования жидкостей с твердыми поверхностями термодинамическое равновесие не устанавливается по различным причинам. Среди факторов, влияющих на установление равновесия, следует отметить условия формирования поверхности контакта, порядок соприкосновения жидкости и газа с твердым телом (нанесение капли или подвод воздушного пузырька), а также шероховатость твердой поверхности, которая характеризуется коэффициентом шероховатости
K |
Sшер |
(6.14) |
|
S0 |
|||
|
|
где Sшер – величина смоченной шероховатой поверхности, а S0 – гладкой (cosΘшер = KcosΘ). Для смачивающих жидкостей cosΘ>0, cosΘшер>cosΘ.
Задержка в установлении равновесного значения называется гистерезисом смачивания. Он выражается также в различии краевых углов натекания и оттекания при перемещении жидкости по поверхности твердого тела. Значение равновесного угла смачивания
равн определяется следующим образом. К капле жидкости,
находящейся на поверхности, с помощью микрошприца добавляют жидкость в избытке и измеряют статический угол, являющийся углом натекания (рис. 6.2). Затем отбирают часть жидкости из капли и измеряют статический угол оттекания.
Значение равновесного угла получают как полусумму статических углов натекания и оттекания:
44
- жидкость - твердое тело. В последнем случае жидкости должны быть взаимно не смешивающимися. Когда конкурируют две жидкости, то смачивание является избирательным. В зависимости от соотношения интенсивности молекулярных сил, действующих между молекулами жидкости и жидкостью и твердым телом, капля жидкости образует с поверхностью твердого тела определенный равновесный угол , называемый краевым углом (рис. 6.1), который является характеристикой смачивания. Этот угол называется также контактным углом, или углом смачивания. Он образован твердой поверхностью и касательной в точке соприкосновения трех фаз и отсчитывается в сторону более плотной фазы. Установившееся равновесие является как механическим, так и термодинамическим.
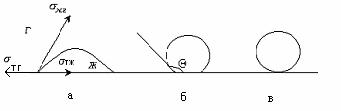
Рис. 6.1. Капля жидкости на поверхности твёрдого тела. а) – смачивание, б) -
несмачивание, в) - идеальное несмачивание.
Краевой угол всегда измеряют со стороны жидкости, а при контакте твердого тела и двух жидкостей - со стороны более полярной фазы. Если 900 , то говорят, что твердое тело смачивается жидкостью. Это имеет место для лиофильных поверхностей. При полном смачивании капля растекается на поверхности до образования мономолекулярной пленки и 00 . Если 900 , то жидкость не смачивает твердое тело, поверхность которого гидрофобна. В случае полного несмачивания капля жидкости имела бы сферическую форму,
41
www.mitht.ru/e-library
если бы не действовала сила тяжести и 1800 . Полное несмачивание реализуется лишь в условиях невесомости. В
гравитационном поле Земли максимальное значение угла достигнуто для капли ртути на поверхности тефлона и равно 1500 . В качестве примеров ниже приведены значения угла смачивания водой различных веществ: кварц - 0°; малахит - 17°; графит - 55°; тальк - 69°; парафин - 106°; тефлон - 108°.
Смачивание зависит от взаимодействия фаз, которое характеризуется величиной поверхностного натяжения между фазами. Поверхностная энергия твердого тела стремится уменьшится, что приводит к растеканию капли по поверхности. Эта энергия равна поверхностному натяжению твердого тела на границе с газом тг .
Межфазная энергия на границе твердого тела с жидкостью тж
стремится сжать каплю, т.к. уменьшение площади поверхности приводит к уменьшению поверхностной энергии. Когезионные силы, действующие внутри капли, также препятствуют растеканию. Их действие направлено по касательной к поверхности и равно жг . В
условиях равновесия, когда капля жидкости перестает растекаться, силы поверхностного натяжения уравновешивают друг друга (рис. 6.1, а). Условие равновесия выражается уравнением Юнга:
тг тж жг cos |
(6.9) |
Решив это уравнение относительно cos , получим: |
|
cos тг тж B |
(6.10) |
жг |
|
Поскольку межфазные натяжения на границе с твердым телом не всегда возможно определить экспериментально, то уравнение Юнга
42
чаще используется для решения обратной задачи смачивания, т.е. определения разности межфазных энергий по измеренным величинам краевого угла.
Необходимо отметить, что мениск объемной жидкости образует краевой угол не с сухой подложкой, а с твердой поверхностью, покрытой тонкой смачивающей пленкой.
Подставим в уравнение Дюпре уравнение Юнга:
WA тг жг тж |
тж жг cos жг тж |
(6.11) |
||||||||||||||
жг (1 cos ) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Ранее мы отмечали, что Wk |
2 жг |
|
|
|
|
|
|
|||||||||
Поделив правую часть уравнения Дюпре - Юнга на 2 жг , получим |
||||||||||||||||
отношение работ адгезии и когезии: |
|
|
|
|
|
|
||||||||||
|
|
|
|
WA |
|
1 cos |
|
|
|
|
|
(6.12) |
||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
WK |
2 |
|
|
|
|
|
|
|
|||||
Проанализируем полученное выражение. При |
00 |
cos 1, |
||||||||||||||
WA Wk , |
что соответствует |
|
полному |
смачиванию |
поверхности |
|||||||||||
твердого тела жидкостью (лиофильные поверхности). |
При 1800 |
|||||||||||||||
cos 1, WA |
0 , |
что |
соответствует |
полному |
несмачиванию |
|||||||||||
жидкостью поверхности твердого тела (лиофобные поверхности). |
|
|||||||||||||||
Условие самопроизвольного смачивания, или растекания |
||||||||||||||||
жидкости, |
которое выполняется при значении 00 |
|
и |
cos 1, |
||||||||||||
можно записать |
в |
виде |
|
неравенства: |
тг |
тж жг |
или |
|||||||||
тг тж |
жг . |
Из |
|
уравнения |
Дюпре |
следует, |
что |
|||||||||
тг тж |
WA жг . |
Следовательно |
WA жг |
жг |
или |
|||||||||||
WA 2 жг , т. е. |
WA Wk . Разность между правой и левой частями |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
43 |
www.mitht.ru/e-library
