
- •Федеральное агентство по образованию
- •им. М. В. Ломоносова
- •И. А. Туторский
- •5. Адсорбция на границе раствора с газом
- •5.1. Поведение растворенных веществ на границе раствора с газом
- •5.2. Поверхностная активность
- •5.3. Поверхностно – инактивные вещества
- •5.4. Вывод адсорбционного уравнения Гиббса
- •5.5. Строение адсорбционного слоя ПАВ на границе раствора с газом
- •5.6. Уравнение состояния двумерного газа
- •5.7. Диаграммы состояния поверхностных пленок
- •5.8. Химические реакции в поверхностных пленках
- •5.9. Самоорганизованные монослои и пленки, перенесенные на твердую подложку с поверхности вода-воздух (пленки Ленгмюра –Блоджетт)
- •5.10. Двухсторонние пленки
- •5.11. Вид изотермы поверхностного натяжения. Уравнение Шишковского
- •5.12. Связь уравнений Ленгмюра и Гиббса с помощью уравнения Шишковского
- •5.13. Вывод уравнения Ленгмюра при совместном решении уравнений Гиббса и Шишковского
- •5.14. Правило Траубе
- •6. АДСОРБЦИЯ НА ГРАНИЦЕ РАЗДЕЛА ТВЕРДОЕ ТЕЛО – РАСТВОР
- •6.1. Введение
- •6.2. Правило вытеснения
- •6.3. Когезия и адгезия
- •6.4. Смачивание и растекание
- •6.5. Практическое значение смачивания
- •6.6. Правило выравнивания полярностей
- •6.7. Адсорбция полимеров из растворов на твердой поверхности
- •7. Коллоидные ПАВ
- •7.1. Введение
- •7.2. Производство и применение ПАВ
- •7.3. Биоразлагаемость и токсичность
- •Рис. 7.1. Биоразлагаемость анионных ПАВ. 1-тетрапропиленбензолсульфонат натрия, 2-линейный алкилбензолсульфонат, 3-алкилсульфат
- •7.4. Классификация и общая характеристика ПАВ
- •7.5. Свойства водных растворов ПАВ. Мицеллообразование
- •Рис. 7.3. Строение сферической мицеллы ПАВ в воде.
- •7.6. Влияние различных факторов на ККМ
- •7.6.1. Влияние длины углеводородного радикала
- •7.6.2. Влияние строения углеводородного радикала
- •7.6.3. Влияние добавок электролитов
- •7.6.4. Влияние полярных органических веществ
- •7.7. Термодинамика мицеллообразования в водной среде
- •7.8. Зависимость растворимости ПАВ в воде от температуры
- •7.9. Мицеллообразование в неводных средах
- •7.10. Оценка дифильных свойств ПАВ
- •7.11. Солюбилизация
- •7.12. Физико-химия моющего действия
- •7.13. Смеси ионных и неионных ПАВ
- •Содержание
7.7. Термодинамика мицеллообразования в водной среде
Причиной мицеллообразования в водной среде являются гидрофобные взаимодействия, т. е. стремление воды к ликвидации внутренних полостей и выталкиванию гидрофобных тел. Этот эффект обусловлен межмолекулярными взаимодействиями и структурой воды, существованием в воде системы водородных связей.
Экспериментально показано, что в водных растворах величина энтальпии мицеллообразования мала и может быть отрицательной. Следовательно, определяющее значение в мицеллообразовании имеют энтропийные изменения. Но следует учесть, что при объединении молекул ПАВ в мицеллу энтропия уменьшается, т. к. число степеней свободы ПАВ уменьшается. Для того чтобы понять причину положительного энтропийного эффекта при мицеллообразовании, необходимо рассмотреть изменение энтропии всей системы, обоих ее компонентов, ПАВ и воды. Движущей силой мицеллообразования является увеличение энтропии системы в целом за счет разрушения упорядоченного расположения молекул воды, связанных водородными связями. Упорядоченные “льдоподобные” структуры существуют вокруг углеводородных радикалов, когда молекулы ПАВ находятся в молекулярно - растворенном состоянии.
Углеводородные радикалы молекул ПАВ оказывают упорядочивающее воздействие на ближайшую к ним область водной среды (вследствие образования Н-связей). Поэтому концентрация Н- связей в 1 моле воды выше вблизи углеводородных цепей. Когда молекулы ПАВ образуют мицеллу, водородные связи в воде разрушаются, молекулы воды приобретают больше степеней свободы, и энтропия воды, а, следовательно, всей системы увеличивается.
68
5.7. Диаграммы состояния поверхностных пленок
Фазовое состояние поверхностных пленок описывается
диаграммой состояния или изотермой сжатия, которая может быть построена в координатах sм .
Поверхностное давление измеряют непосредственно с помощью весов Ленгмюра. Этот метод основан на прямом измерении горизонтальной силы, которая действует на поплавок, отделяющий пленку от поверхности чистого растворителя. Современные весы позволяют определять поверхностные давления с точностью до сотых долей дины\см. В общем случае при уменьшении площади реализуются газообразное, жидкое и твердое состояние монослоя. Каждое состояние монослоя характеризуется определенной ориентацией молекул, зависящей от sм , адгезионных и когезионных свойств систем. В диапазоне давления и площади, занимаемой 1 молем ПАВ, отвечающем всем трем агрегатным состояниям пленки, диаграмма состояния имеет вид, показанный на рисунке 5.7 .
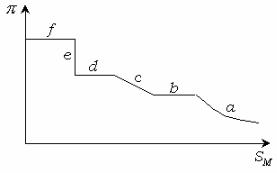
Рис. 5.7. Диаграмма состояния поверхностных пленок.
Участок a соответствует двумерному газу и аналогичен кривой сжатия газа. На участке b происходит конденсация. В этом состоянии
17
www.mitht.ru/e-library
пленка называется растянутой жидкой пленкой и способна к сжатию,
которому соответствует участок c . На участке d происходит фазовый переход, участку e соответствует конденсированная (твердая)
пленка. Участку f соответствует разрушение мономолекулярной
пленки, т. е. образование капли для жидкой пленки или многослойных образований для твердой пленки. Поверхностные пленки реальных ПАВ описываются диаграммами состояния, отвечающими определенному участку общей диаграммы состояния. Это зависит от длины углеводородного радикала молекулы ПАВ. Так, лауриновая
кислота благодаря сравнительно короткому радикалу
образует только газообразные пленки (кривая 1, рис. 5.8).
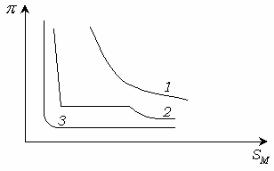
Рис. 4.8. Диаграммы состояния поверхностных пленок лауриновой (1), миристиновой (2) и пальмитиновой (3) кислот.
Миристиновая кислота C13 H 27 COOH образует как газообразные,
так и конденсированные пленки (кривая 2, рис. 5.8). Пальмитиновая
кислота C15 H31COOH при обычной температуре образует только конденсированные пленки вследствие большой длины углеводородного радикала (кривая 3, рис. 5.8).
18
Благодаря экранирующему действию недиссоциированных полярных групп спирта уменьшаются силы электрического отталкивания между одноимённо заряженными полярными группами ПАВ, что способствует мицеллообразованию и снижению ККМ. Низкомолекулярные добавки (метанол, ацетон и др.) понижают ККМ за счёт их хорошей растворимости.
Существует два подхода к мицеллообразованию: квазихимический и фазовый. При квазихимическом подходе к мицеллообразованию мицелла рассматривается как большая молекула, состоящая из многих малых молекул ПАВ. Мицеллообразование можно рассматривать как быструю квазихимическую реакцию, протекающую по схеме:
ni Ai M
где ni - число агрегации, Ai - молекула ПАВ, M - мицелла.
Равновесный мицелярный раствор характеризуется узким распределением мицелл по размеру, форме и составу, т. е. их монодисперсностью. Эта реакция протекает настолько быстро, что время жизни молекулы ПАВ в мицелле составляет 10 7 с.
При фазовом подходе к мицеллообразованию мицелла рассматривается как микрофаза. Но эта микрофаза не имеет макроскопического аналога т. к. при равновесии мицеллярного раствора с твердой фазой мицелла не является зародышем. Мицеллы существуют в нерасторжимом единстве с окружающей жидкой средой и не могут быть из неё выделены.
67
www.mitht.ru/e-library
