
- •Теоретические основы химии
- •Основные понятия и законы химии Атомно - молекулярное учение.
- •Закон сохранения массы веществ
- •Составление химических уравнений
- •Расчеты по химическим уравнениям
- •Закон постоянства состава
- •Закон кратных отношений
- •Закон объемных отношений
- •Закон Авогадро и молярный объем газа
- •Следствия.
- •Закон эквивалентов
- •Основные классы неорганических
- •2. Разложение некоторых кислородсодержащих веществ (оснований, кислот, солей) при нагревании:
- •Основания
- •Получение оснований
- •Химические свойства оснований
- •Кислоты
- •Классификация кислот
- •Химические свойства кислот
- •Получение кислот
- •Средние соли
- •Химические свойства солей
- •Кислые соли
- •Графическое изображение формул
- •Энергетика химических реакций
- •Химическое равновесие. Константа химического равновесия
- •Энтропия
- •Энергия Гиббса направленность химических процессов
- •Примеры термодинамических расчетов
- •Полученные значения h и s характеризуют процесс испарения SnBr2. Процесс эндотермический, испарение требует нагревания. При испарении энтропия увеличивается.
- •Химическая кинетика. Скорость химической реакции
- •Молекулярность элементарных реакций
- •Уравнение Аррениуса
- •Катализ
- •Смещение химического равновесия
- •3 Влияние температуры на положение равновесия
- •Фазовые равновесия
- •Основные характеристики растворов
- •Растворимость газов в газах
- •Растворимость газов в жидкостях
- •Взаимная растворимость жидкостей
- •Растворимость твердых веществ в жидкостях
- •Растворы неэлектролитов
- •1. Давление насыщенного пара разбавленных растворов
- •2. Давление пара идеальных и реальных растворов
- •3. Температура кристаллизации разбавленных растворов
- •4. Температура кипения разбавленных растворов
- •5. Осмотическое давление разбавленных растворов
- •6. Понятие активности растворенного вещества
- •Слабые электролиты. Константа диссоциации
- •Сильные электролиты
- •PН растворов
- •Произведение растворимости
- •Гидролиз солей
- •Количественные характеристики процесса гидролиза соли.
- •Комплексные соединения
- •Направленность реакций в растворах электролитов
- •Протонная теория Брёнстеда-Лоури
- •В случае взаимодействия нейтральных молекулпродукт реакции (например bf3∙nh3) часто называют аддуктом.
- •Теория сольвосистем
- •Металлы, как типичные восстановители, окисляются до соединений, содержащих атомы металлов в более высоких степенях окисления, в зависимости от природы металла и характера среды:
- •Электродные потенциалы
- •Гальванические элементы
- •Электролиз
- •Законы электролиза
- •Примеры электролиза Расплавы
- •Растворы
- •Хими́ческие исто́чники то́ка
- •Коррозия металлов и методы защиты металлов от коррозии
- •Электрохимическая коррозия
- •Защита металлов от коррозии
- •Строение атома
- •Волновое уравнение. Квантовомеханическое объяснение строения атома
- •Электронная структура атомов и периодическая система элементов
- •Структура периодической системы элементов д.И. Менделеева.
- •Периодичность свойств химических элементов и их соединений
- •Ковалентная связь. Метод валентных связей
- •Способы образования ковалентной связи
- •Гибридизация атомных орбиталей
- •Метод молекулярных орбиталей
- •Ионная связь
- •Водородная связь
- •Квантовомеханические теории строения комплексных соединений
- •1. Теория валентных связей
- •2. Гибридизация орбиталей и структура комплексов
- •3. Теория кристаллического поля.
- •4. Цветность комплексных соединений
Основные характеристики растворов
Существование абсолютно чистых веществ невозможно – всякое вещество обязательно содержит примеси, или, иными словами, всякая гомогенная система многокомпонентна. Если имеющиеся в веществе примеси в пределах точности описания системы не оказывают влияния на изучаемые свойства, можно считать систему однокомпонентной; в противном случае гомогенную систему считают раствором.
Раствор – гомогенная система, состоящая из двух или более компонентов, состав которой может непрерывно изменяться в некоторых пределах без скачкообразного изменения её свойств.
Раствор может иметь любое агрегатное состояние; соответственно их разделяют на твердые, жидкие и газообразные (последние обычно называют газовыми смесями). Обычно компоненты раствора разделяют на растворитель и растворенное вещество. Как правило, растворителем считают компонент, присутствующий в растворе в преобладающем количестве либо компонент, кристаллизующийся первым при охлаждении раствора; если одним из компонентов раствора является жидкое в чистом виде вещество, а остальными – твердые вещества либо газы, то растворителем считают жидкость. С термодинамической точки зрения это деление компонентов раствора не имеет смысла и носит поэтому условный характер. Как правило, процессы растворения сопровождаются изменением объема и температуры. Например, при смешении равных объемов этилового спиртаиводыобъем смеси меньше суммы объемов компонентов (это явление называется контракцией).
Одной из важнейших характеристик раствора является его состав, описываемый с помощью понятия концентрация раствора. Ниже дается определение наиболее распространенных способов выражения концентрации и формулы для пересчета одних концентраций в другие: Если для разрушения структуры вещества необходимо больше теплоты, чем ее образуется при гидратации, то растворение - эндотермический процесс. Это происходит, например, при растворении в воде NаNОз, KCl, K2S04, NH4Cl и др.
При работе с растворами необходимо знать их количественный состав. Количественный состав растворов выражается различными способами:
1. Массовая доля ω–число граммов растворенного вещества в 100 граммах раствора.Например, форма записи «раствор NaCl с массовой долейω(NaCl) = 25%» означает, что 25 г NaClсодержится в 100 г раствора. Масса воды в нем равна 75 г
Массовая доля растворенного вещества ω(Х) - безразмерная величина, равная отношению массы вещества m(Х) к массе раствора m(р-ра):
ω(Х)
=
 (1)
(1)
m(р-ра) = m(Х) + m(растворителя).
Массовую долю выражают в долях единицы или в процентах.
.
2. Молярная концентрацияС(X)– число молейnрастворенного вещества в одном литре раствора. Молярная концентрация равна отношению химического количества растворенного вещества (п(Х), моль) к объему раствора (V, л):
С(Х)
=
 (2)
(2)
Химическое количество вещества выражается соотношением
n(Х)
=
 (3)
(3)
где m(Х) - масса вещества Х, г; М(Х) - молярная масса вещества Х, г/моль.
Подставляя формулу (3) в (2), получаем
С(Х)=
 (4)
(4)
(5)
Если известна масса т и плотность ρ раствора, то его объем V
V= ρ m(р-ра) (5)
Молярная концентрация выражается в моль/л или вмоль/дм3 (эта размерность часто обозначается М). Например: 2 М NaOH или C(NaOH) = 2 моль/л. Данная форма записи означает, что 2 моля NaOH содержится в 1 л раствора.
3.
Молярная
концентрация эквивалента (нормальная
концентрация)
С( X)
– число молей эквивалентов растворенного
вещества nэкв.
в
одном литре раствора.
X)
– число молей эквивалентов растворенного
вещества nэкв.
в
одном литре раствора.
Молярная
концентрация эквивалента равна отношению
химического количества вещества
эквивалента n( X)
или (nэквX)
к объёму раствора V(л):
X)
или (nэквX)
к объёму раствора V(л):
С( Х)=
Х)= (4)
(4)
Молярная
концентрация эквивалента
выражается
в моль/л или моль/дм3
(часто обозначается н.).
Например: 2 н. Na2SO4
или С( Na2SO4)
=
2
моль/л. Данная форма записи означает,
что 2 моль эквивалента
Na2SO4
содержится в 1 л раствора.
Na2SO4)
=
2
моль/л. Данная форма записи означает,
что 2 моль эквивалента
Na2SO4
содержится в 1 л раствора.
Если взаимодействуют растворы веществ с известными нормальными концентрациями, то в точке эквивалентности справедливы соотношения:
n( (Х))
=n(
(Х))
=n( (Y));
(Y));
С( (Х))V(X)
= С(
(Х))V(X)
= С( (Y))V(Y).
(Y))V(Y).
4..Моляльная концентрация b – число молей растворенного вещества в одном килограмме растворителя.
b
(X) =
 =
=
где n(X) – число молей вещества X; m – масса вещества Х; М – молярная масса вещества Х; m(р-ля) –массарастворителя , кг. Измеряют моляльность в моль/кг.
Мольная доля χ–это отношение количества компонента, содержащегося в данной системе ( в молях), к общему количеству веществ в системе ( в молях). Выражают в долях единицы или процентах
(Х)
=
 ,
,
где
n(Х) количество вещества
Х в растворе, моль;ni– количество вещества каждого компонента
раствора, моль. Для двухкомпонентного
раствора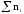 =n(Х) +n(S),
гдеn(S) –
количество вещества растворителяS.
Мольная доля также выражается в долях
единицы или процентах. Сумма массовых
(мольных) долей всех компонентов раствора
равна 1.
=n(Х) +n(S),
гдеn(S) –
количество вещества растворителяS.
Мольная доля также выражается в долях
единицы или процентах. Сумма массовых
(мольных) долей всех компонентов раствора
равна 1.
6 Очень часто в аналитической химии используют такой способ выражения концентраций раствора как титр: определяется числом граммов растворённого вещества в 1 мл раствора. Титрованные, или стандартные растворы – это растворы с точно известным содержанием вещества. Без таких растворов невозможно представить проведение химического анализа.
Пример 1.Найти молярную концентрацию раствора с массовой долей 15%H2SO4и плотностью1,10 г/мл.
Решение.
Пусть Vр-ра = 1 л = 1000 мл.
Найдем массу 1 л раствора:
m р-ра = р-ра Vр-ра = 1,10 г/мл 1000 мл = 1100 г.
Найдем массу H2SO4 в 1 л раствора:
m(H2SO4) = m р-ра = 0,15 1100 = 165 г.
Найдем молярную концентрацию:
С
H SO
SO =
=
 =
= = 1,68 моль/л.
= 1,68 моль/л.
Пример 2. Сколько миллилитров 30%-ного раствора HCl (плотность 1,150 г/мл) нужно для приготовления 1 л 0,1 н. раствора HCl?
Решение.
Найдем массу соляной кислоты, которая должна содержаться в приготовленном растворе:
m(HCl)
= C( HCl)
M(
HCl)
M( HCl)
Vр-ра,
HCl)
Vр-ра,
где
M( HCl)
= 1
M(HCl)
= 36,5 г/моль.
HCl)
= 1
M(HCl)
= 36,5 г/моль.
m(HCl) = 0,1 36,5 1 = 3,65 г.
Поскольку раствор готовят разбавлением водой 30%-го раствора, то такая же масса HCl должна содержаться в 30%-м растворе. Найдем массу 30%-го раствора, содержащую 3,65 г HCl:
(HCl)
=

mр-ра
=
mр-ра
=
 =
= = 12,167 г.
= 12,167 г.
Найдем объем 30%-го раствора:
V
=
 =
= = 10,58
мл.
= 10,58
мл.
Пример 3. Сколько граммов Na2SO4 10H2O надо растворить в 800 г воды, чтобы получить раствор с массовой долей Na2SO4 10%?
Решение.
Обозначим массу кристаллогидрата за х:
m(Na2SO4 H2O) = х(г), тогда
(Na2SO4)
=
 =
= = 0,1.
= 0,1.
Выразим
массу Na2SO4,
содержащуюся в х
г кристаллогидрата, используя молярные
массы М(Na2SO4)
= 142 г/моль МNa SO
SO
H
H O
= = 142 + 180 = 322 г/моль.
O
= = 142 + 180 = 322 г/моль.
322 г Na2SO4 H2O содержат 142 г Na2SO4,
х
г Na2SO4
H2O
содержат m
г Na2SO4
m(Na2SO4)
=
 .
.
Подставим m(Na2SO4) в выражение для и найдем х:
(Na2SO4)
=
 = 0,1;
= 0,1;
142 х = 0,1 322 (800 + х) = 25 760 + 32,2х;
109,8х = 25 760, х = 234,6.
m(Na2SO4 H2O) = 234,6 г.
Пример 4. Сколько граммов СаСО3 выпадет в осадок, если к 800 мл 0,5 н. раствора СаСl2 прибавить избыток раствора соды?
Решение. При сливании растворов СаСl2и соды (Nа2СО3) протекает реакция обмена: СаСl2+Nа2СО3= СаСО3+ 2NaCl.
Для решения задачи будем использовать закон эквивалентов: при взаимодействии количества веществ эквивалентов разных веществ одинаковы, т.е.
n( СаСО3)
= C(
СаСО3)
= C( СаСl2)
Vр-ра
= 0,5
0,8 = 0,4 моль.
СаСl2)
Vр-ра
= 0,5
0,8 = 0,4 моль.
Найдем
массу СаСО3,
М СаСО3
=
СаСО3
=

100 г/моль:
100 г/моль:
m(СаСО3)
= n( СаСО3)
М
СаСО3)
М СаСО3
= 0,4
СаСО3
= 0,4

100 = 20 г.
100 = 20 г.
V
=
 =
= = 10,58 мл.
= 10,58 мл.
Концентрация компонента в растворе может изменяться от нуля до некоторого максимального значения, называемого растворимостью компонента. Растворимость S – концентрация компонента в насыщенном растворе. Насыщенный раствор – раствор, находящийся в равновесии с растворенным веществом. Величина растворимости характеризует равновесие между двумя фазами, поэтому на неё влияют все факторы, смещающие это равновесие (в соответствии с принципом Ле Шателье ).
Образование раствора является сложным физико-химическим процессом. Процесс растворения всегда сопровождается увеличением энтропии системы; при образовании растворов часто имеет место выделение либо поглощение теплоты. Количество тепла, поглощаемого или выделяемого при растворении 1 молявещества, называетсятеплотой растворения(∆Hs). При растворении твердого вещества происходит разрушениекристаллической решетки. На это требуется затрата энергии. Однако многие процессы растворения протекают с выделением тепла, т.е. эти процессы являются экзотермическими. (∆Hs<0). Поэтому можно предположить, что наряду с разрушением кристаллической решетки протекает экзотермический процесс. Было показано, что этим процессом являетсясольватация, т.е. соединение молекул растворенного вещества в неустойчивые соединения –сольваты. Когда растворителем является вода, то эти соединения называются гидратами, а процесс –гидратацией. Поскольку молекула воды оченьполярна, то многие гидраты весьма устойчивы и могут быть выделены в кристаллическом состоянии (кристаллогидраты), например CuSO4∙5H2O – медный купорос, Na2CO3∙10H2O – кристаллическая содаи др.
В общем случае при растворении происходит изменение свойств и растворителя, и растворенного вещества, что обусловлено взаимодействием частиц между собой по различным типам взаимодействия: Ван-дер-Ваальсового (во всех случаях), ион-дипольного (в растворах электролитов в полярных растворителях), специфических взаимодействий (образование водородных или донорно-акцепторных связей). Учет всех этих взаимодействий представляет собой очень сложную задачу. Очевидно, что чем больше концентрация раствора, тем интенсивнее взаимодействие частиц, тем сложнее структура раствора. Поэтому количественная теория разработана только для идеальных растворов, единственной движущей силой образования такого раствора является увеличение энтропии системы ΔS; какие-либо тепловые или объемные эффекты при растворении отсутствуют (ΔН = 0, ΔV = 0. К идеальным можно отнести газовые растворы и растворы неполярных жидкостей, в которых энергия взаимодействия разнородных частиц EA-B близка к энергиям взаимодействия одинаковых частиц EA-A и EB-B. Идеальными можно считать также бесконечно разбавленные растворы, в которых можно пренебречь взаимодействием частиц растворителя и растворенного вещества между собой. Свойства таких растворов зависят только от концентрации растворенного вещества, но не зависят от его природы.
