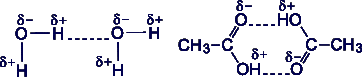- •А.Л.Галкин, в.К.Османов химия
- •Isbn 978-5-502-00158-8 © нгту им. Р.Е. Алексеева, 2013
- •Введение
- •Классификация неорганических веществ
- •Аллотропия
- •1.4 Соли
- •Комплексные соли
- •Генетическая связь между различными классами соединений
- •Основание Кислота Примеры
- •Основные понятия и законы химии
- •Закон сохранения массы
- •Закон постоянства состава
- •Закон эквивалентов
- •Закон авогадро
- •Уравнение состояния идеального газа
- •3. Строение атома
- •3.1. Квантовые числа
- •3.2. Принципы заполнения атомных орбиталей
- •3.3. Полная электронная формула атома
- •3.4. Периодический закон элементов д. И. Менделеева
- •Физический смысл химической периодичности
- •4. Химическая связь и строение молекул
- •4.1. Физические основы образования молекул
- •4.2. Метод валентных связей (метод вс)
- •Значения длины и энергии связи у галогеноводородных кислот
- •Взаимосвязь кратности, длины и энергии связи с - с, с - о и n - n
- •Одна s-орбиталь и одна p-орбиталь превращаются в две одинаковые «гибридные» орбитали, угол между осями которых равен 180°:
- •4.3. Метод молекулярных орбиталей
- •Энергия, длина и порядок связи в молекулах элементов I периода
- •4.4. Металлическая связь
- •4.5. Межмолекулярные взаимодействия
- •5. Энергетика и направление химических процесов
- •5.1. Термодинамическая система и ее состояния
- •5.2. Изменение свойств термодинамической системы
- •5.3. Энергия, работа, теплота
- •5.4. Обратимые и необратимые процессы
- •5.5. Первый закон термодинамики
- •5.6. Направление химических реакций
- •Второй закон термодинамики
- •Постулат планка (третий закон термодинамики)
- •6. Скорость химических реакций и и химическое равновесие
- •6.1. Влияние концентрации реагентов на скорость реакции
- •6.2. Влияние температуры на скорость реакции
- •6.3. Влияние катализатора на скорость реакции
- •А) без катализатора и б) в присутствии катализатора
- •6.4. Скорость гетерогенных химических реакций
- •6.5. Химическое равновесие
- •6.5.1. Влияние внешних факторов на состояние равновесия
- •7. Растворы
- •7.1. Вода
- •Вода в природе
- •7.2. Образование растворов
- •7.3. Способы выражения концентраций растворов
- •7.4. Растворы электролитов
- •7.4.2. Равновесные процессы в растворах электролитов
- •Цвета кислотно-основных индикаторов в зависимости от рН раствора
- •8. Окислительно – восстановительные реакции
- •8.1. Степень окисления
- •8.2. Типичные окислители и восстановители
- •8.3. Классификация окислительно-восстановительных реакций
- •8.4. Составление уравнений окислительно-восстановительных реакций
- •9. Основы электрохимических процессов
- •9.1. Измерение стандартных электродных потенциалов
- •9.2. Направление окислительно-восстановительных реакций
- •9.3. Влияние внешних факторов на величину электродного потенциала
- •9.4. Законы фарадея
- •9.5. Элементы технической электрохимии
- •10. Коррозионные процессы
- •10.1. Электрохимическая коррозия
- •10.2. Кинетика коррозионных процессов
- •10.3.Методы защиты металлов от коррозии
- •11. Номенклатура и классификация органических соединений
- •11.1. Номенклатура органических соединений
- •11. 2. Классификация органических соединений по номенклатуре июпак
- •12. Высокомолекулярные соединения
- •12.1. Классификация высокомолекулярных соединений
- •12.1.1. Классификация высокомолекулярных соединений по структуре макромолекул
- •12.1.2. Классификация полимеров по поведению при нагревании
- •12.2. Сополимеры
- •12.3. Синтез высокомолекулярных соединений
- •12.4. Свойства полимеров
- •12.5. Важнейшие полимерные материалы
- •Примеры решения задач
- •1.Основные понятия и законы химии
- •Строение атома
- •Химическая связь и строение молекул
- •Задача 4.
- •Молекула bf3 . Электронная формула атома бора 5b - 2s22p1. При образовании трех -связей атом бора переходит в возбужденное состояние
- •Решение. Последовательность действий для предсказания геометрии молекул на основании теории локализованных электронных пар следующая:
- •1.Подсчитывают число валентных электронов молекулы или иона и записывают электронную валентную структуру (льюисову структуру);
- •2.По валентной структуре определяют число -связывающих и несвязывающих электронных пар, т.Е. Тип молекулы aBnEm (n – число - связей, m – число несвязывающих электронных пар);
- •Энергетика и направление химических процессов
- •4 Моль н2 – - 150,8 кДж
- •Скорость химических реакций и химическое равновесие Задача 1
- •Растворы Примеры решения задач
- •Окислительно-восстановительные реакции примеры решения типовых задач
- •Основы электрохимических процессов
- •Коррозионные процессы
- •Галкин Андрей Львович Османов Владимир Кимович
- •603950, Нижний Новгород, ул.Минина, 24.
4.5. Межмолекулярные взаимодействия
Водородная связь
Водородная связь – это связь между положительно заряженным атомом водорода одной молекулы и отрицательно заряженным атомом другой молекулы или между положительно заряженным атомом водорода одной молекулы и отрицательно заряженным атомом той же молекулы (внутримолекулярная водородная связь).
Водородная связь возникает между электроотрицательным элементом (F, O, N, S, Cl) и атомом водорода.
Водородная связь имеет частично электростатический и частично донорно-акцепторный механизм возникновения.
|
а)б)
|
Рис. 4.10. Примеры водородных связей в Н2О (а) и уксусной кислоте (б)
41
Наличием водородных связей обусловлены уникальные свойства многих веществ, в том числе и воды. Трехатомная молекула Н2О образует четыре
водородные связи. В их образовании принимают участие оба атома водорода и атом кислорода, имеющий две неподеленные электронные пары, которые образуют две водородные связи с атомами водорода соседних молекул воды.
Водородные связи являются причиной и другого уникального свойства воды – плотность льда меньше плотности воды. В структуре льда каждый атом кислорода связан через атомы водорода с четырьмя другими атомами кислорода – из других молекул воды. В результате образуется очень рыхлая «ажурная» структура. Вот почему лед такой легкий.
При плавлении льда (0оС) около 10% водородных связей разрушается, и молекулы воды немного сближаются. Поэтому плотность жидкой воды при температуре плавления выше, чем плотность льда. Дальнейшее нагревание за счет увеличения амплитуды колебания молекул вызывает увеличение объема воды. Это происходит со всеми веществами.
Наличие водородных связей влияет и на кислотные свойства многих веществ. Так фтороводородная кислота, в отличие от других галогеноводородных кислот, является слабой, так как атомы водорода связаны сразу с двумя атомами фтора, что и препятствует отщеплению протона. Благодаря особо прочным водородным связям фтороводородная кислота – единственная одноосновная кислота, способная образовывать кислые соли, например, NaHF2.
В газовой фазе HF существует в виде димера.
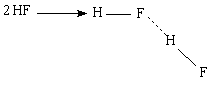
Наличие водородных связей объясняет высокие температуры кипения воды, спиртов и карбоновых кислот. Водородная связь увеличивает вязкость растворов, температуры кипения и плавления веществ. Энергия водородной связи находится в диапазоне 8-40 кДж/моль, что меньше энергии обычной ковалентной связи (150-400 кДж/моль).
Межмолекулярное взаимодействие – взаимодействие молекул между собой, не приводящее к разрыву или образованию новых химических связей. На расстояниях ~10-9 м между соседними молекулами возникают заметные силы притяжения, называемые Ван-дер-Ваальсовыми силами. Эти силы имеют электрическую природу и включают в себя три составляющие (ориентационную, индукционную и дисперсионную), которые определяют отличие реальных газов от идеальных, существование жидкостей и молекулярных кристаллов. От них зависят многие структурные, спектральные и другие свойства веществ.
Ориентационное взаимодействие. Полярные молекулы, в которых центры тяжести положительного и отрицательного зарядов не совпадают, например, HCl, H2O, NH3, ориентируются таким образом, чтобы рядом находились концы с противоположными зарядами. Между ними возникает притяжение:
42

Притяжение диполь-диполь может осуществляться только тогда, когда энергия притяжения превышает тепловую энергию молекул, что обычно имеет место в твердых и жидких веществах. Диполь-дипольное взаимодействие проявляется также в полярных жидкостях (вода, фтороводород и в ряде других).
Индукционное взаимодействие. Если полярная молекула окажется рядом с неполярными молекулами, то она начнет влиять на них. Поляризация нейтральной частицы под действием внешнего поля (наведение диполя) происходит благодаря наличию у молекул свойства поляризуемости γ. Поляризуемость – это способность вещества или молекулы образовывать диполь при наложении электрического поля. Постоянный диполь, или заряженная частица, может индуцировать дипольное распределение зарядов в неполярной молекуле.
Под действием заряженных концов полярной молекулы электронные облака неполярных молекул смещаются в сторону положительного заряда и подальше от отрицательного. Неполярная молекула становится полярной, и молекулы начинают
притягиваться друг к другу, только намного слабее, чем две полярные молекулы:

Этот вид взаимодействия проявляется, главным образом, в растворах полярных соединений в неполярных растворителях.
Дисперсионное взаимодействие. Между неполярными молекулами также может возникнуть притяжение. Электроны, которые находятся в постоянном движении, на миг могут оказаться сосредоточенными с одной стороны молекулы, то есть неполярная частица на мгновение станет полярной. Это вызывает перераспределение зарядов в соседних молекулах, и между ними устанавливаются кратковременные связи:

Силы притяжения между неполярными частицами (атомами, молекулами) являются короткодействующими. Эти связи очень слабые – самые слабые из всех межмолекулярных взаимодействий.
Дисперсионное взаимодействие универсально, оно присуще всем молекулам и чем больше поляризуемость молекул, тем сильнее дисперсионное взаимодействие.
Энергия дисперсионного взаимодействия невелика (0,8-8,0 кДж/моль), примерно в 100 раз меньше энергии химической связи.
43
Межмолекулярное отталкивание. Если бы молекулы только притягивались друг к другу, это привело бы к их слиянию. Но на очень малых расстояниях их электронные оболочки начинают отталкиваться.
Таким образом, межмолекулярное взаимодействие присутствует всегда и обусловлено действием ориентационных, индукционных и дисперсионных сил,
которые увеличивают температуры кипения и плавления веществ, напряжения сдвига и т.д. Наличие этих сил приводит к образованию целого ряда непрочных и устойчивых лишь при низких температурах соединений, в образовании которых могут участвовать и молекулы инертных газов: HgHe, WНе2, Ar(H2O)6 и т.д.
44