
- •А.Л.Галкин, в.К.Османов химия
- •Isbn 978-5-502-00158-8 © нгту им. Р.Е. Алексеева, 2013
- •Введение
- •Классификация неорганических веществ
- •Аллотропия
- •1.4 Соли
- •Комплексные соли
- •Генетическая связь между различными классами соединений
- •Основание Кислота Примеры
- •Основные понятия и законы химии
- •Закон сохранения массы
- •Закон постоянства состава
- •Закон эквивалентов
- •Закон авогадро
- •Уравнение состояния идеального газа
- •3. Строение атома
- •3.1. Квантовые числа
- •3.2. Принципы заполнения атомных орбиталей
- •3.3. Полная электронная формула атома
- •3.4. Периодический закон элементов д. И. Менделеева
- •Физический смысл химической периодичности
- •4. Химическая связь и строение молекул
- •4.1. Физические основы образования молекул
- •4.2. Метод валентных связей (метод вс)
- •Значения длины и энергии связи у галогеноводородных кислот
- •Взаимосвязь кратности, длины и энергии связи с - с, с - о и n - n
- •Одна s-орбиталь и одна p-орбиталь превращаются в две одинаковые «гибридные» орбитали, угол между осями которых равен 180°:
- •4.3. Метод молекулярных орбиталей
- •Энергия, длина и порядок связи в молекулах элементов I периода
- •4.4. Металлическая связь
- •4.5. Межмолекулярные взаимодействия
- •5. Энергетика и направление химических процесов
- •5.1. Термодинамическая система и ее состояния
- •5.2. Изменение свойств термодинамической системы
- •5.3. Энергия, работа, теплота
- •5.4. Обратимые и необратимые процессы
- •5.5. Первый закон термодинамики
- •5.6. Направление химических реакций
- •Второй закон термодинамики
- •Постулат планка (третий закон термодинамики)
- •6. Скорость химических реакций и и химическое равновесие
- •6.1. Влияние концентрации реагентов на скорость реакции
- •6.2. Влияние температуры на скорость реакции
- •6.3. Влияние катализатора на скорость реакции
- •А) без катализатора и б) в присутствии катализатора
- •6.4. Скорость гетерогенных химических реакций
- •6.5. Химическое равновесие
- •6.5.1. Влияние внешних факторов на состояние равновесия
- •7. Растворы
- •7.1. Вода
- •Вода в природе
- •7.2. Образование растворов
- •7.3. Способы выражения концентраций растворов
- •7.4. Растворы электролитов
- •7.4.2. Равновесные процессы в растворах электролитов
- •Цвета кислотно-основных индикаторов в зависимости от рН раствора
- •8. Окислительно – восстановительные реакции
- •8.1. Степень окисления
- •8.2. Типичные окислители и восстановители
- •8.3. Классификация окислительно-восстановительных реакций
- •8.4. Составление уравнений окислительно-восстановительных реакций
- •9. Основы электрохимических процессов
- •9.1. Измерение стандартных электродных потенциалов
- •9.2. Направление окислительно-восстановительных реакций
- •9.3. Влияние внешних факторов на величину электродного потенциала
- •9.4. Законы фарадея
- •9.5. Элементы технической электрохимии
- •10. Коррозионные процессы
- •10.1. Электрохимическая коррозия
- •10.2. Кинетика коррозионных процессов
- •10.3.Методы защиты металлов от коррозии
- •11. Номенклатура и классификация органических соединений
- •11.1. Номенклатура органических соединений
- •11. 2. Классификация органических соединений по номенклатуре июпак
- •12. Высокомолекулярные соединения
- •12.1. Классификация высокомолекулярных соединений
- •12.1.1. Классификация высокомолекулярных соединений по структуре макромолекул
- •12.1.2. Классификация полимеров по поведению при нагревании
- •12.2. Сополимеры
- •12.3. Синтез высокомолекулярных соединений
- •12.4. Свойства полимеров
- •12.5. Важнейшие полимерные материалы
- •Примеры решения задач
- •1.Основные понятия и законы химии
- •Строение атома
- •Химическая связь и строение молекул
- •Задача 4.
- •Молекула bf3 . Электронная формула атома бора 5b - 2s22p1. При образовании трех -связей атом бора переходит в возбужденное состояние
- •Решение. Последовательность действий для предсказания геометрии молекул на основании теории локализованных электронных пар следующая:
- •1.Подсчитывают число валентных электронов молекулы или иона и записывают электронную валентную структуру (льюисову структуру);
- •2.По валентной структуре определяют число -связывающих и несвязывающих электронных пар, т.Е. Тип молекулы aBnEm (n – число - связей, m – число несвязывающих электронных пар);
- •Энергетика и направление химических процессов
- •4 Моль н2 – - 150,8 кДж
- •Скорость химических реакций и химическое равновесие Задача 1
- •Растворы Примеры решения задач
- •Окислительно-восстановительные реакции примеры решения типовых задач
- •Основы электрохимических процессов
- •Коррозионные процессы
- •Галкин Андрей Львович Османов Владимир Кимович
- •603950, Нижний Новгород, ул.Минина, 24.
12.1. Классификация высокомолекулярных соединений
Различают три типа высокомолекулярных соединений:
1. Карбоцепные высокомолекулярные соединения - основные полимерные цепи состоят только из углеродных атомов.
2. Гетероцепные высокомолекулярные соединения - основные полимерные цепи, кроме атомов углерода, содержат гетероатомы (кислород, азот, фосфор, серу и др.).
3. Элементорганические высокомолекулярные соединения - основные полимерные цепи содержат элементы, не входящие в состав природных органических соединений (кремний, титан, свинец, олово и т. д). Каждый класс подразделяется на группы в зависимости от строения цепи, наличия кратных связей, количества и природы заместителей.
Гетероцепные соединения классифицируют также в зависимости от природы и количества гетероатомов, а элементорганические - в зависимости от сочетания углеводородных звеньев с атомами кремния, олова, алюминия и др.
Карбоцепные полимеры делятся на следующие основные группы:
1. Полимеры с насыщенными цепями
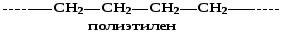
2. Полимеры с ненасыщенными цепями
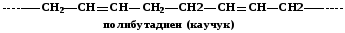
3. Галогензамещенные полимеры
132
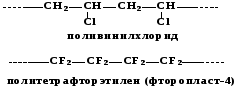
4. Полимеры спиртов (виниловый спирт) и их производных (винилацетат),
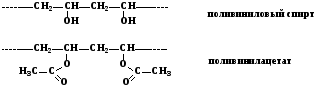
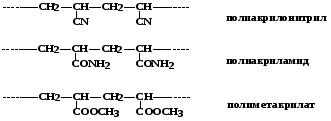
5. Полимеры непредельных карбоновых кислот и их производных (акрилонитрил, акриламид, эфиры акриловой кислоты)
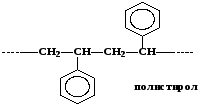
6. Полимеры ароматических углеводородов (стирол)
133
Гетероцепные полимеры делятся на следующие основные группы:
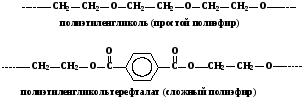
Полимеры, содержащие в основной цепи атомы кислорода (полиэфиры)
2. Полимеры, содержащие в основной цепи атомы азота (полиамиды)
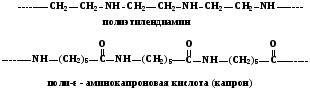
3.Полимеры, содержащие в основной цепи атомы серы (полисульфиды)
134
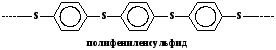
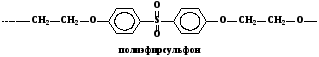
4. Полимеры, которые в основной цепи одновременно содержат несколько
различных гетероатомов (атомы азота, кислорода, серы, фосфора)
5.Элементоорганические полимерные соединения
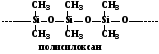
134
12.1.1. Классификация высокомолекулярных соединений по структуре макромолекул
Макромолекулы полимеров могут иметь линейную, разветвленную и пространственную трехмерную структуру.
Линейные полимеры состоят из макромолекул линейной структуры, которые представляют собой совокупность мономерных звеньев (-А-), соединенных в длинные неразветвленные цепи
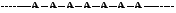
Каждое элементарное звено такого полимера связано только с двумя соседними. Линейные полимеры имеют волокнистую структуру, состоящую из переплетенных между собой макроцепей.
Разветвленные полимеры характеризуются наличием в основных цепях макромолекул, также состоящих из повторяющихся мономерных звеньев, боковых ответвлений, более коротких, чем основная цепь.

Полимеры, построенные из линейных и разветвленных молекул, эластичны, прочны, плавятся при сравнительно низких температурах и растворяются в различных органических растворителях.
Пространственные полимеры с трехмерной структурой характеризуются наличием макромолекулярных цепей, соединенных между собой посредством поперечных мостиков, образованных за счет функциональных групп в мономерной молекуле. Образование таких полимеров возможно только из мономерных молекул, содержащих две или более функциональные группы, способные участвовать в полимеризации (диены, акриловая кислота и т.д.).
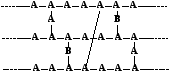
Пространственные полимеры с частым расположением поперечных связей называют сетчатыми. Они, как правило, не плавятся, не растворяются и обладают малой пластичностью.
135
