
- •А.Л.Галкин, в.К.Османов химия
- •Isbn 978-5-502-00158-8 © нгту им. Р.Е. Алексеева, 2013
- •Введение
- •Классификация неорганических веществ
- •Аллотропия
- •1.4 Соли
- •Комплексные соли
- •Генетическая связь между различными классами соединений
- •Основание Кислота Примеры
- •Основные понятия и законы химии
- •Закон сохранения массы
- •Закон постоянства состава
- •Закон эквивалентов
- •Закон авогадро
- •Уравнение состояния идеального газа
- •3. Строение атома
- •3.1. Квантовые числа
- •3.2. Принципы заполнения атомных орбиталей
- •3.3. Полная электронная формула атома
- •3.4. Периодический закон элементов д. И. Менделеева
- •Физический смысл химической периодичности
- •4. Химическая связь и строение молекул
- •4.1. Физические основы образования молекул
- •4.2. Метод валентных связей (метод вс)
- •Значения длины и энергии связи у галогеноводородных кислот
- •Взаимосвязь кратности, длины и энергии связи с - с, с - о и n - n
- •Одна s-орбиталь и одна p-орбиталь превращаются в две одинаковые «гибридные» орбитали, угол между осями которых равен 180°:
- •4.3. Метод молекулярных орбиталей
- •Энергия, длина и порядок связи в молекулах элементов I периода
- •4.4. Металлическая связь
- •4.5. Межмолекулярные взаимодействия
- •5. Энергетика и направление химических процесов
- •5.1. Термодинамическая система и ее состояния
- •5.2. Изменение свойств термодинамической системы
- •5.3. Энергия, работа, теплота
- •5.4. Обратимые и необратимые процессы
- •5.5. Первый закон термодинамики
- •5.6. Направление химических реакций
- •Второй закон термодинамики
- •Постулат планка (третий закон термодинамики)
- •6. Скорость химических реакций и и химическое равновесие
- •6.1. Влияние концентрации реагентов на скорость реакции
- •6.2. Влияние температуры на скорость реакции
- •6.3. Влияние катализатора на скорость реакции
- •А) без катализатора и б) в присутствии катализатора
- •6.4. Скорость гетерогенных химических реакций
- •6.5. Химическое равновесие
- •6.5.1. Влияние внешних факторов на состояние равновесия
- •7. Растворы
- •7.1. Вода
- •Вода в природе
- •7.2. Образование растворов
- •7.3. Способы выражения концентраций растворов
- •7.4. Растворы электролитов
- •7.4.2. Равновесные процессы в растворах электролитов
- •Цвета кислотно-основных индикаторов в зависимости от рН раствора
- •8. Окислительно – восстановительные реакции
- •8.1. Степень окисления
- •8.2. Типичные окислители и восстановители
- •8.3. Классификация окислительно-восстановительных реакций
- •8.4. Составление уравнений окислительно-восстановительных реакций
- •9. Основы электрохимических процессов
- •9.1. Измерение стандартных электродных потенциалов
- •9.2. Направление окислительно-восстановительных реакций
- •9.3. Влияние внешних факторов на величину электродного потенциала
- •9.4. Законы фарадея
- •9.5. Элементы технической электрохимии
- •10. Коррозионные процессы
- •10.1. Электрохимическая коррозия
- •10.2. Кинетика коррозионных процессов
- •10.3.Методы защиты металлов от коррозии
- •11. Номенклатура и классификация органических соединений
- •11.1. Номенклатура органических соединений
- •11. 2. Классификация органических соединений по номенклатуре июпак
- •12. Высокомолекулярные соединения
- •12.1. Классификация высокомолекулярных соединений
- •12.1.1. Классификация высокомолекулярных соединений по структуре макромолекул
- •12.1.2. Классификация полимеров по поведению при нагревании
- •12.2. Сополимеры
- •12.3. Синтез высокомолекулярных соединений
- •12.4. Свойства полимеров
- •12.5. Важнейшие полимерные материалы
- •Примеры решения задач
- •1.Основные понятия и законы химии
- •Строение атома
- •Химическая связь и строение молекул
- •Задача 4.
- •Молекула bf3 . Электронная формула атома бора 5b - 2s22p1. При образовании трех -связей атом бора переходит в возбужденное состояние
- •Решение. Последовательность действий для предсказания геометрии молекул на основании теории локализованных электронных пар следующая:
- •1.Подсчитывают число валентных электронов молекулы или иона и записывают электронную валентную структуру (льюисову структуру);
- •2.По валентной структуре определяют число -связывающих и несвязывающих электронных пар, т.Е. Тип молекулы aBnEm (n – число - связей, m – число несвязывающих электронных пар);
- •Энергетика и направление химических процессов
- •4 Моль н2 – - 150,8 кДж
- •Скорость химических реакций и химическое равновесие Задача 1
- •Растворы Примеры решения задач
- •Окислительно-восстановительные реакции примеры решения типовых задач
- •Основы электрохимических процессов
- •Коррозионные процессы
- •Галкин Андрей Львович Османов Владимир Кимович
- •603950, Нижний Новгород, ул.Минина, 24.
10. Коррозионные процессы
Коррозия – это процесс самопроизвольного разрушения металлов при их химическом, электрохимическом или биохимическом взаимодействии с частицами окружающей среды. Коррозионные процессы относятся к разряду окислительно - восстановительных реакций, в которых металл всегда является восстановителем, а частицы окружающей среды выступают в роли окислителя. Процесс коррозии становится возможным, если потенциал металла будет меньше, чем потенциал окислителя. Наиболее распространенным окислителем является атмосферный кислород.
Различают химическую, электрохимическую и биохимическую коррозию. Химическая коррозия металлов – это разрушение металлов под действием агрессивных газов при высоких температурах (газовая коррозия), а также
разрушение металлов в растворах неэлектролитов, т.е. в непроводящих средах.
Биохимическая коррозия вызывается жизнедеятельностью различных микроорганизмов, использующих металл в качестве питательной среды. Биокоррозия обычно сочетается с другими видами коррозии. Для ее развития наиболее благоприятны почвы определенного состава, застойные воды и некоторые органические продукты.
Электрохимическая коррозия встречается чаще других видов коррозионного разрушения и наиболее опасна для металлов. Она может протекать в газовой атмосфере, когда на поверхности металла возможна конденсация влаги (атмосферная коррозия), в почве (почвенная коррозия), в соленой и пресной воде.
В зависимости от характера разрушений при электрохимической коррозии различают сплошную коррозию, захватывающую всю поверхность металла и местную коррозию, локализующуюся на определенных участках. Очаги местной коррозии могут иметь вид пятен (пятнистая коррозия) или точек (питтинговая коррозия), которые могут захватывать зерна только одного из компонентов сплава (избирательная или селективная коррозия ), проходить через все зерна в виде узких трещин (транскристаллитная коррозия) или сосредоточиться на границах зерен (межкристаллитная коррозия).
10.1. Электрохимическая коррозия
Окислителем при электрохимической коррозии металлов может быть растворенный в воде кислород. В этом случае говорят, что коррозия протекает с кислородной деполяризацией:
О2 + 4Н+ + 4е = 2Н2О ( рН=0) Ео= +1,228 В
О2 + 2Н2О + 4е = 4ОН- (рН=7) Ео= +0,81 В
О2 + 2Н2О + 4е = 4ОН- (рН=14) Ео= +0,401 В
Таким образом, в кислой среде подвергаться коррозии с кислородной деполяризацией могут металлы, стандартный электродный потенциал которых отрицательнее +1,23 В, в нейтральной +0,81 и щелочной – отрицательнее + 0,4В.
111
Активные металлы в кислой среде корродируют с водородной деполяризацией, т.е в качестве окислителя выступают свободные ионы водорода:
2Н+ + 2е = Н2 (рН =0) Ео = 0 В
Наиболее простой моделью коррозионного процесса, идущего по электрохимическому механизму, является модель коррозионного гальванического элемента (микрогальванопар). Возникновение катодных и анодных участков на поверхности металла связано: с химической и геометрической неоднородностью поверхности; механическими напряжениями; неоднородностью коррозионной среды; температурным градиентом поверхности; контактом с другими металлами и многими другими факторами. Рассмотрим некоторые из этих факторов более подробно.
Химическая неоднородность поверхности. Ниже приведены схемы коррозии углеродистой стали для различных сред, в которых пассивными (катодными) участками являются зерна карбида железа (Fe3C).
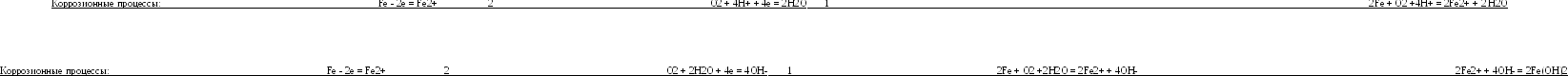
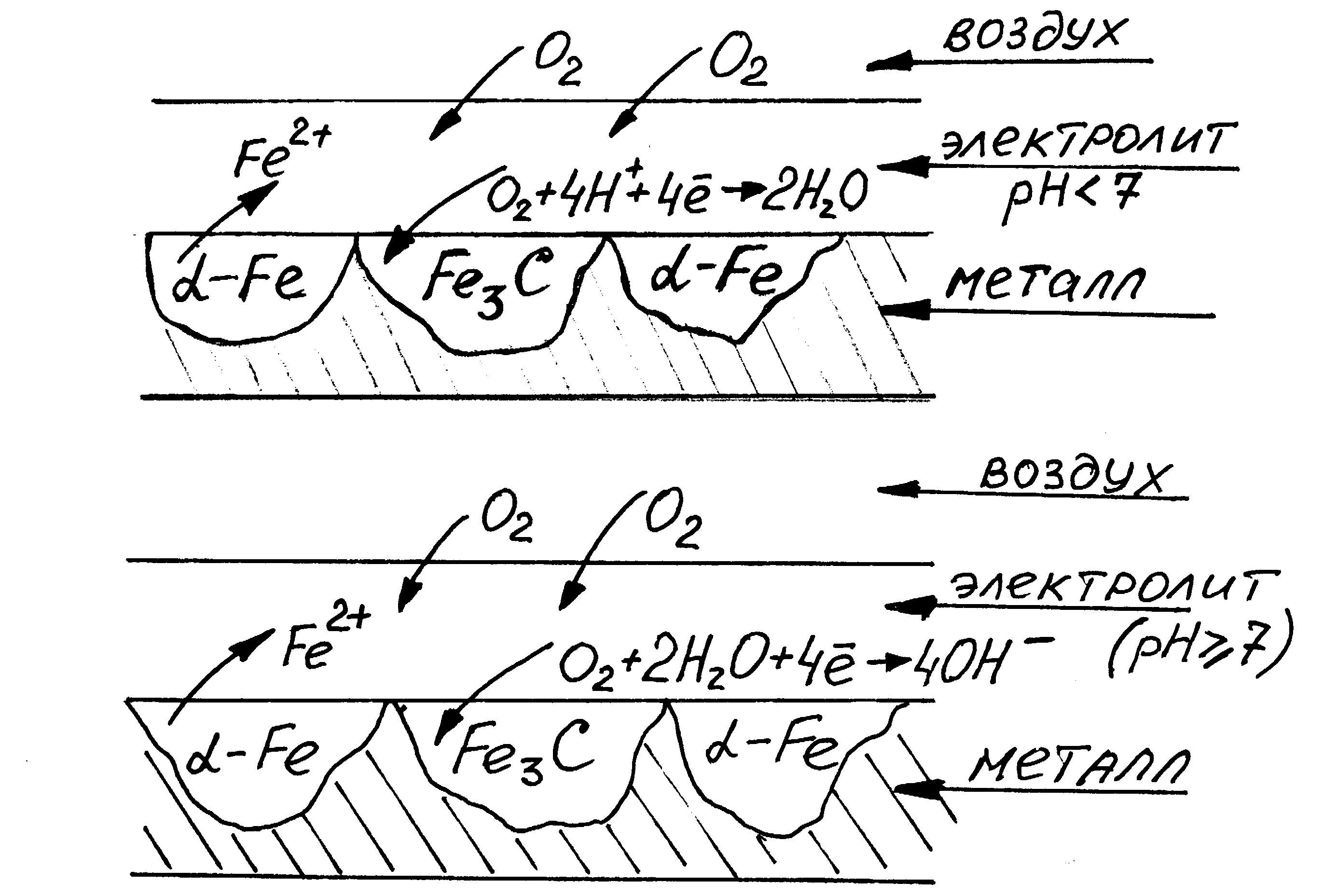
В
данном примере рассматривается работа
коррозионной микрогальванопары металл
и его соединение. При коррозии
эвтектического сплава возможен процесс
металл
и его соединение. При коррозии
эвтектического сплава возможен процесс
селективного вытравливания зерен одного из компонентов (более активного металла).
Контактная коррозия металлов. При контакте двух различных металлов, находящихся в растворе электролита, анодным участком будет более активный металл. Например:
Коррозионные процессы:
(кислая среда)
Fe - 2e = Fe2+ 2Н+ +2е = Н2 Fe + 2H+ = Fe2+ + H2
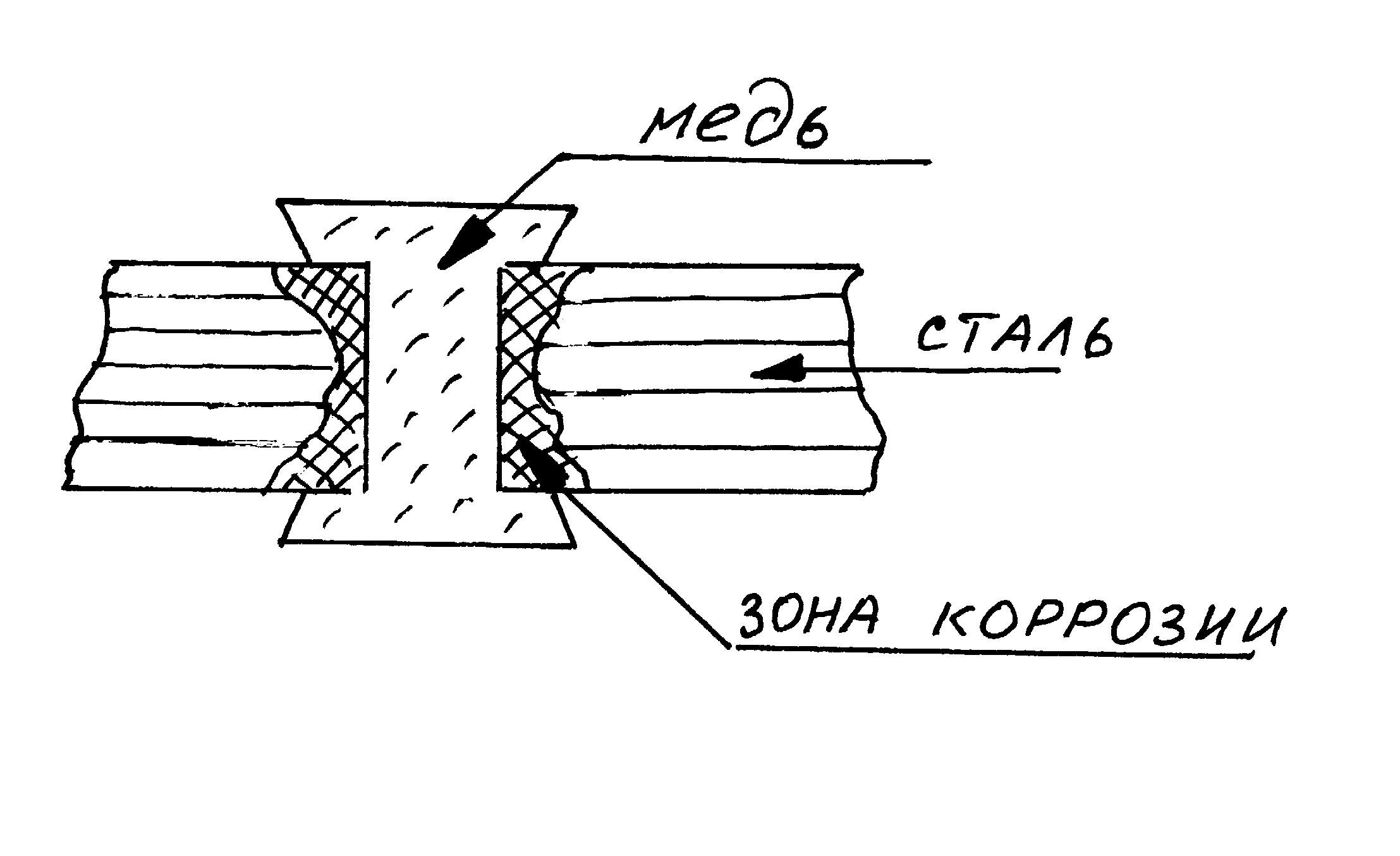
112
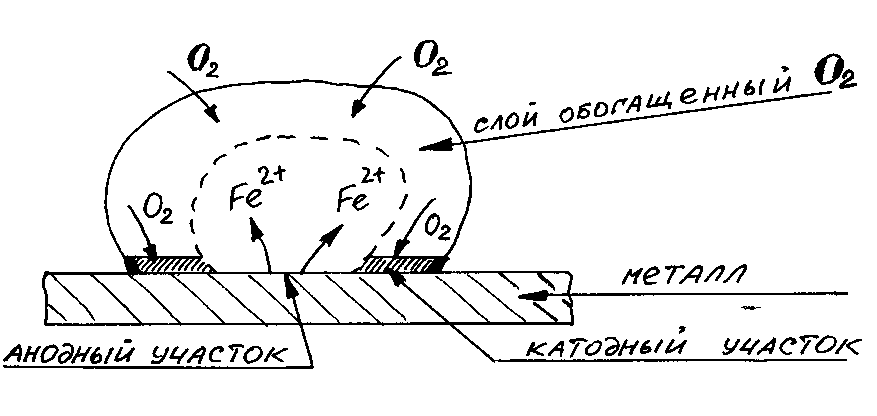
Влияние неоднородности состава коррозионной среды. Неоднородность состава среды может приводить к образованию микрогальванопар даже на поверхности одного и того же металла. Примером может служить коррозия металла под каплей воды. Так как поверхностные слои воды содержат больше растворенного кислорода, чем внутренние, поверхность металла в центре под каплей оказывается более активной (анодный участок). После высыхания капли в центре металлической пластинки появляется довольно глубокое пятно ржавчины. Такие процессы наиболее часто наблюдаются при атмосферной и почвенной коррозии. В общем случае неоднородность состава среды приводит к неравенству электродных потенциалов на различных участках поверхности металла, что и способствует образованию микрогальванопар.
Механические напряжения. Коррозионные микрогальванопары могут
возникать при действии внешних и внутренних механических напряжений (например, остаточные напряжения после сварки). Коррозия при действии внешних
и внутренних напряжений приводит к межкристаллитному растрескиванию, или так называемой «ножевой» коррозии.
