- •Росжелдор
- •Введение: основные понятия и определения
- •Основы номенклатуры неорганических соединений можно изложить следующим образом:
- •1 Классы неорганических соединений
- •Растворимость солей, кислот и оснований в воде
- •2 Химическая термодинамика
- •3 Скорость химических реакций
- •3.1 Количественное определение скорости химической реакции
- •3.2 Влияние катализатора
- •4 Химическое равновесие
- •4.1 Понятие о химическом равновесии
- •4.2 Динамический характер и устойчивость химического равновесия
- •4.3 Константа химического равновесия
- •4.4 Положение равновесия и его зависимость от внешних факторов
- •4.4.1 Зависимость равновесия от концентрации
- •4.4.2 Зависимость равновесия от температуры
- •4.4.3 Влияние давления на равновесие
- •4.4.4 Влияние катализатора на равновесие
- •В выражение константы равновесия входят равновесные концентрации веществ:
- •5 Строение электронных оболочек атомов. Периодический закон д.И. Менделеева
- •6 Химическая связь и строение молекул
- •7 Растворы
- •7.1 Способы выражения концентрации растворов
- •7.2 Физико-химические свойства разбавленных растворов неэлектролитов. Давление пара растворов. Закон Рауля
- •7.2.1 Понижение температуры замерзания и повышение температуры кипения растворов (следствия из закона Рауля)
- •7.3 Растворы электролитов
- •7.4 Ионное произведение воды. Водородный показатель рН
- •8 Окислительно-восстановительные реакции
- •9 Гальванические элементы
- •9.1 Понятие об электродном потенциале
- •9.2 Гальванический элемент
- •10 Коррозия металлов
- •10.1 Защита от коррозии
- •11 Электролиз
- •11.1 Катодные процессы
- •11.2 Анодные процессы
- •12 Полимеры
- •12.1 Реакция полимеризации
- •12.2 Реакция поликонденсации
- •12.3 Полимерные материалы
- •13 Дисперсные системы
- •14 Химический анализ
- •Библиографический список
- •Содержание
- •Мигаль Юрий Фёдорович
9 Гальванические элементы
9.1 Понятие об электродном потенциале
Электроды – электрохимические системы, состоящие из металла или полупроводника, погруженного в раствор или расплав электролита. Фактически, это металлические или графитовые изделия (проводники первого рода), находящиеся в среде, проводящей электрический ток (проводники второго рода). Носителями свободных зарядов в проводниках первого рода являются электроны, а в проводниках второго рода – ионы обоих знаков.
Металлы, как правило, имеют кристаллическое строение. В узлах кристаллической решетки расположены положительные ионы (катионы), находящиеся в равновесии с электронным газом:
Me Men+ + nē.
При погружении металла в раствор начинается сложное взаимодействие металла с компонентами раствора. Катионы металла выходят в электролит, а катионы электролита встраиваются в кристаллическую решетку металла. Со временем устанавливается равновесие между электродом и электролитом. В зависимости от того, куда смещено это равновесие, поверхность металла приобретает больший или меньший потенциал.
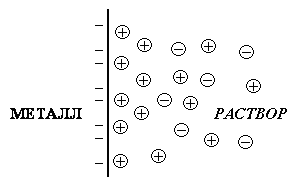
В результате перераспределения зарядов на границе «металл – раствор» возникает двойной электрический слой (рис. 9.1) и возникает скачок потенциала между металлом и раствором.
|
|
|
Рис. 9.1. Двойной электрический слой на границе раздела «металл – раствор» |
Потенциал электрода, опущенного в электролит, называется электродным потенциалом. Его значения зависят от многих факторов: материала электрода, состава электролита, температуры, давления и т. д. Величину электродного потенциала измеряют относительно некоторого выбранного электрода сравнения, потенциал которого принимают равным нулю. В качестве электрода сравнения обычно принимают стандартный водородный электрод.
Стандартным электродным потенциалом (0) называется потенциал металла, погруженного в раствор собственной соли и измеренный относительно водородного электрода в стандартных условиях. Стандартные условия: концентрация ионов в растворе 1 моль/л, температура Т = 298 К, давление Р = 1,01325∙105 Па.
По результатам измерений получен ряд стандартных электродных потенциалов (табл. 9.1), который позволяет дать количественную характеристику электрохимической активности металлов. Чем меньше значение φ0, тем сильнее выражены восстановительные свойства металла, т. е. он легче отдает электроны, легче окисляется. Чем больше значение φ0, тем сильнее окислительные свойства катиона металла, находящегося в растворе.
Таблица 9.1
Стандартные электродные потенциалы φ0 некоторых металлов
|
Электрод |
Электродный потенциал, В |
Электрод |
Электродный потенциал, В |
|
Li+/Li |
–3,05 |
Cd2+/Cd |
–0,40 |
|
Rb+/Rb |
–2,93 |
Co2+/Co |
–0,28 |
|
K+/K |
–2,92 |
Ni2+/Ni |
–0,25 |
|
Ba2+/Ba |
–2.90 |
Sn2+/Sn |
–0,136 |
|
Ca2+/Ca |
–2,87 |
Pb2+/Pb |
–0,127 |
|
Na+/Na |
–2,71 |
2H+/H |
0,00 |
|
Mg2+/Mg |
–2,37 |
Sb3+/Sb |
+0,20 |
|
Al3+/Al |
–1,70 |
Bi3+/Bi |
+0,22 |
|
Ti2+/Ti |
–1,60 |
Cu2+/Cu |
+0,34 |
|
V2+/V |
–1,18 |
Ag+/Ag |
+0,85 |
|
Mn2+/Mn |
–1,18 |
Hg2+/Hg |
+0,85 |
|
Zn2+/Zn |
–0,76 |
Pt2+/Pt |
+1,19 |
|
Cr3+/Cr |
–0,74 |
Au3+/Au |
+1,5 |
|
Fe2+/Fe |
–0,44 |
|
|
Для вычисления электродных потенциалов в условиях, отличных от стандартных, используют уравнение Нернста:
|
|
|
(9.1) |
где T – температура, К;
F – число Фарадея, равное 96 500 Кл/моль;
R – универсальная газовая постоянная, равная 8,314 Дж/(моль. К);
n – число электронов, принимающих участие в элементарном акте окислительно-восстановительного процесса;
![]() –концентрация
ионов металла в растворе, моль/л.
–концентрация
ионов металла в растворе, моль/л.
При T = 298 К формула Нернста приобретает вид:
|
|
|
(9.2) |