
- •Содержание
- •Введение
- •Промышленные методы получения изопропилбензола
- •Получение гидропероксида изопропилбензола
- •Механизм окисления изопропилбензола
- •2. Описание технологической схемы
- •3.Характеристика исходного сырья и готовой продукции, обращающихся в технологическом процессе
- •4.Материальный баланс установки окисления ипб в гидроперекись изопропилбензола
- •Расчёт состава примесей в окислительной шихте
- •Расчёт состава окислительной шихты
- •Расчёт количества окислителя
- •Расчёт количества продуктов, уносимых с абгазами
- •5.Тепловой баланс установки окисления ипб в гидроперекись изопропилбензола
- •6. Конструктивно-механический расчёт колонны
- •6.1. Расчёт общей высоты колонны.
- •6.2. Расчёт штуцеров колонны
- •6.3. Расчёт толщины обечайки корпуса.
- •6.4. Расчёт толщины стенки днища.
- •6.5. Расчёт опор колонны.
- •7.Расчёт и подбор вспомогательного оборудования
- •7.2. Расчёт теплообменного аппарата.
- •7.3. Расчёт ёмкости сбора абгазов.
- •8. Нормы технологического режима
- •9.Аналитический контроль технологического процесса
- •10. Автоматизация и сигнализация процесса
- •Заключение
- •Библиографический список
Министерство образования Российской федерации
Государственное образовательное учреждение
высшего профессионального образования
«САМАРСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ»
Кафедра общего органического и нефтехимического синтеза
Курсовой проект на тему:
«Окисление изопропилбензола»
Выполнил студент
5 курса 2 группы
(специальность 240401)
Артюнина Е.С.
_________________________
Научный руководитель
Дружинина Ю. А.
____________________
Работа защищена
апреля 2012г.
Оценка___________________
САМАРА 2012
Содержание
|
|
Введение |
3 |
|
1. |
Литературный обзор |
4 |
|
2. |
Описание технологической схемы процесса |
|
|
3. |
Характеристика сырья и готовой продукции |
|
|
4. |
Материальный баланс процесса |
|
|
5. |
Тепловой баланс процесса |
|
|
6. |
Конструктивно-механический расчёт основного аппарата |
|
|
7. |
Расчёт и подбор вспомогательного оборудования |
|
|
8. |
Нормы технологического режима |
|
|
9. |
Аналитический контроль производства |
|
|
10. |
Автоматизация и сигнализация процесса |
|
|
11. |
Заключение |
|
|
|
Библиографический список |
|
|
|
|
|
Введение
Фенол и ацетон являются важнейшими крупнотоннажными продуктами промышленности органического и нефтехимического синтеза. Совместное их получение гораздо более экономичнее всех ранее реализованных методов, вследствие чего оно нашло широкое применение во всех промышленно развитых странах мира.
Широкое распространение получил кумольный метод синтеза фенола совместно с ацетоном, основанный на окислении изопропилбензола в гидроперекись и последующем разложении гидроперекиси на фенол и ацетон. При этом образуется также небольшое количество побочных продуктов. Изопропилбензол, в свою очередь, получается алкилированием бензола пропиленом. Таким образом, исходным сырьем для получения фенола и ацетона по кумольному методу являются бензол и пропилен.
Первое крупное производство фенола и ацетона кумольным методом было реализовано в 1949 году в Советском Союзе. В основу этого производства были положены исследования П.П Сергеева, Б.Д. Кружалова и Р.Ю. Удриса по окислению изопропил бензола в гидроперекись с последующим её разложением на фенол и ацетон[2].
Процесс производства фенола и ацетона кумольным методом складывается из следующих стадий:
1. Алкилирование бензола пропиленом.
2. Окисление изопропилбензола в гидроперекись.
3. Выделение гидроперекиси изопропилбензола.
4. Разложение технической гидроперекиси изопропилбензола серной кислотой.
5. Нейтрализация реакционной массы после разложения.
6. Ректификация реакционной массы после разложения и выделение товарных фенола и ацетона.
Наиболее важной стадией кумольной технологии фенола является окисление кумола до его гидропероксида (ГПК), так как именно на этой стадии образуются основные и побочные продукты производства. Побочные продукты в дальнейших стадиях участвуют в разнообразных реакциях, тем самым усложняют производство.
Промышленные методы получения изопропилбензола
Изопропилбензол, или кумол, С6Н5СН (СН3)2 был впервые получен сухой перегонкой кальциевой соли или бариевой соли куминовой
(n- изопропилбензойной) кислоты. Впоследствии его обнаружили в продуктах сухой перегонки каменного угля. Строение кумола установили Р.Фиттинг и его ученики, а классический синтез по Вюрцу-Фиттингу взаимодействием йодистого изопропилбензола, бромбензола и натрия провёл О.Якобисен. в 1895 году был осуществлён синтез изопропилбензола из бензола и пропилена при помощи безводного хлористого алюминия в жидкой фазе.
Изопропилбензол в обычных условиях - бесцветная легкоподвижная жидкость с приятным запахом, при большом разведении, напоминающем запах древесины хвойных пород.
Несмотря на то, что химические методы получения изопропилбензола разработаны давно, промышленное производство его впервые было начато лишь во время второй мировой войны в СССР и США. В то время изопропилбензол целиком использовался в качестве высокооктановой добавки к авиационным бензинам.
В промышленности органического синтеза изопропилбензол стал применяться совсем недавно как исходный продукт для получения фенола и ацетона, а также в производстве а-метилстирола.
Известны три метода получения изопропилбензола, имеющие промышленное значение:
1.Алкилирование бензола пропиленом в присутствии безводного хлористого алюминия (алкилирование по Фриделю-Крафтсу).
2.Алкилирование бензола пропиленом в паровой фазе с применением фосфорнокислотного катализатора.
3.Алкилирование бензола пропиленом в жидкой фазе в присутствии серной кислоты как катализатора.
В России изопропилбензол производят главным образом алкилированиемпоФриделю-Крафтсу.
В основе всех перечисленных методов получения кумола лежит реакция алкилирования бензола пропиленом, которая протекает по схеме:
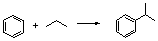
Физико-химические свойствагидропероксида изопропилбензола
Гидроперекись изопропилбензола С6Н5(СН3)2-О-ОН представляет собой бесцветную маслянистую, немного вязкую жидкость с характерным запахом, напоминающим запах озона. При попадании на кожу вызывает ожоги, подобно концентрированным растворам Н2О2.
В глубоком вакууме гидроперекись перегоняется без разложения. Перегонка при остаточном давлении выше 5 мм.рт. ст. сопровождается, по-видимому, уже незначительным разложением, о чём можно судить по бледной, зеленовато-жёлтой окраске дистиллята, отбираемого в этих условиях, в отличие от бесцветных дистиллятов, получаемых при большом разложении.
Гидроперкись хорошо растворима в обычных органических растворителях (спирте, эфире, бензоле, ацетоне и др.) и сравнительно плохо - в воде.
В обычных условиях гидроперекись является вполне стойким соединением; так, при хранении в течение длительного времени в стеклянной посуде на рассеянном свету(комнатная температура) она не разлагается. Опыты, проведённые П.Г.Сергеевым по хранению технической (87%-ной) гидроперекиси в таре из углеродистой стали показали, что состав гидроперекиси не изменился в течении четырёх лет.
Гидроперекись как «детонатор» часто добавляют к дизельному топливу для повышения его цетанового числа.
Гидроперкись не даёт окрашенных растворов с хромовой и титановой кислотами. Поэтому с помощью данных реактивов можно обнаружить присутствие перекиси водорода при наличии гидроперекиси изопропилбензола. При кипячении с водой гидроперекись частично перегоняется с водяным паром без изменения, остальное количество её распадается с образованием перекиси водорода и диметилфенилкарбинола.
Гидроперекись изопропилбензола медленно реагирует при комнатной температуре с раствором 2,4-динитрофенилгидразина в соляной кислоте, причём выпадает коричневый осадок, состав которого не исследован. Это обстоятельство следует учитывать при попытках идентификации кетонов и альдегидов в виде гидразонов в присутствии гидроперекиси.[2]
Гидроперекись является активным инициатором полимризации в водных эмульсиях таких соединений, как дивинил, стирол, а-метилстирол и т.п.
