
- •Содержание
- •Введение
- •Промышленные методы получения изопропилбензола
- •Получение гидропероксида изопропилбензола
- •Механизм окисления изопропилбензола
- •2. Описание технологической схемы
- •3.Характеристика исходного сырья и готовой продукции, обращающихся в технологическом процессе
- •4.Материальный баланс установки окисления ипб в гидроперекись изопропилбензола
- •Расчёт состава примесей в окислительной шихте
- •Расчёт состава окислительной шихты
- •Расчёт количества окислителя
- •Расчёт количества продуктов, уносимых с абгазами
- •5.Тепловой баланс установки окисления ипб в гидроперекись изопропилбензола
- •6. Конструктивно-механический расчёт колонны
- •6.1. Расчёт общей высоты колонны.
- •6.2. Расчёт штуцеров колонны
- •6.3. Расчёт толщины обечайки корпуса.
- •6.4. Расчёт толщины стенки днища.
- •6.5. Расчёт опор колонны.
- •7.Расчёт и подбор вспомогательного оборудования
- •7.2. Расчёт теплообменного аппарата.
- •7.3. Расчёт ёмкости сбора абгазов.
- •8. Нормы технологического режима
- •9.Аналитический контроль технологического процесса
- •10. Автоматизация и сигнализация процесса
- •Заключение
- •Библиографический список
Механизм окисления изопропилбензола
1.
2.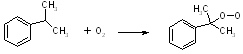

3.
Влияние различных факторов на процесс окисления изопропилбензола
Процесс окисления изопропилбензола чрезвычайно чувствителен по отношению к целому ряду факторов. Особенно большое значение имеет чистота изопропилбензола. Присутствие вокисляемом изопропилбензоле даже следов некоторых веществможет существенно изменить скорость процесса. В качествепримера можно привести влияние тиофена и его производных,а также фенола на процесс окисления. Наличие этих продуктовв чистом изопропилбензоле вполне возможно: тиофен содержится в бензоле, идущем на приготовление изопропилбензола,а следы фенола (появляются в изопропилбензоле при его получении. Оба продукта в большой степени тормозят окислениеизопропилбензола.[2]
Этот и многие другие факторы, как правило, не учитываютсяв равной степени в опытах одних и тех же авторов, а тем болеев работах, выполненных различными исследователями. В литературе опубликованы результаты опытов по окислению изопропилбензола при разнообразных скоростях накопления гидроперекиси и использовании сырья различного качества. Поскольку указанные опыты проводились по различной методике, топри оценке полученных данных можно легко допустить ошибку.
Однако при тщательном анализе всех имеющихся в настоящее время экспериментальных данных удается обнаружить общие закономерности, свойственные процессу окисления чистогоизопропилбензола. Сюда относится влияние температуры, глубины окисления, количества катализаторов, примесей некоторых веществ и других факторов (на выход и скорость накопления гидроперекиси. При окислении наиболее чистых образцов изопропилбензола скорость накопления гидроперекиси может достигать величины 10—13% в час, в то время как в промышленных условиях эта величина составляет 5—7% в час.


|
Рис 1. Зависимость скорости накопления гидроперикиси изопропилбензола от продолжительности окисления |
Рис 2. Влияние температуры на скорость накопления гидроперекиси изопропилбензола |
На рис. 1 показан характерный вид зависимости скорости накопления гидроперекиси от времени. Кривая имеет s-образную форму, свойственную цепным процессам. Вначале протекает процесс зарождения цепи (индукционный период), затем скорость реакции резко возрастает и остается постоянной в течение некоторого промежутка времени, после чего происходит уменьшение скорости, вызванное увеличивающимся распадом гидроперекиси и торможением (процесса окисления продуктами ее распада. Добавка некоторого количества гидроперекиси к изопропилбензолу перед окислением позволяет избежать индукционного периода.
Общий характер влияния температуры на скорость окисления изопропилбензола в пределах 90—120 °С показан на рис. 2. Повышение температуры приводит к увеличению скорости накопления гидроперекиси, но одновременно увеличивается и ее термический распад.
Было показано, что средняя скорость накопления гидроперекиси с повышением температуры последовательно от 90 до100 °С, от 100 до 110°С и от 110 до 120 °С возрастает неодинаково (соответственно в 2,3, 1,8 и 1,1 раза).
Установлено также, что при 120° С продукты распада в количестве более 1% можно обнаружить в реакционной массе через 1 ч после начала окисления; при 110 °С это происходит через 4—5 ч, а при 100 °С — через 6—8 ч.
Существенное значение для получения оптимальных выходовгидроперекиси имеет степень конверсии изопропилбензола вгидроперекись и продолжительность протекания процесса.В качестве примера приведем данные (рис. 3), полученные приокислении одного из образцов изопропилбензола при 110°С.Эти данные показывают, что для достижения высокого выход гидроперекиси при минимальном распаде необходимо ограничить глубину окисления изопропилбензола до содержания гидроперекиси 20—25%. Для других образцов изопропилбензолаэта величина составляет 20—30%. В условиях жидкофазногоокисления дальнейшее увеличение содержания гидроперекиси вреакционной массе неизбежно приводит к повышенному содержанию продуктов ее распада и к снижению выхода.
|
|
Поскольку
целью процесса окисления
изопропилбензолаявляется получение
гидроперекиси, то при выборе
оптимальныхусловий процесса необходимо
учитывать факторы, способствующие
распаду гидроперекиси. С этой точки
зрения следует подходить к выбору
материалов
для изготовления оборудования,применяющегося в производстве гидроперекиси, и к оценке схемтехнологического и аппаратурного оформления процесса. Так,многочисленные эксперименты показали, что
Рис 3. Влияние глубины окисления на
скорость накопления гидроперекиси
и её распад.
лучшие результаты достигаются при окислении изопропилбензола в аппаратах, изготовленных из нержавеющей стали марки 1Х18Н9Т. В этомслучае процесс протекает так же эффективно, как в стеклянномили эмалированном оборудовании.Как уже подчеркивалось, основным фактором, влияющимна процесс получения гидроперекиси с высоким выходом,является чистота изопропилбензола, подвергаемого окислению.Вредные примеси различных веществ, ингибирующих процессокисления, могут попадать в реакционную зону из следующихисточников: со свежим изопропилбензблом; с возвратным изопропилбензолом после отгонки его от гидроперекиси из реакционной смеси; в результате побочных реакций, протекающихв самом процессе окисления изопропилбензола; с воздухом, трипомощи которого производится окисление изопропилбензола.Рассмотрим каждый из этих источников в отдельности.
Примеси в свежем изопропилбензоле. Как показал опыт эксплуатации действующих предприятий по совместному получению фенола и ацетона, а также лабораторныеисследования, в свежем изопропилбензоле возможно наличиеследующих вредных примесей, способных в значительной степени тормозить или полностью ингибировать процесс окисления:сернистые соединения, непредельные углеводороды, алкилбензолы, ближайшие гомологи изопропилбензола, фенол.
Из сернистых соединений наибольшую опасность представляет тиофен, который содержится в бензоле, поступающем наприготовление изопропилбензола. Тиофен одновременно с бензолом может подвергаться алкилированию пропиленом, а образовавшийся при этом изопропилтиофен практически невозможноотделить от изопропилбензола путем ректификации.
Непредельные углеводороды образуются в процессе алкилирования бензола за счет полимеризации пропилена на катализаторе, применяемом при алкилировании. Отдельные фракциитримеров пропилена имеют темлературы кипения, близкие ктемпературе кипения изопропилбензола, и трудно отделимы отнего.
Алкилбензолы (этилбензол и бутилбензолы) появляютсяв процессе алкилирования за счет примесей этилена и бутиле-нов, содержащихся в пропилене, идущем на получение изопропилбензола. Этилбензол и бутилбензолы довольно простоотделить от изопропилбензола ректификацией. Однако есливсе же названные алкилбензолы попадают в чистый изопропилбензол, то скорость окисления его резко снижается.
Фенол неоднократно удавалось обнаруживать в чистом товарном изопропилбензоле с помощью чувствительных колориметрических методов.
Примеси в возвратном изопропилбензоле.Ввиду рассмотренных выше особенностей автокаталитическогопроцесса окисления, для достижения высоких выходов гидроперекиси окисление изопропилбензола проводят с конверсией, обычно не превышающей 30% за один проход. Поэтому 2/з изопропилбензола после отгонки от гидроперекиси возвращают снова на окисление. Такой изопропилбензол неизбежно бывает загрязнен фенолом, образовавшимся в результате распада гидроперекиси на стадии окисления. Из других продуктов распада гидроперекиси в возвратном изопропилбензоле могут присутствовать а-метилстирол и ацетофенон, которые также тормозят процесс окисления.
Примеси, образующиеся в самом процессе окисления. В ходе процесса окисления изопропилбензола за счет термического распада гидроперекиси появляются различные продукты, способные ингибировать реакцию окисления. Это в первую очередь продукты глубокого окисления изопропилбензола, такие, как фенол, формальдегид, муравьиная кислота и др.
Примеси в воздухе, применяемом в процессе окисления изопропилбензола. В воздух, поступающий на окисление изопропилбензола, вредные примеси могут попадать двумя путями. Во-первых, как показал опыт работы промышленных установок по окислению изопропилбензола в гидроперекись, весьма существенно правильно определить место забора свежего воздуха. Если в данном месте воздух загрязнен топочными или другими газами, особенно сернистым ангидридом или сероводородом, то это обстоятельство отрицательно влияет на скорость процесса окисления. Во-вторых, было установлено, что незначительные количества машинного масла, находящегося в сжатом воздухе после компримирования, значительно ингибируют процесс окисления изопропилбензола.
Технологическое оформление процесса окисления изопропилбензола
Экспериментальное изучение двух основных задач, связанных с процессом окисления изопропилбензола, — ускорения этого процесса и уменьшения распада гидроперекиси — привело к разработке двух технологически совершенно различных методов окисления.
По одному из этих методов, разработанному фирмой «DistillersCompanyLimited» на основании исследования Армстронга с сотр., окисление изопропилбензола проводится в водно-щелочной эмульсии при температуре около 90°С. рН среды поддерживается в пределах 8,5—10,5; при более высоких рН выходы гидроперекиси вследствие ее разложения снижаются, в то время как в интервале от нейтральной до кислой реакции окисление протекает с недопустимо малой скоростью.
Существенное значение имеет также соотношение водной иуглеводородной фаз: скорость реакции возрастает с увеличением разбавления изопропилбензола, но одновременно с этимотношение объем—время—конверсия в реакторе должно бытьвозможно больше. Для соотношения объем—время—выходоптимальная пропорция обеих фаз составляет —3:1. Дляобеспечения оптимальных условий реакции наряду с применением эмульгатора процесс проводят при интенсивном перемешивании. Важную роль играет выбор эмульгатора; установлено,что высокоэффективным эмульгатором является стеараг натрия.
По другому методу, разработанному фирмами «DistillersCompanyLimited» ,и «HerculesPowderCompany», окислениеизопропилбензола осуществляют в практически гомогенной фазепри 100—130°С. В патентах фирмы «DistillersCompanyLimited»указывается, что пределы взрываемости смеси кислород—изопропилбензол находятся в интервале 1—54% содержания изопропилбензола. Это соответствует парциальным давлениям изопропилбензола при температурах от 27 до 130 "С.Однако, поскольку -при 120—135°С могут образовыватьсявзрывчатые смеси кислорода и углеводорода, к смеси добавляют водяной пар.
Окисление в гомогенной фазе часто проводят в несколькоступеней при различных температурах, например на первойступени при 120°С до получения в реакционной массе около10% гидроперекиси, на второй — при 117°С до содержаниягидроперекиси 15%, на третьей — при 115°С примерно до20%-пого содержания гидроперекиси и на четвертой — при10°С до содержания гидроперекиси 27%. При таком способеокисления уменьшается распад гидроперекиси и образованиепобочных продуктов (диметилфенилкарбинола и ацетофенона),содержание которых возрастает с увеличением концентрациигидроперекиси в реакционной массе. В качестве окислителяприменяют воздух или очищенный кислород. При использовании кислорода из реактора уносится меньше изопропилбензолаи достигается более высокая пропускная способность на единицу объема реактора. Преимущество применения воздуха заключается в его более низкой стоимости и меньшей опасностиобразования взрывчатой смеси. Для уменьшения уноса изопропилбензола окисление его воздухом проводят в большинствеслучаев при повышенных избыточных давлениях (около4—6 or).
В сообщении о пуске первого завода по производству фенола и ацетона фирмы «British—AmericanShowingan» в г. Монреале (Канада) указывается, что окислительная установка состоит из четырех вертикальных колонн диаметром 1,2 м и высотой 9 м, размещенных каскадно. Сжатый воздух поступает внижнюю часть каждой колонны, изопропилбензол также подается в нижнюю часть первой колонны, проходит до верха колонны, перетекает в нижнюю часть второй колонны и т. д.
Скорость образования гидроперекиси, или скорость конверсииувеличивается при использовании в качестве сырья тщательно очищенногоизопропилбензола составляет в среднем от 3 до 13% в час.Максимальная из известных в литературе скоростей конверсииравна 11 —13% гидроперекиси изопропилбензола в час, получаемой путем окисления изопропилбензола при 120°С в присутствии металлической меди, предварительно обработаннойазотной кислотой52. Несмотря на высокую скорость образованиягидроперекиси, о промышленном применении этого метода ничего неизвестно. Как сообщают, это объясняется частыми нарушениями нормального хода процесса, вызываемого чувствительностью реакции к состоянию поверхности меди53. Скоростьреакции окисления, достигаемая в промышленных условиях,составляет 5—7% гидроперекиси изопропилбензола в час.
Как уже указывалось, в начале реакции выход гидроперекиси почти количественный. Однако в процессе дальнейшейконверсии изопропилбензола происходит разложение гидроперекиси и протекают другие побочные реакции, которые снижают эффективность ее образования. Это снижение в значительной степени вызывается разложением гидроперекиси, которое катализируется карбоновыми кислотами (главным образоммуравьиной кислотой), образующимися в небольших количествах в процессе окисления. Во избежание описанного явленияреакцию проводят в присутствии щелочи в количестве, достаточном для нейтрализации кислот по мере их образования.Установлено, что оптимальные условия достигаются прирН = 8,5—10,5. Необходимую щелочность среды можно поддерживать при помощи карбоната натрия с добавкой малорастворимой соли, например стеарата натрия.
Для ускорения реакции окисления изоропилбензола былопредложено большое число катализаторов и промоторов. Скорость окисления изопропилбензола, как известно, увеличиваетсяпри применении солей тяжелых металлов (например, нафтенатов и резинатов кобальта, марганца, свинца и других металлов) ; с другой стороны, при этом возрастает также степеньразложения образовавшейся в процессе окисления гидроперекиси. Поэтому приходится подбирать условия, в которых окисление изопропилбензола протекает со значительно большейскоростью, чем разложение гидроперекиси. Таким основнымфактором является концентрация катализатора.
Сообщают, что оптимальный выход достигается при концентрации на.фтената марганца 0,25—0,5%. Установлено, что содержание катализатора не должно превышать концентрации,при которой разлагается 10% перекиси, содержащейся в смеси,состоящей из 15 вес частей гидроперекиси изопропилбензолаи 85 вес. частей изопропилбензола при 80°С в течение 45 ч.Такое требование ограничивает допустимую концентрацию растворенного марганца до 0,0012%. Если соединение марганцанерастворимо в изопропилбензоле, то катализатор можно вводить в большей концентрации. Так, например, предусматривают применение двуокиси марганца в количестве 0,5—1,0% от веса изопропилбензола. Использование щелочного катализатора благоприятно сказывается на скорости и на выходе продуктов реакции. Указывают, что добавление формиата натрия увеличивает выход гидроперекиси с 1,74 до 5,59% в час. Аналогично действует карбонат натрия. Опубликованы также данныеоб увеличении скорости реакции и повышении выходов гидроперекиси в случае использования в качестве катализаторов при окислении изопропилбензола третичных аминов (например, пиридин) в количестве 0,01—1 вес. %.
По мере протекания реакции окисления усиливаются побочные реакции, снижающие выход гидроперекиси. Поэтому полную конверсию изопропилбензола за один проход осуществитьневозможно. В промышленной практике глубина окисления(степень конверсии изопропилбензола за проход) поддерживается в пределах 25—30%. Таким образом, реакционная масса, получаемая в результате окисления, содержит около65—70% непревращенного изопропилбензола. Обычно основнуюмассу этого углеводорода удаляют путем перегонкив вакууме;конечная смесь содержит от 75 до 85% гидроперекиси изопропилбензола.
В сообщении о пуске завода по производству фенола и ацетона в Шотландии указывается, что изопропилбензол поступает в окислительную систему, где подвергается окислению подизбыточным давлением в несколько атмосфер при 100 °С. Окислительная система характеризуется рядом особенностей, обеспечивающих достижение максимальной эффективности окисления;одним из важных условий является строгий контроль за температурой.
Поскольку в процессе окисления значительная часть изопропилбензола не вступает в реакцию, необходимо концентрирование гидроперекиси. При этом в глубоком вакууме от высококипящей гидроперекиси отгоняется изопропилбензол. Отгонкупроизводят в секционных перегонных аппаратах, сконструированных таким образом, чтобы избежать распада гидроперекиси.Отогнанный изопропилбензол возвращается на окисление.
Концентрат гидроперекиси, содержащий ряд примесей, средикоторых преобладают остаточный изопропилбензол, ацетофенони диметилфенилкарбинол, направляется без дальнейшей очистки для разложения гидроперекиси на фенол и ацетон.

|
Рис. 4. Принципиальная схема установки каскадного типа для окисления изопропилбензола в гидроперекись 1 – реакторы; 2 – теплообменники; 3 – промежуточные ёмкости; 4 – сборник реакционной массы; 5 – насос; 6, 7 – конденсаторы
|
Аппаратурное оформление процесса окисления изопропилбензола в гидроперекись может быть различным. Общим длявсех способов непрерывного окисления изопропилбензолаявляется проведение процесса в несколько ступеней (от 3 до 8).Довольно распространено расположение отдельных ступеней попринципу каскада (рис. 4). [2]
Для
гетерогенных процессов окисления,
протекающих вводно-щелочной среде,
наиболее пригодны аппараты с мешалками
или эрлифтами. Эрлифты применимы также
для процессов гомогенного окисления.
|
Рис. 5. Реактор колонного типа
|
колонной отверстиями и переливными стаканами на каждой тарелке (рис. 5).
Сравнивая секционную колонну с каскадной системой,необходимо отметить, что последняя обладает рядом, преимуществ, основные из которых состоят в следующем:
В случае нарушения нормального режима в какой-либоступени (колонне), вызванногоповышением температуры ибыстрым распадом гидроперекиси (приводящим к большомувыделению газов и паров),сработают предохранительнаямембрана или клапан, установленные в верхней части колонны, и образовавшиеся газыбудут направленно выведеныв атмосферу.
В колоннах секционного типа предохранительные клапаны, расположенные наверху, посуществу не играют никакойроли, и указанное нарушениережима может привести к аварии.
Параллельность в потоках воздуха и изопропилбензола благоприятствует окислению, так как легкокипящие продукты распада гидроперекиси (муравьиная кислота и формальдегид) будут удаляться с отходящими газами. Отработанный воздух с последнихступеней окисления, содержащий больше продуктов распада,не попадает на первые ступени, поскольку на каждую ступеньподают свежий воздух.
