
- •Міністерство освіти і науки України
- •1 Програма з розділу «загальні основи аналітичної хімії»
- •Тема 1. 1 Предмет загальної, неорганічної та аналітичної хімії. Значення дисципліни для підготовки товарознавця. Найважливіші поняття та закони загальної хімії, які потрібні для вивчення курсу
- •Тема1.2 Періодичний закон та періодична система елементів
- •Тема 1.3 Сучасні теорії будови атомів та хімічного зв’язку як основа вивчення хіміко-аналітичних і фізичних властивостей сировини та матеріалів
- •Тема 1.4 Швидкість та механізм хімічних реакцій
- •Тема 1.5 Розчини та теорія електролітичної дисоціації
- •Тема 1.6 Рівновага у розчинах солей, які піддаються гідролізу
- •Тема 1.7 Рівновага у розчинах малорозчинних сполук
- •Тема 1.8 Рівновага у розчинах координаційних (комплексних) сполук
- •Тема 1.9 Рівновага при перебігу окисно-відновних реакцій (овр)
- •Тема 1.10 Систематичний аналіз катіонів та аніонів
- •Тема 1.11 Органічні аналітичні реагенти
- •Тема 1.12 Теорія та практика відбирання проби та її підготовка
- •Тема 1.13 Методи розподілу і концентрування
- •Тема 1.14 Об’ємний (титриметричний) аналіз
- •Тема 1.15 Гравіметричний (ваговий) аналіз
- •Студент повинен вміти:
- •Додаткова
- •Методичні матеріали
- •2 Приклади рішення типових задач. Питання та задачі до контрольних робіт
- •2.1 Приклади рішення типових задач з теми
- •2.2 Питання та задачі до контрольних робіт з теми
- •2.3. Приклади рішення типових задач з теми
- •2.4 Питання та задачі до контрольних робіт з теми
- •2.5 Приклади рішення типових задач з теми
- •2.6 Питання та задачі до контрольних робіт з теми
- •2.7 Приклади рішення типових задач з теми “Хімічний зв’язок”
- •2.8 Питання та задачі до контрольних робіт з теми “Хімічний зв’язок”
- •2.9 Приклади рішення типових задач з теми
- •2.10 Питання та задачі до контрольних робіт з теми
- •2.11 Приклади рішення типових задач з теми
- •2.12 Питання та задачі до контрольних робіт з теми
- •2.13 Приклади рішення типових задач з теми
- •2.14 Питання та задачі до контрольних робіт з теми
- •2.15 Приклади рішення типових задач з теми
- •2.16 Питання та задачі до контрольних робіт з теми
- •2.17 Приклади рішення типових задач з теми
- •2.18 Питання та задачі до контрольних робіт з теми
- •2.19 Приклади рішення типових задач з теми
- •2.20 Питання та задачі до контрольних робіт з теми
- •2.21 Приклади рішення типових задач з теми
- •2.22 Питання та задачі до контрольних робіт з теми
- •3. Варіанти контрольних робіт
2.17 Приклади рішення типових задач з теми
“Рівновага при перебігу окисно-відновних реакцій (ОВР)”
Приклад 1. Методом напівреакцій підберіть коефіцієнти в наступній окиснювально-відновній реакції. Вкажіть окисник і відновник:
![]() .
.
Розв’язання:
Визначаємо ступені окиснення атомів, які їх змінюють у реагуючих речовин та продуктів реакції:
+3 +7 +6 +2
![]()
Далі визначаємо окисник та відновник.
У даній реакції окисником виступає
манган(VII)сполуки
![]() ,
який відновлюється до манган(II)-катіону,
а хром(III)-катіон
у хром(III)
сульфаті може бути тільки відновником.
,
який відновлюється до манган(II)-катіону,
а хром(III)-катіон
у хром(III)
сульфаті може бути тільки відновником.
Складаємо іонну схему реакції, записуючи тільки ті іони та молекули, які беруть участь у окисно-відновній реакції. При цьому сильні електроліти записуємо у вигляді іонів, а слабкі електроліти та нелектроліти-у вигляді молекул:
![]() .
.
3) Складаємо рівняння напівреакцій окиснення та відновлення так, щоб кількості атомів кожного з елементів у лівій та правій частинах були однаковими:
![]() ;
;
![]() .
.
4) Множимо рівняння кожної напівреакції на такий коефіцієнт, щоб кількість електронів, які приєднуються, дорівнювала кількості відданих електронів:
![]() 5
5
![]() 6
6
Одержані коефіцієнти переносимо у повне іонне рівняння окиснювально-відновної реакції:
![]() .
.
Записуємо молекулярне рівняння та перевіряємо за киснем вірність написання рівняння реакції (кількість атомів кисню зліва повинна дорівнювати кількості атомів кисню справа):
![]()
2.18 Питання та задачі до контрольних робіт з теми
“Рівновага при перебігу окисно-відновних реакцій (ОВР)”
Що називають окисненням та відновленням, окисником та відновником? Назвіть речовини найбільш відомі як сильні окисники чи відновники. За рахунок чого кожна з них проявляє ці властивості?
Що покладено в основу класифікації хімічних процесів на реакції обміну та окисно-відновні? Які з наведених нижче реакцій відносяться до перших чи других:
![]()
![]()
![]() ,
,
![]()
![]()
![]()
Що називають окисно-відновними коефіцієнтами? Які існують методи для їх визначення? Покажіть сутність кожного та поясніть, в яких випадках і чому один з них краще застосовувати ніж інший.
Які два одночасно перебігаючих процеси включає кожна з реакцій, що виражаються наступними схемами:
а)
![]() ;
в)
;
в)
![]() ;
;
б)
![]() ;
г)
;
г)
![]() .
.
В яких випадках речовини проявляють тільки окисну, тільки відновну, обидві функції? Наведіть відповідні приклади.
Який елемент і в якому ступені окиснення визначає можливість для наведених нижче речовин проявляти окисні чи відновні властивості:
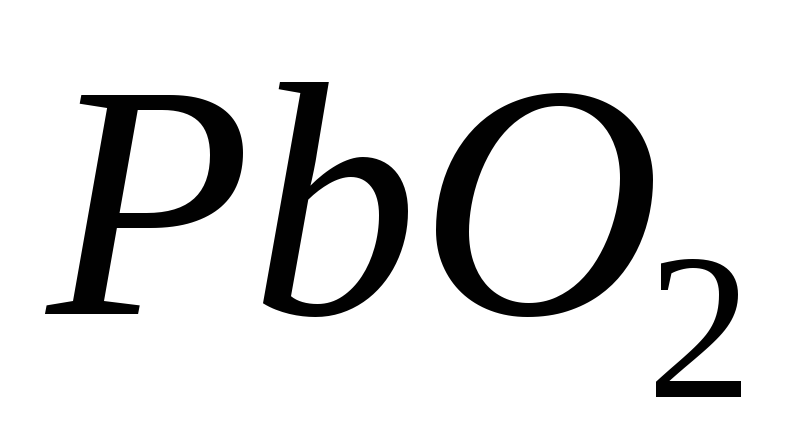 ,
,
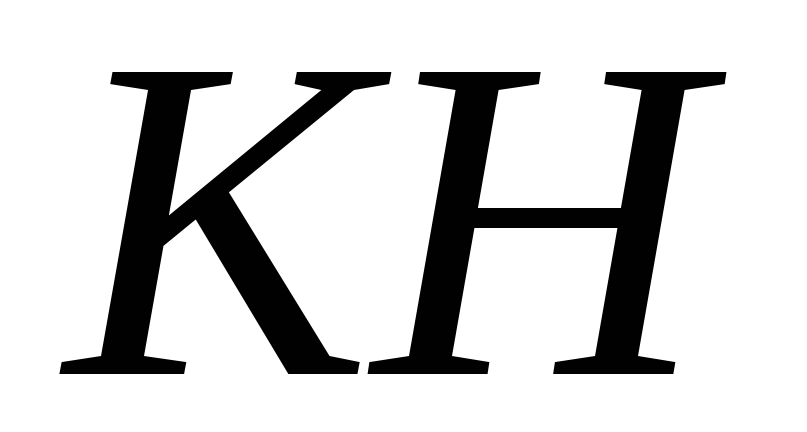 ,
,
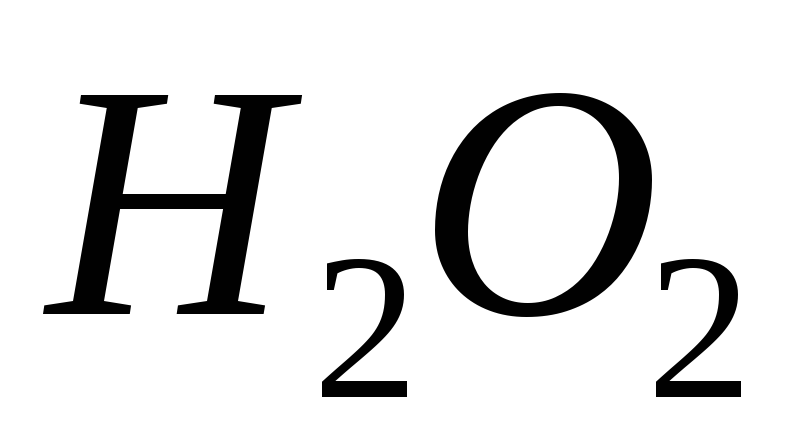 ,
,
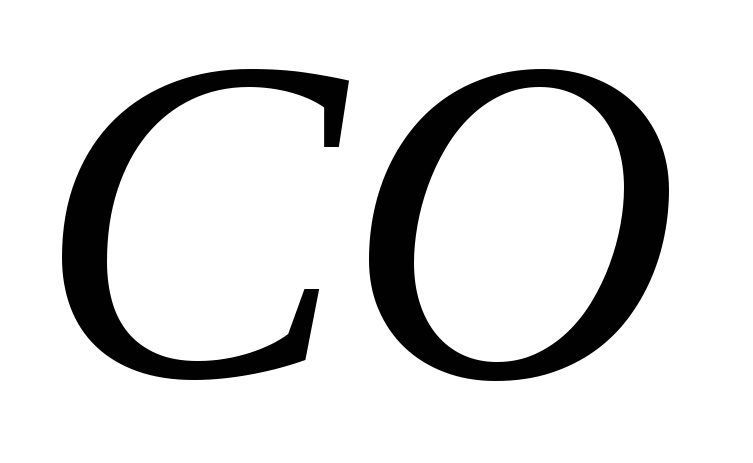 ,
,
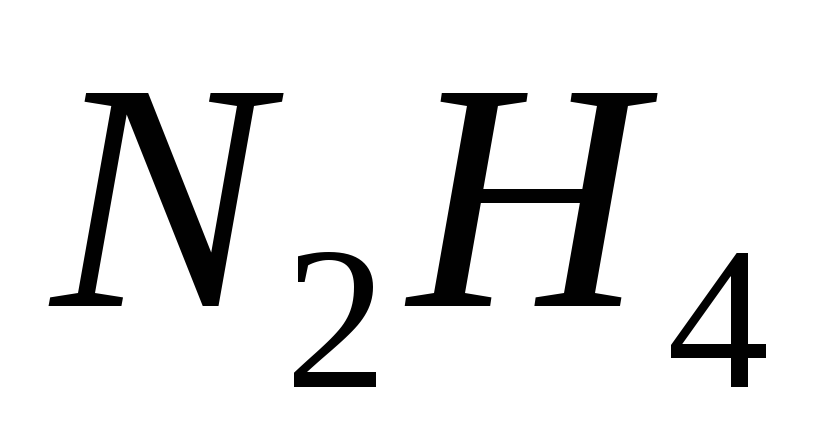 ,
,
 ?
?Які елементи у вигляді простих речовин є:
а) більш сильними відновниками (калій чи мідь, мідь чи золото);
б) більш сильними окисниками (бром чи йод, сірка чи хлор)?
На чому базується класифікація ОВР? Наведіть можливі типи цих реацій. Які з них називають реакціями диспропорціонування та зворотнього диспропорціонування?
|
№ |
Напишіть рівняння напівреакцій та іонно-молекулярні рівняння, якими можуть бути виражені процеси окиснення та відновлення в водних розчинах, що проходять за схемами: |
|
279 |
а)
б)
|
|
280 |
а)
б)
|
|
281 |
а) б)
|
|
№ |
Методом напівреакцій підберіть коефіцієнти в схемах окиснювально-відновних реакцій. Вкажіть окисник і відновник |
|
282 |
а)
б)
|
|
283 |
а)
б)
|
|
284 |
а)
б)
|
|
285 |
а)
б)
|
|
286 |
а)
б)
|
|
287 |
а)
б)
|
|
288
|
а)
б)
|
|
289 |
а)
б)
|
|
290 |
а)
б)
|
|
291 |
а)
б)
|
|
292 |
а)
б)
|
|
293 |
а)
б)
|
|
294 |
а)
б)
|
|
295 |
а)
б)
|
|
296 |
а)
б)
|
|
297 |
а)
б)
|
|
298 |
а)
б)
|
|
299 |
а)
б)
|
|
300 |
а)
б)
|
