
- •Міністерство освіти і науки України
- •1 Програма з розділу «загальні основи аналітичної хімії»
- •Тема 1. 1 Предмет загальної, неорганічної та аналітичної хімії. Значення дисципліни для підготовки товарознавця. Найважливіші поняття та закони загальної хімії, які потрібні для вивчення курсу
- •Тема1.2 Періодичний закон та періодична система елементів
- •Тема 1.3 Сучасні теорії будови атомів та хімічного зв’язку як основа вивчення хіміко-аналітичних і фізичних властивостей сировини та матеріалів
- •Тема 1.4 Швидкість та механізм хімічних реакцій
- •Тема 1.5 Розчини та теорія електролітичної дисоціації
- •Тема 1.6 Рівновага у розчинах солей, які піддаються гідролізу
- •Тема 1.7 Рівновага у розчинах малорозчинних сполук
- •Тема 1.8 Рівновага у розчинах координаційних (комплексних) сполук
- •Тема 1.9 Рівновага при перебігу окисно-відновних реакцій (овр)
- •Тема 1.10 Систематичний аналіз катіонів та аніонів
- •Тема 1.11 Органічні аналітичні реагенти
- •Тема 1.12 Теорія та практика відбирання проби та її підготовка
- •Тема 1.13 Методи розподілу і концентрування
- •Тема 1.14 Об’ємний (титриметричний) аналіз
- •Тема 1.15 Гравіметричний (ваговий) аналіз
- •Студент повинен вміти:
- •Додаткова
- •Методичні матеріали
- •2 Приклади рішення типових задач. Питання та задачі до контрольних робіт
- •2.1 Приклади рішення типових задач з теми
- •2.2 Питання та задачі до контрольних робіт з теми
- •2.3. Приклади рішення типових задач з теми
- •2.4 Питання та задачі до контрольних робіт з теми
- •2.5 Приклади рішення типових задач з теми
- •2.6 Питання та задачі до контрольних робіт з теми
- •2.7 Приклади рішення типових задач з теми “Хімічний зв’язок”
- •2.8 Питання та задачі до контрольних робіт з теми “Хімічний зв’язок”
- •2.9 Приклади рішення типових задач з теми
- •2.10 Питання та задачі до контрольних робіт з теми
- •2.11 Приклади рішення типових задач з теми
- •2.12 Питання та задачі до контрольних робіт з теми
- •2.13 Приклади рішення типових задач з теми
- •2.14 Питання та задачі до контрольних робіт з теми
- •2.15 Приклади рішення типових задач з теми
- •2.16 Питання та задачі до контрольних робіт з теми
- •2.17 Приклади рішення типових задач з теми
- •2.18 Питання та задачі до контрольних робіт з теми
- •2.19 Приклади рішення типових задач з теми
- •2.20 Питання та задачі до контрольних робіт з теми
- •2.21 Приклади рішення типових задач з теми
- •2.22 Питання та задачі до контрольних робіт з теми
- •3. Варіанти контрольних робіт
2.2 Питання та задачі до контрольних робіт з теми
“Класи неорганічних сполук”
Назвати оксиди, що мають формули:

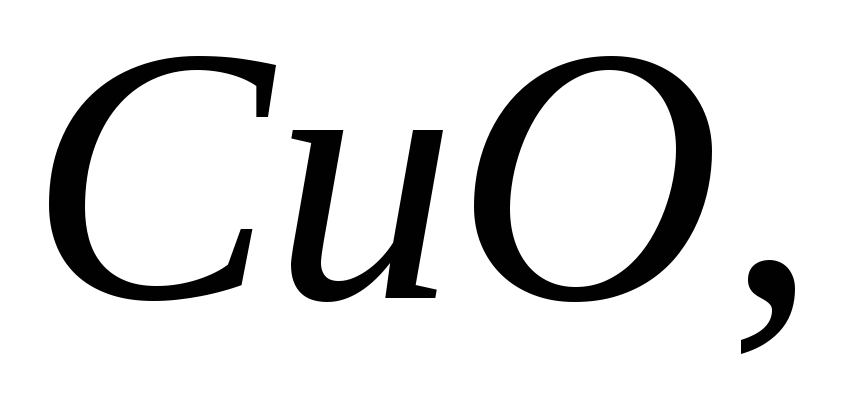
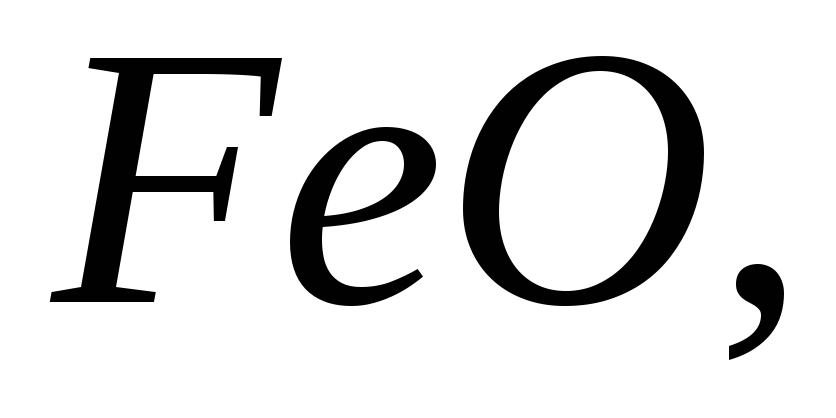
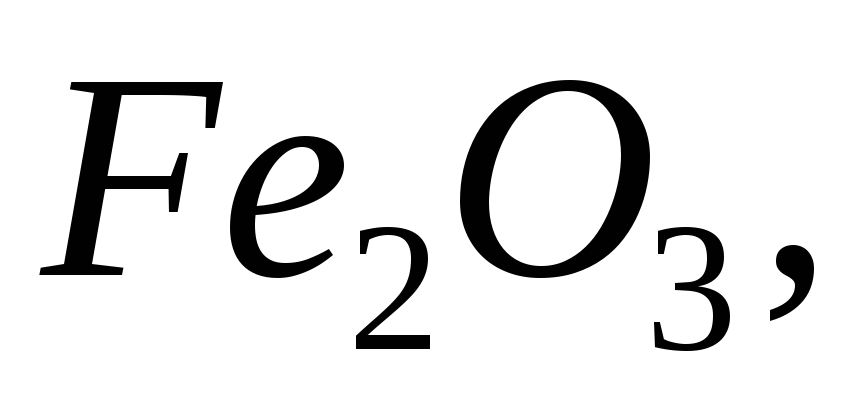

Напишіть формули оксидів
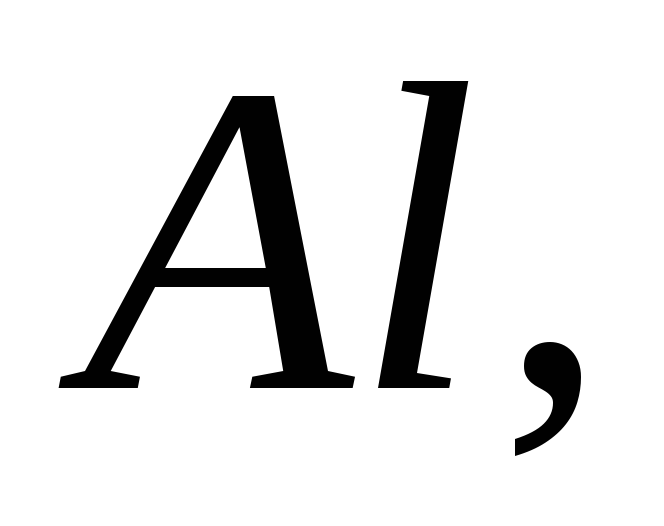
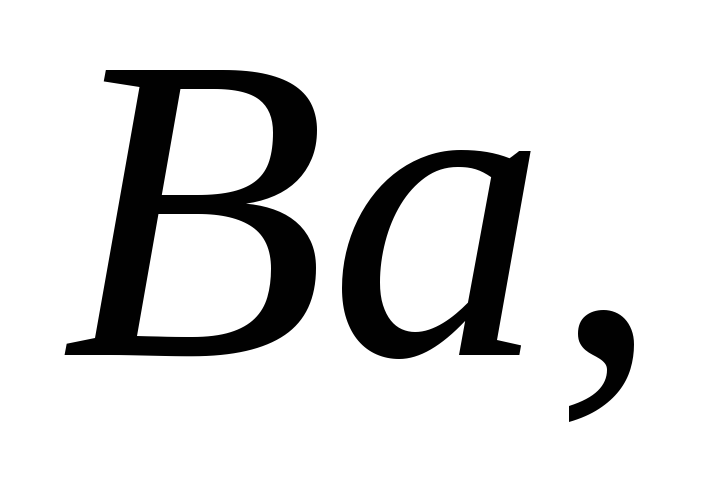

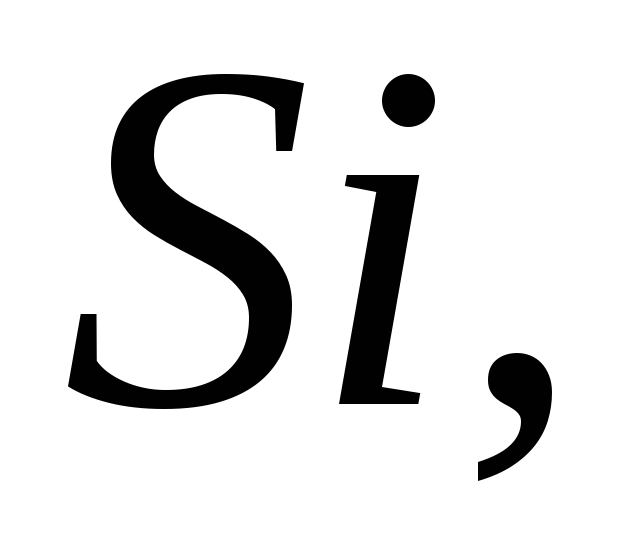
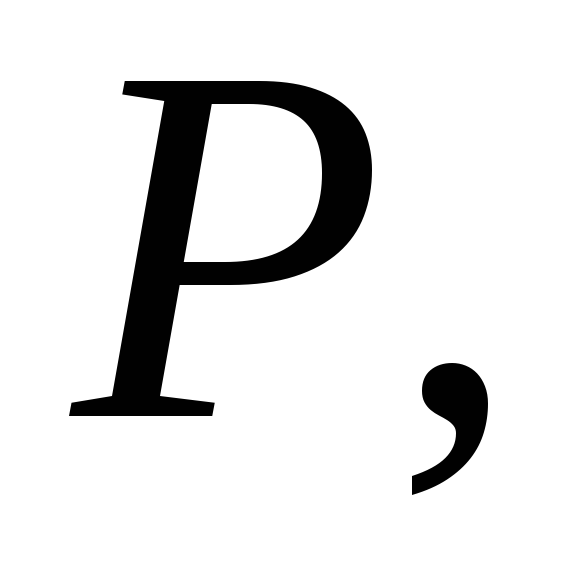

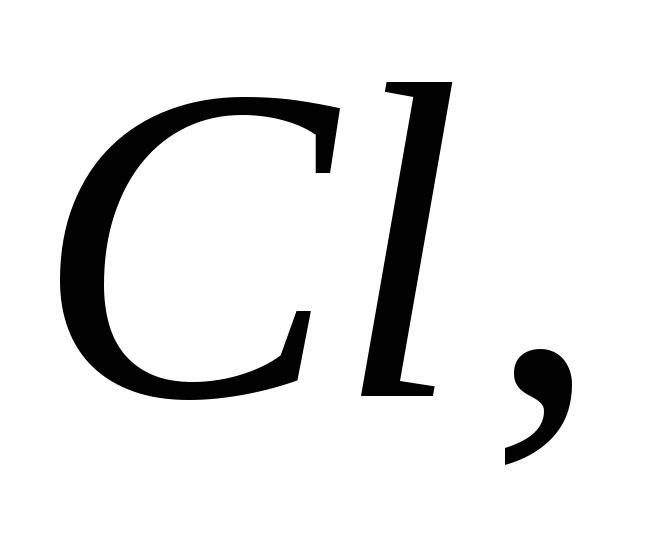
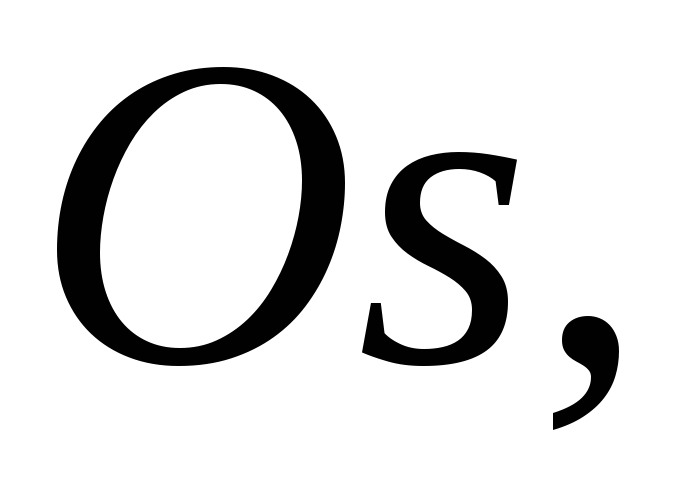 знаючи, що валентність елементу
відповідає номеру групи періодичної
системи.
знаючи, що валентність елементу
відповідає номеру групи періодичної
системи.
3.
Напишіть формули оксидів ![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() знаючи, що валентність елементу відповідає
номеру групи періодичної системи.
знаючи, що валентність елементу відповідає
номеру групи періодичної системи.
4.
Якою є валентність мангану в оксидах,
формули яких ![]()
![]()
![]()
![]()
![]() ?
?
5.
Якою є валентність нітрогену, фосфору,
силіцію, та сульфуру у сполуках, формули
яких ![]()
![]()
![]()
![]()
![]()
6. Якою є валентність
елементів у сполуках, формули яких
![]()
![]()
![]()
![]()
Знайдіть формули кислот, які мають наступний склад:
а)
![]()
![]() ,
,
![]() ;
;
б)
![]()
![]()
![]() ;
;
в)
![]()
![]()
![]() .
.
Які з наведених нижче оксидів будуть реагувати з водою за нормальних умов:
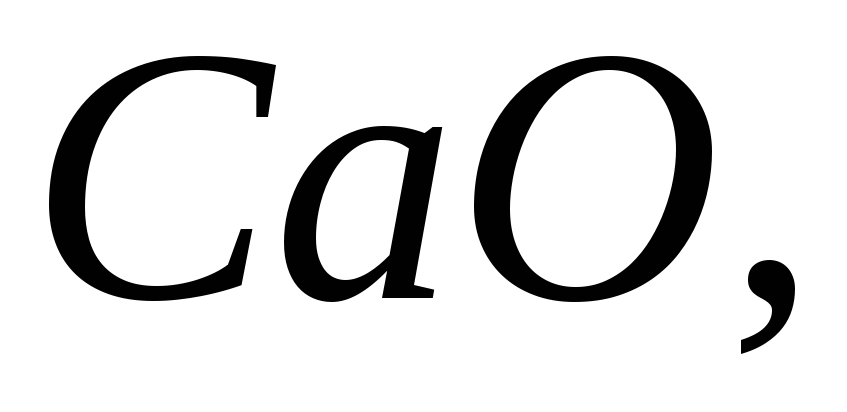
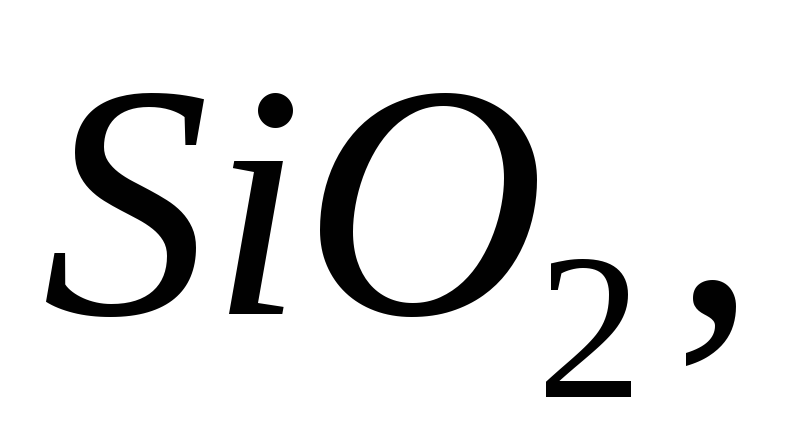
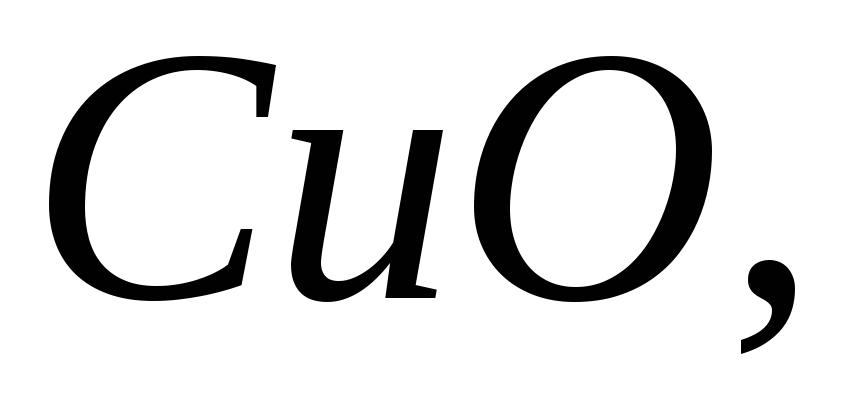
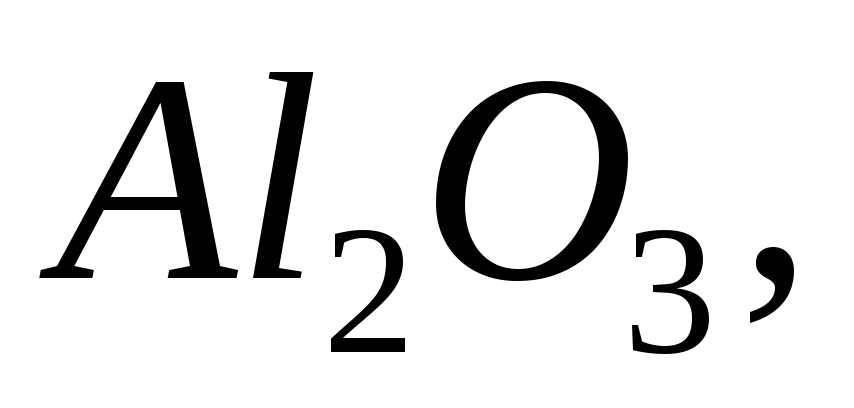


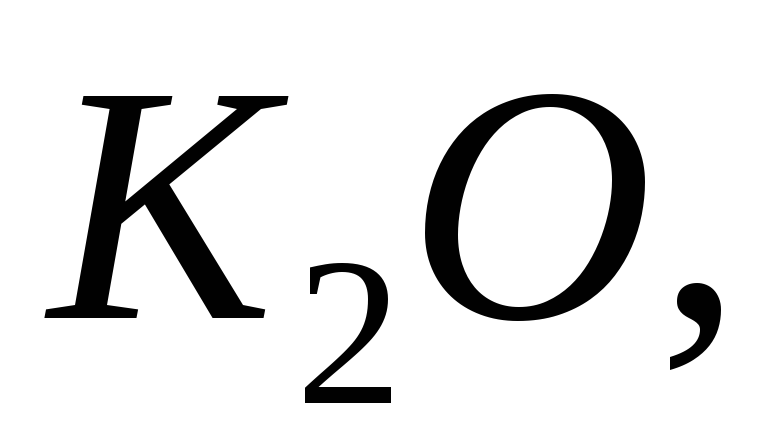

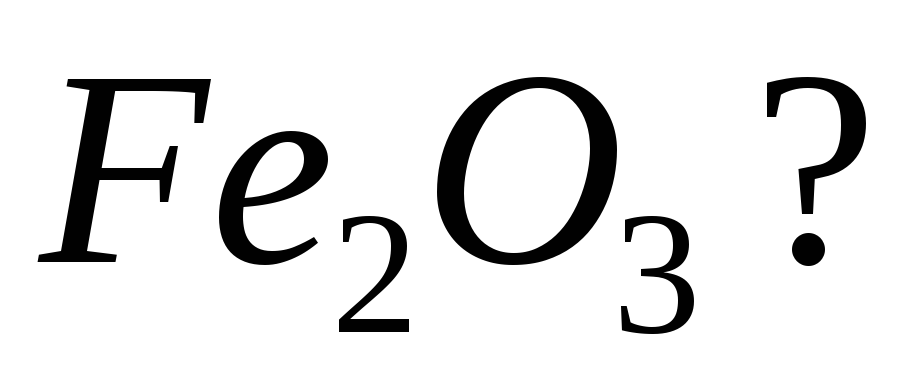 Написати рівняння реакцій.
Написати рівняння реакцій.
9.Чи можуть оксиди різних елементів реагувати друг з другом? Відповідь пояснити.
Порівняти хімічні властивості основних, кислотних та амфотерних оксидів. Навести приклади відповідних реакцій.
Напишіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення:

Напишіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення:
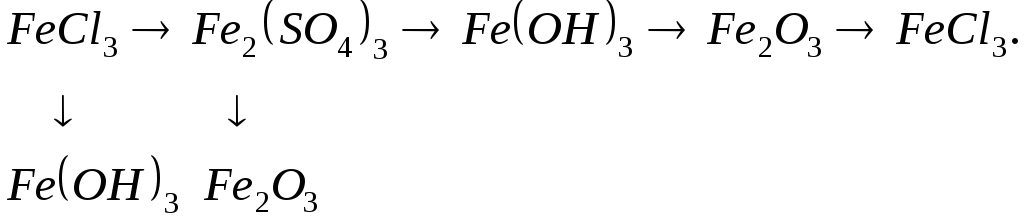
Напишіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення:
![]()
14.Цинк хлорид одержують виходячи або з цинку, або з цинк оксиду. Чим треба обробити ці речовини, щоб отримати цинк хлорид? Напишіть рівняння відпо-відних реакцій.
15.Як отримати манган(II)гідроксид, якщо ви маєте манган, кисень та воду? Напишіть рівняння реакцій. Чи можна подібним шляхом отримати купрум(II) гідроксид?
16.Розрахувати вміст заліза в 1
![]()
![]() та
та
![]() ?
?
17.Напишіть рівняння всіх можливих реакцій між такими речовинами, що взято попарно: кальцій(II) оксид, фосфор(V) оксид, хлоридна кислота, натрій гідроксид, купрум(II) оксид, калій сульфід.
18.Магній карбонат під час нагрівання
розкладається на два оксиди. Розрахувати,
яка кількість кожного оксиду утворюється
при розкладанні 210
![]() магній карбонату?
магній карбонату?
19.Цинк(II)
оксид отримують спалюванням цинкового
пилу в присутності повітря в спеціальних
ретортах. Вважаючи, що цинковий пил не
містить ніяких домішок, розрахуйте,
скільки його необхідно взяти для
одержання 40,5
![]() цинк(II) оксиду?
цинк(II) оксиду?
20.Суміш
натрій гідроксиду та кальцій(II)
гідроксиду використовують для поглинання
![]() .
На чому будується це використання?
Напишіть рівняння відповідних реакцій.
.
На чому будується це використання?
Напишіть рівняння відповідних реакцій.
2.3. Приклади рішення типових задач з теми
“Основні закони хімії”
Приклад 1. Густина газу за воднем дорівнює 14. Визначте густину цього газу за повітрям.
Розв’язання: відношення маси певного об’єму одного газу до маси такого самого об’єму іншого газу (взятого за однакових умов) називається густиною першого газу за другим (позначається літероюD):
![]()
звідки
![]() .
.
Звичайно
густину газу визначають відносно
найлегшого газу – водню (позначають
![]() ).
Молярна маса водню дорівнює 2,016
).
Молярна маса водню дорівнює 2,016
![]() .
Тому, молярна маса іншого газу буде
дорівнювати:
.
Тому, молярна маса іншого газу буде
дорівнювати:
![]() .
.
Знаючи густину за воднем, знаходимо молярну масу газу:
![]()
![]() .
.
Оскільки
молярна маса повітря заокруглено
дорівнює 29
![]() ,
густина за повітрям буде дорівнювати:
,
густина за повітрям буде дорівнювати:
![]() .
.
Відповідь: 0,966.
Приклад
2.Розрахуйте еквівалентні маси
наступних сполук:
![]()
![]()
![]()
![]()
Розв’язання: Еквівалентна маса складної сполуки розраховується за формулою:
![]() ,
,
де
![]() молекулярна маса
речовини,
молекулярна маса
речовини,
![]() ;
;
![]() кількість атомів металу;
кількість атомів металу;
![]() валентність металу.
валентність металу.
![]()
![]() ,
,
![]()
![]() ,
,
![]()
![]() ,
,
![]()
![]() .
.
Відповідь:
![]()
![]() ,
,
![]()
![]() ,
,
![]()
![]() ,
,
![]()
![]() .
.
Приклад 3. Визначити еквівалент Ме, 1 г оксиду якого при розчиненні в сульфатній кислоті дає 3 г сульфату.
Розв’язання: При розв’язанні задачі треба мати на увазі:
а)
еквівалент (еквівалентна маса) оксиду
дорівнює сумі еквівалентів (еквівалентних
мас) металу та кисню:
![]() .
.
б)
еквівалент (еквівалентна маса) солі
дорівнює сумі еквівалентів (еквівалентних
мас) металу та кислотного залишку:
![]() .
.
У відповідності з законом еквівалентів маси реагуючих речовин пропорційні їх еквівалентним масам:
![]() ;
;
![]() ;
;
![]() ;
;
![]() ;
;
![]()
![]()
Відповідь:
![]()
![]() .
.
