
- •Міністерство освіти і науки України
- •1 Програма з розділу «загальні основи аналітичної хімії»
- •Тема 1. 1 Предмет загальної, неорганічної та аналітичної хімії. Значення дисципліни для підготовки товарознавця. Найважливіші поняття та закони загальної хімії, які потрібні для вивчення курсу
- •Тема1.2 Періодичний закон та періодична система елементів
- •Тема 1.3 Сучасні теорії будови атомів та хімічного зв’язку як основа вивчення хіміко-аналітичних і фізичних властивостей сировини та матеріалів
- •Тема 1.4 Швидкість та механізм хімічних реакцій
- •Тема 1.5 Розчини та теорія електролітичної дисоціації
- •Тема 1.6 Рівновага у розчинах солей, які піддаються гідролізу
- •Тема 1.7 Рівновага у розчинах малорозчинних сполук
- •Тема 1.8 Рівновага у розчинах координаційних (комплексних) сполук
- •Тема 1.9 Рівновага при перебігу окисно-відновних реакцій (овр)
- •Тема 1.10 Систематичний аналіз катіонів та аніонів
- •Тема 1.11 Органічні аналітичні реагенти
- •Тема 1.12 Теорія та практика відбирання проби та її підготовка
- •Тема 1.13 Методи розподілу і концентрування
- •Тема 1.14 Об’ємний (титриметричний) аналіз
- •Тема 1.15 Гравіметричний (ваговий) аналіз
- •Студент повинен вміти:
- •Додаткова
- •Методичні матеріали
- •2 Приклади рішення типових задач. Питання та задачі до контрольних робіт
- •2.1 Приклади рішення типових задач з теми
- •2.2 Питання та задачі до контрольних робіт з теми
- •2.3. Приклади рішення типових задач з теми
- •2.4 Питання та задачі до контрольних робіт з теми
- •2.5 Приклади рішення типових задач з теми
- •2.6 Питання та задачі до контрольних робіт з теми
- •2.7 Приклади рішення типових задач з теми “Хімічний зв’язок”
- •2.8 Питання та задачі до контрольних робіт з теми “Хімічний зв’язок”
- •2.9 Приклади рішення типових задач з теми
- •2.10 Питання та задачі до контрольних робіт з теми
- •2.11 Приклади рішення типових задач з теми
- •2.12 Питання та задачі до контрольних робіт з теми
- •2.13 Приклади рішення типових задач з теми
- •2.14 Питання та задачі до контрольних робіт з теми
- •2.15 Приклади рішення типових задач з теми
- •2.16 Питання та задачі до контрольних робіт з теми
- •2.17 Приклади рішення типових задач з теми
- •2.18 Питання та задачі до контрольних робіт з теми
- •2.19 Приклади рішення типових задач з теми
- •2.20 Питання та задачі до контрольних робіт з теми
- •2.21 Приклади рішення типових задач з теми
- •2.22 Питання та задачі до контрольних робіт з теми
- •3. Варіанти контрольних робіт
2.19 Приклади рішення типових задач з теми
“Систематичний аналіз катіонів та аніонів”
Приклад
1. Запропонуйте хід аналізу суміші
![]() та
та
![]() .
Напишіть рівняння відповідних реакцій.
.
Напишіть рівняння відповідних реакцій.
Розв’язання:
Суміш складається з електролітів, тобто в розчині присутні аргентум(I)-катіони, плюмбум(II)-катіони та нітрат-іони. Катіони відносяться до першої аналітичної групи. Груповим реагентом на катіони першої аналітичної групи є2 н. розчин хлоридної кислоти. Тому до частини розчину, який аналізуємо, додається розчин хлоридної кислоти. Випаде білий осад аргентум та плюмбум(II) хлоридів.
![]() ,
,
![]() .
.
Осад обробляємо гарячою водою: плюмбум(II)
хлорид переходить у розчин, а аргентум
хлорид залишається в осаді. У центрифугаті
відкриваємо катіон
![]() .
Краще це зробити за допомогою калій
йодиду:
.
Краще це зробити за допомогою калій
йодиду:
![]() .
.
При наявності іону
![]() утворюється жовтий осад
утворюється жовтий осад
![]() ,
який при нагріванні розчиняється, а при
охолодженні знову випадає осад у вигляді
золотистих кристалів.
,
який при нагріванні розчиняється, а при
охолодженні знову випадає осад у вигляді
золотистих кристалів.
В осаді виявляємо катіони
![]() .
Для цього до осаду приливають по краплях
розчин амоніаку. Аргентум хлорид під
дією амоніаку переходить у розчин у
вигляді комплексного амоніакату
.
Для цього до осаду приливають по краплях
розчин амоніаку. Аргентум хлорид під
дією амоніаку переходить у розчин у
вигляді комплексного амоніакату
![]() :
:
![]() .
.
Центрифугат розділяємо на дві частини,
до однієї з них додають калій йодид, до
іншої – нітратну кислоту. При наявності
іонів
![]() у першому випадку утворюється жовтий
осад аргентум йодиду
у першому випадку утворюється жовтий
осад аргентум йодиду
![]() ,
у другому – білий осад аргентум хлориду
,
у другому – білий осад аргентум хлориду
![]() :
:
![]() ,
,
![]() .
.
Нітрат-іон відноситься до третьої аналітичної групи аніонів, яка не має групового реактву. Тому аніони цієї групи виявляють за допомогою специфічних реакцій. Для того, щоб виявити нітрат-іони в розчині до частини початкового розчину добавимо концентровану сульфатну кислоту та мідні стружки, суміш нагріємо. Виділення бурого газу нітроген(IV) оксиду буде свідчити про наявність нітрат-іонів в розчині:
![]()
Завдяки кисню повітря нітроген(II) оксид перетворюється в нітроген(IV) оксид:
![]() .
.
2.20 Питання та задачі до контрольних робіт з теми
“Систематичний аналіз катіонів та аніонів”
Предмет та задачі аналітичної хімії. Чутливість аналітичних реакцій.
Умови виконання аналітичних реакцій. Збільшення чутливості аналітичних реакцій.
Макро-, напівмікро- та мікроаналіз. Систематичний та дрібний аналіз. Наведіть приклади.
Буферні розчини. Їх властивості та значення. Протолітична рівновага в буферних розчинах. Поясніть буферну дію на прикладі
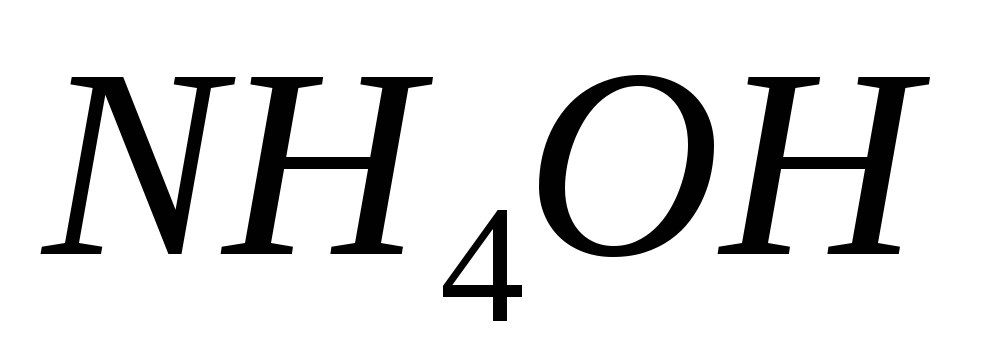 та
та
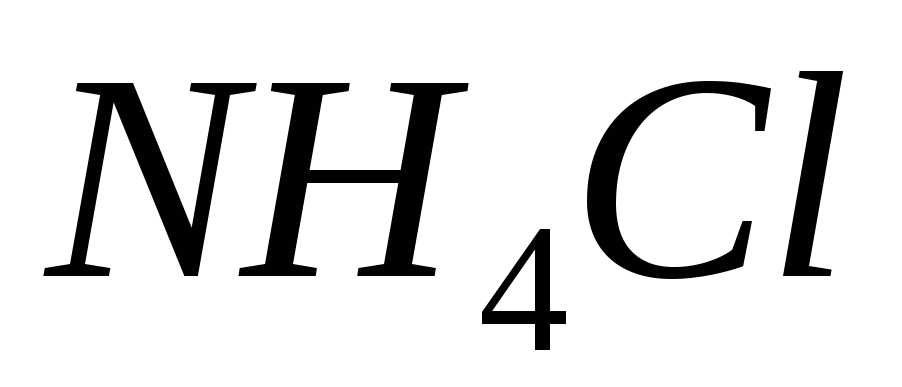 .
.Хіміко-аналітична характеристика катіонів VIаналітичної групи. Характерні реакції катіонів шостої аналітичної групи. Умови їх визначення.
Хіміко-аналітична характеристика катіонів Iаналітичної групи. Груповий реагент та умови його застосування. Як можна розділити аргентум хлорид та меркурій(I) хлорид та визначити меркурій(I)-катіони. Напишіть рівняння відповідних реакцій.
Груповий реагент на катіони IIаналітичної групи та умови його застосування. Напишіть рівняння хімічних реакцій, що дозволяють розділити та визначити барій(II)- та стронцій(II)-катіони при їх одночасній присутності в розчині.
Поясніть вибір групового реагенту на катіони III аналітичної групи та умови його застосування.Напишіть рівняння хімічних реацій взаємодії алюміній(III)- та цинк(II)-катіонів з груповим реагентом та реакції їх визначення.
Поясніть вибір групового реагенту на катіони IV аналітичної групи. Напишіть рівняння реакцій визначення ферум(II)-, ферум(III)-, магній(II)-катіонів у ході аналізу суміші катіонів цієї групи.
Класифікація аніонів по групам. Групові реагенти на аніони I, II групи. Умови їх застосування.
|
№ |
Запропонуйте хід аналізу суміші наступних речовин. Напишіть рівняння відповідних реакцій. |
|
311 |
|
|
312 |
|
|
313 |
|
|
314 |
|
|
315 |
|
