
- •1.2.Общие вопросы теории химического строения и реакционной способности органических соединений
- •1S22s22p2 или 1s22s22pх 2p y
- •2S 2Px 2Py 2Pz
- •2S 2Px 2Py 2Pz
- •Тема 2. Предельные углеводороды
- •2.3. Физические свойства предельных углеводородов
- •2.4. Химические свойства предельных углеводородов
- •2.5. Получение предельных углеводородов
- •Тема 3. Этиленовые углеводороды
- •3.1. Состояние углерода в этиленовых углеводородах, природа двойной связи
- •3.2. Изомерия, номенклатура углеводородов ряда этилена
- •3.4. Физические свойства
- •3.5. Химические свойства
- •Тема 4. Ацетиленовые углеводороды
- •4.1. Номенклатура углеводородов ряда ацетилена
- •4.2. Физические свойства ацетиленовых углеводородов
- •4.3. Способы получения
- •4.4. Химические свойства
- •Тема 5. Механизм реакций органических соединений
- •5.1. Гомолитическое и гетеролитическое расщепления
- •5.2. Факторы, определяющие реакционную способность молекулы
- •5.3. Классификация органических соединений
- •Тема 6. Ароматические углеводороды
- •6.1. Строение ароматических углеводородов
- •6.2. Номенклатура и изомерия
- •6.3. Способы получения
- •6.4. Химические свойства
- •6.5. Химические свойства гомологов бензола
- •Тема 7. Спирты
- •7.1. Номенклатура и изомерия спиртов
- •7.2. Физические свойства спиртов
- •7.3. Способы получения
- •7.4. Химические свойства
- •7.5. Многоатомные спирты
- •Тема 8. Фенолы
- •8.1. Номенклатура фенолов
- •8.2. Физические свойства
- •8.3. Способы получения
- •8.4. Химические свойства
- •Тема 9. Альдегиды. Кетоны
- •9.1. Номенклатура и изомерия
- •9.2. Способы получения
- •9.3. Физические свойства
- •9.4. Химические свойства
- •Тема 10. Органические кислоты. Амиды
- •10.1. Классификация карбоновых кислот
- •10.2. Номенклатура и изомерия
- •10.3. Способы получения
- •10.4. Физические свойства
- •10.5. Строение
- •10.6. Химические свойства
- •10.7. Амиды
- •Тема 11. Сложные эфиры
- •11.1. Номенклатура и изомерия
- •11.2. Физические свойства сложных эфиров
- •11.3. Химические свойства сложных эфиров
- •Тема 12. Жиры
- •12.1. Номенклатура и изомерия
- •12.2. Физические свойства
- •12.3. Химические свойства
- •Тема 13. Азотсодержащие органические соединения
- •13.1. Нитросоединения
- •13.2. Азотсодержащие гетероциклические соединения
- •13.3. Шестичленные гетероциклы
- •13.4. Соединения с пятичленным циклом
- •13.5. Нуклеиновые кислоты
- •13.6. Амины
- •13.7. Аминокислоты
- •13.8. Белки
- •Тема 14. Углеводы
- •14.1. Номенклатура
- •14.2. Моносахариды
- •14.3. Олигосахариды
- •14.4. Полисахариды
ДНІПРОПЕТРОВСЬКИЙ УНІВЕРСИТЕТ імені АЛЬФРЕДА НОБЕЛЯ
КАФЕДРА ТОВАРОЗНАВСТВА І ТОРГОВЕЛЬНОГО ПІДПРИЄМНИЦТВА
В.М.Орлова
"Хімія"
Опорний конспект лекцій
Частина 2
Дніпропетровськ
2012
Хімія. Опорний конспект лекцій. Частина 2 / В.М. Орлова. – Д.: Вид-во Дніпропетровський університет імені Альфреда Нобеля, 2012. – 88 с.
Укладач: В.М. Орлова, к.т.н., доцент кафедри товарознавства і торговельного підприємництва.
Затверджено на засіданні кафедри.
Протокол № 1 від 30.08.2012 р.
Відповідальна за випуск: В.А. Павлова, д.е.н., професор, зав. кафедрою товарознавства і торговельного підприємництва.
ЗМІСТ
Частина 2
Тема 1. Углеводороды и их производные 3
Тема 2. Предельные углеводороды 6
Тема 3. Этиленовые углеводороды 12
Тема 4. Ацетиленове углеводороды 25
Тема 5. Механизм реакций органических соединений 28
Тема 6. Ароматические углеводороды 34
Тема 7. Спирты 41
Тема 8. Фенолы 45
Тема 9. Альдегиды. Кетоны 48
Тема 10. Органические кислоты. Амиды 52
Тема 11. Сложные эфиры 58
Тема 12. Жиры 59
Тема 13. Азотсодержащие органические соединения 61
Тема 14. Углеводы 76
Литература 86

РАЗДЕЛ 2. ОРГАНИЧЕСКАЯ ХИМИЯ
ТЕМА 1. УГЛЕВОДОРОДЫ И ИХ ПРОИЗВОДНЫЕ
ПЛАН
1.1.Предмет органической химии
1.2.Сырьевые источники органических соединений
1.3.Общие вопросы теории химического строения и реакционной способности органических соединений
Предмет органической химии
Органическая химия изучает соединения углерода – углеводороды и их производные, в состав которых входят многие элементы периодической системы.
В состав углеводородов входят элементы углерод и водород, а производные углеводородов имеют в своем составе также: кислород, галогены, азот, серу, фосфор, металлы и другие элементы.
Выделение органической химии в самостоятельную научную дисциплину обусловлено большим количеством и многообразием соединений углерода, наличием специфических свойств, отличающих их от соединений других элементов и, наконец, их исключительным значением в жизни человека.
В настоящее время известно несколько миллионов органических соединений, в то время как соединений неорганических всего несколько десятков тысяч.
Особое значение органической химии в системе химических наук обусловлено тем, что она изучает более высоко организованную материю, чем неорганическая химии, и тесно связана с биологией. Считается, что органические вещества появились во вселенной позже, чем неорганические. Они являются носителями жизнедеятельности организмов человека, животных и растений.
Органические вещества составляют основу многих отраслей химической промышленности (пластических масс, синтетического каучука и резины, моторного топлива и смазочных материалов, растворителей, лаков, пигментов, красителей, медикаментов, взрывчатых веществ, текстильных, кожевенных и пищевых материалов) и широко используются в производстве.
На ранней стадии развития химии науки, считали, что органические вещества возникают только в живом организме под влиянием особой «жизненной силы» (научное направление – «витализм»).
В 1824 г. немецкий химик Вёлер из неорганических веществ получил щавелевую кислоту, а в 1828 г. – мочевину.
В 1842 г. русский ученых Зинин Н.Н. синтезировал анилин – краситель, который ранее получали только из растительного сырья.
В 1845 г. немецкий химик Кольбе синтезировал уксусную кислоту, а французский ученых Бертло – жиры (1854 г.).
В 1861 г. русский ученый Бутлеров А.М. синтезировал сахаристые вещества.
1.2.Общие вопросы теории химического строения и реакционной способности органических соединений
Развитие органической химии привело к созданию теории химического строения, которая было сформулирована в 1858 г. А.М. Бутлеровым (теория Бутлерова А.М.):
1.Веществам присуще химическое строение – строгий порядок в чередовании атомов в молекуле и расположении их в пространстве. Каждому химическому веществу присуще только одно определенное химическое строение.
2.Атомы в составе молекул оказывают вполне определенное влияние друг на друга (как непосредственно на соседние атомы, так и на более удаленные посредством передачи своего влияния через другие атомы – путем поляризации молекулы или через окружающее пространство – эффект поля.).
3.Химическое строение веществ определяют их химические и физические свойства.
4.На основании изучения свойств веществ можно установить их химическое строение.
5.Углерод в органических соединениях, как правило, четерехвалентен и способен, соединяясь друг с другом, образовывать длинные цепи.
6. Вещества, имеющие одинаковые качественный и количественный состав, а также молекулярную массу, могут отличаться по физическим и химических свойствам, вследствие различного химического строения. Такие вещества называются изомерами.
Изомерия, обусловленная изменением чередования атомов в молекуле называется, структурной изомерией.
Изолированный атом углерода имеет заряд ядра равный +6 (в ядре находится 6 протонов). Вокруг ядра на вполне определенных орбиталях находится 6 электронов. Таким образом атом электронейтрален. Электронная конфигурация атома углерода, описываемая квантовыми числами может быть представлена следующим образом:
1S22s22p2 или 1s22s22pх 2p y
Расположение электронов в энергетических ячейках может быть представлено следующим образом:
1S
-
↓↑
↓↑
↑
↑
2S 2Px 2Py 2Pz
Поэтому углерод должен быть двухвалентным, так как он имеет на наружном электронном уровне только два неспаренных электрона. Однако, точно установлено, что он в органических соединениях в основном четырехвалентный, что указывает на наличие в нем четырех неспаренных электронов. Это возможно, если один из электронов 2s ячейки перейдет в свободную ячейку 2pz.
1S
-
↓↑
↑
↑
↑
↑
2S 2Px 2Py 2Pz
Однако такой переход требует затраты дополнительной энергии, так как электрону с меньшей энергией необходимо перейти на орбиталь с большей энергией. Если все же такой процесс имеет место, то углерод действительно становится четырехвалентным, но одна из четырех его связей (образованная 2s – электроном) в его соединениях должна отличаться от трех других (образованных 2p – электронами), что не подтверждено проведенными исследованиями.
К настоящему времени установлено, что на самом деле атом углерода в процессе образования связи переходит предварительно в некоторое гибридное состояние. При этом один s-электрон и три р-электрона образуют четыре смешанных (гибридных) совершенно одинаковых электронных облака (одинаковой симметрии и одинаковой энергии). В процессе гибридизации на переход электронов на смешанную орбиталь затрачивается 96 ккал/моль, а выделяется в результате гибридизации 395,2 ккал/моль.
В результате атом углерода переходит в так называемое sp3– гибридное состояние (обозначается это гибридное состояние как q4).
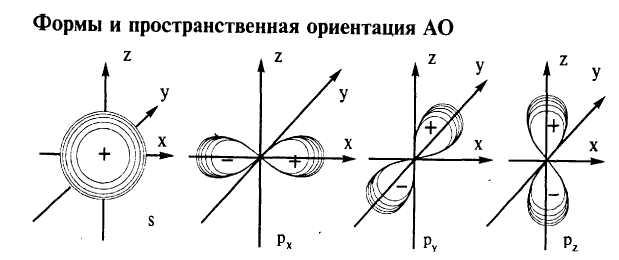
Пространственная конфигурация sp3– гибридной орбитали представлена ниже.

Пространственная конфигурация гибридизованного атома углерода представлена ниже.
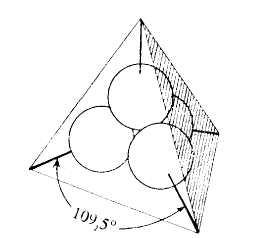
Гибридизация объясняет четырехвалентность атома углерода, равноценность всех его связей и вполне определенную ориентацию последних в пространстве. В гибридизириванном состоянии все четыре орбитали атома углерода имеют концентрацию электронного облака вдоль некоторых осей, направленных к вершинам правильного тетраэдра под углом 109028/, и цилиндрическую симметрию относительно этих осей.
