
- •Міністерство освіти і науки України
- •Лабораторна робота №1 визначення маси цинку методом витіснення
- •Класи неорганічних сполук
- •Визначення теплоти нейтралізації лугу сильною кислотою
- •Швидкість хімічної реакції. Вплив концентрацій реагуючих речовин на швидкість реакції натрій тіосульфату і сульфатної кислоти
- •Загальні властивості розчинів
- •2.Приготування розчину із наважки твердої речовини і води
- •3.Приготування розчину сульфатної кислоти з заданою масовою часткою із більш концентрованої сульфатної кислоти та води
- •Реакції в розчинах електролітів
- •1.Зміщення рівноваги в напрямку утворення малодисоційованих і газоподібних речовин
- •2.Вплив однойменних іонів на ступінь дисоціації слабкого електроліту
- •3.Утворення малорозчинних сполук
- •Кислотно-основна рівновага у водних розчинах солей. Гідроліз солей
- •1.Забарвлення кислотно-основних індикаторів у різних середовищах
- •2.Солі, утворені сильними основами й сильними кислотами
- •3.Солі, утворені сильними кислотами й слабкими основами
- •4.Солі, утворені сильними кислотами й слабкими основами
- •5.Дослідження факторів, що мають вплив на ступінь гідролізу солей
- •6.Взаємне підсилення гідролізу при взаємодії розчинів солей
- •Окисно-відновні реакції
- •1.Окисники – аніони вищих оксигеновмісних кислот
- •2.Окисники – катіони металів у вищому степені окислення
- •9.Вплив характеру середовища на проходження окисно-відновних реакцій
- •Гідроген, оксиген
- •1.Отримання водню
- •2.Отримання кисню
- •2.Отримання брому
- •3.Отримання йоду
- •4.Властивості йоду
- •5.Отримання гідроген хлориду і хлоридної кислоти
- •6.Відновні властивості галогенід-іонів
- •7.Властивості хлорної води
- •8.Властивості білильного вапна (кальцій гіпохлориту–хлориду)
- •8.Властивості калій хлорату (V)
- •9. Властивості калій іодату (V)
- •4.Отримання сульфур (IV) оксиду
- •5.Рівновага в розчині сульфітної кислоти
- •Лабораторна робота №12
- •7.Отримання нітроген (і) оксиду і його властивості
- •8.Отримання нітроген (іі) оксиду і його властивості
- •9. Нітроген (IV) оксид і його властивості
- •10.Отримання нітритної кислоти і її розклад
- •14.Відношення нітратів до нагрівання
- •15.Окисні властивості нітратів
- •1.Властивості ортофосфат-іонів
- •2.Вивчення відновних властивостей кислот і солей фосфору в нижчих ступенях окиснення
- •Карбон, силіцій
- •6.Силікатна кислота та її солі
- •1.Отримання борної кислоти
- •2.Властивості борної кислоти
- •3.Солі борних кислот
- •11. Аналітична реакція виявлення іона кальцію
- •12. Дія кислот на алюміній
- •13. Взаємодія алюмінію з лугом
- •Ферум, кобальт
- •1. Відношення заліза та кобальта до кислот
- •2. Отримання і властивості гідроксидів феруму і кобальту
- •3. Властивості солей феруму (іі)
- •Розчини. Реакції в розчинах електролітів. Гідроліз солей. Добуток розчинності. Водневий показник. Окисно-відновні реакції. Комплексні сполуки
- •Неметали
- •Варіанти завдань
- •Загальна хімія та хімія біогенних елементів Методичні вказівки до виконання лабораторних робіт та завдання для самостійної роботи для спеціальності 6.091711
Класи неорганічних сполук
Запропоновані завдання розкривають та ілюструють теоретичні знання, розвивають навички хімічного експерименту. Кожному студенту запропоновується свій варіант завдання. Перш ніж виконувати експериментальну частину роботи уважно прочитайте завдання та складіть детальний план проведення дослідів.
Реакції виконуйте в пробірках, реактиви додавайте обережно, в кількості декількох крапель. Кожну наступну реакцію виконуйте після перенесення частини реакційної суміші в іншу пробірку. Для вивчення властивостей малорозчинних сполук після утворення осадів дайте суміші відстоятися, злийте обережно розчин і розділіть осад на декілька проб. Уважно спостерігайте та фіксуйте в лабораторному журналі ефекти, які супроводжують перебіг кожного досліду. Складіть рівняння виконаних хімічних реакцій в молекулярній та йонно-молекулярній формах.
Варіант 1
1.Дослідним шляхом доведіть, в яких пробірках містяться розчини: натрій хлориду, натрій гідроксиду, хлоридної кислоти. Визначте за характерними реакціями, в якій з пробірок міститься яка речовина. Напишіть рівняння реакцій в молекулярній та іонній формах.
2.Здійсніть перетворення речовин:


![]() Б
Б
C



 u
u![]() A
A![]() В
В![]() Г
Г
![]() Д
Д
Варіант 2
1.Дослідним шляхом доведіть, в яких пробірках містяться розчини: натрій хлориду, амоній хлориду, натрій карбонату. Визначте за характерними реакціями, в якій з пробірок міститься яка речовина. Напишіть рівняння реакцій в молекулярній та іонній формах.
2.Здійсніть перетворення речовин:
мідь ® купрум (ІІ) оксид ® купрум (ІІ) хлорид ® купрум (ІІ) гідроксид ® купрум (ІІ) сульфат ® купрум (ІІ) хлорид ® аргентум хлорид.
Варіант 3
1.Дослідним шляхом доведіть, в яких пробірках містяться розчини: ферум (ІІ) сульфат, алюміній сульфат, ферум (ІІІ) хлорид. Визначте за характерними реакціями, в якій з пробірок міститься яка речовина. Напишіть рівняння реакцій в молекулярній та іонній формах.
2.Здійсніть перетворення речовин:
залізо ® ферум (ІІ) хлорид ® ферум (ІІ) гідроксид ® ферум (ІІІ) гідроксид® ферум (ІІІ) оксид ® ферум (ІІІ) сульфат ® ферум (ІІІ) хлорид.
Варіант 4
1.Дослідним шляхом доведіть, в яких пробірках містяться кристалічні солі: натрій сульфат, натрій хлорид, натрій йодид. Визначте за характерними реакціями, в якій з пробірок міститься яка речовина. Напишіть рівняння реакцій в молекулярній та іонній формах.
2.Здійсніть перетворення речовин:
 цинк
сульфат®цинк
хлорид
цинк
сульфат®цинк
хлорид
цинк®цинк хлорид®цинк гідроксид
 натрій
тетрагідроксосульфат
натрій
тетрагідроксосульфат
Варіант 5
1.Дослідним шляхом доведіть, в яких пробірках містяться розчини солей: натрій сульфат, натрій сульфід, натрій сульфіт. Визначте за характерними реакціями, в якій з пробірок міститься яка речовина. Напишіть рівняння реакцій в молекулярній та іонній формах.
2.Здійсніть перетворення речовин:
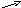 Na[Pb(OH)4]
Na[Pb(OH)4]
Pb ® Pb(NO3)2 ® Pb(OH)2

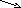 Pb(NO3)2
Pb(NO3)2![]() А
А
+Al ¯
Б
Варіант 6
1.Дослідним шляхом доведіть, в яких пробірках містяться розчини : нітратної кислоти, натрій гідроксиду, сульфатної кислоти.Визначте за характерними реакціями, в якій з пробірок міститься яка речовина. Напишіть рівняння реакцій в молекулярній та іонній формах.
2.Здійсніть перетворення речовин:


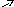
 AlCl3
®
AgCl
Al(NO3)3
AlCl3
®
AgCl
Al(NO3)3
A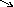 l®
Al2(SO4)3
®
Al(OH)
l®
Al2(SO4)3
®
Al(OH)
Na[Al(OH)4]
ЛАБОРАТОРНА РОБОТА №3
