
- •2. Марганец и его соединения. Биологическая роль.
- •3. Железо и его соединения. Биологическая роль.
- •4. Ионное произведение воды. Водородный показатель.
- •5. Силы Ван-дер-Вальса.
- •7. Упругость пара над раствором. Законы Рауля.
- •9. Ионная связь.
- •11. Кислородосодержащие кислоты хлора. Соли этих кислот. Биологическая роль.
- •12. Координационная теория Вернера.
- •13. Классификация и изомерия комплексных соединений.
- •15. Кислородосодержащие кислоты серы. Соли этих кислот.
- •16. Понятие о квантовой механике.
- •17. Многоэлектонные атомы и периодический закон.
- •18. Окисли азота.
- •19. Окислительно-восстановительные реакции.
- •20. Аммиак и его свойства.
- •21. Водородные соединения галогенов. 22. Галогеноводородные кислоты.
- •23. Метод молекулярных орбиталей.
- •25. Константа и степень электролитической диссоциации.
- •26. Азотная кислота и ее соли.
- •27. Гибридизация атомных орбиталей.
- •29. Периодичность изменения свойств элементов и их соединений.
- •30. Гидролиз.
- •32. Благородные газы.
- •35. Металлическая связь.
- •38. Современная химическая атомистика.
- •39. Осмос. Осмотическое давление. Закон Вант Гоффа.
- •41. Теория Бора.
- •43. Скорость химических реакций. Химическое равновесие.
- •44. Понятие об активном комплексе и энергии активации.
- •45. Серная кислота
- •46. Растворы. Растворимость как физико-химический прочес (гидратная теория, теория Менделеева).
20. Аммиак и его свойства.
Летучим характеристическим водородным соединением азота является аммиак,самое важное водородное соединение азота. По своей химической природе он представляет собой нитрид водорода H3N. В химическом строении аммиакаsp3-гибридные орбитали атома азота образуют три σ-связи с тремя атомами водорода, которые занимают три вершины чуть искаженного тетраэдра.Четвертая вершина тетраэдра занята неподеленной электронной парой азота, что обеспечивает химическую ненасыщенность и реакционноспособность молекул аммиака, а также большую величину электрического момента диполя.При н.у. бесцветный газ с резким запахом.
Получение:пром:N2+3H2=2NH3,лаб:NH4Cl+NaOH=NH3+NaCl+H2O/РеакцииNH3+HOH⇄NH4OH\ 4NH3+ 3O2 → 2N2↑ + 6H2O\NH3+HCl⇄NH4Cl\NH3+H3PO4 → (NH4)3PO4 Аммиак взаимодействует с солями некоторых металлов с образованием комплексных соединений – аммиакатов:CuSO4+ 4NH3→ [Cu(NH3)4]SO4 сульфат тетрааммин меди (II),AgCl+ 2NH3→ [Ag(NH3)2]Clхлорид диаммин серебра (I).Аммиак восстанавливает некоторые металлы из их оксидов:2NH3+ 3CuO→N2↑ +3Cu+3H2OОн токсичен: раздражает слизистые оболочки, а острое отравление вызывает поражение глаз и воспаление легких. Вследствие полярности молекул и достаточно высокой диэлектрической проницаемости жидкий аммиак является хорошим растворителем. В жидком аммиаке хорошо растворяются щелочные и щелочно-земельные металлы, сера, фосфор, йод, многие соли и кислоты. По растворимости в воде аммиак превосходит любой другой газ. Этот раствор называется аммиачной водой, или нашатырным спиртом. Прекрасная растворимость аммиака в воде обусловлена возникновением межмолекулярных водородных связей.
21. Водородные соединения галогенов. 22. Галогеноводородные кислоты.
Галогеноводороды — бесцветные газы, с резким запахом, легко растворимы в воде.. Фтороводород смешивается с водой в любых соотношениях. Высокая растворимость этих соединений в воде позволяет получать концентрированные растворы.
При растворении в воде галогеноводороды диссоциируют по типу кислот. HF относится к слабо диссоциированным соединениям, что объясняется особой прочностью связи. Остальные же растворы галогеноводородов относятся к числу сильных кислот. HF — фтороводородная (плавиковая) кислота НСl— хлороводородная (соляная) кислота HBr — бромоводородная кислота HI — иодоводородная кислота
Сила кислот в ряду HF — НСl — HBr — HI возрастает, что объясняется уменьшением в том же направлении энергии связи и увеличением межъядерного расстояния. HI — самая сильная кислота из ряда галогеноводородных кислот.
Поляризуемость растет вследствие того, что вода поляризует больше ту связь, чья длина больше. Соли галогеноводородных кислот носят соответственно следующие названия: фториды, хлориды, бромиды, иодиды.
Химические свойства галогеноводородных кислот
В сухом виде галогеноводороды не действуют на большинство металлов.
1. Водные растворы галогеноводородов обладают свойствами бескислородных кислот. Энергично взаимодействуют со многими металлами, их оксидами и гидроксидами; на металлы, стоящие в электрохимическом ряду напряжений металлов после водорода, не действуют. Взаимодействуют с некоторыми солями и газами.
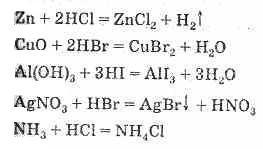
Фтороводородная кислота разрушает стекло и силикаты:
SiO2+4HF=SiF4+2Н2O
Поэтому она не может храниться в стеклянной посуде.
2. В окислительно-восстановительных реакциях галогеноводородные кислоты ведут себя как восстановители, причем восстановительная активность в ряду Сl-, Br-, I- повышается.

Получение
Фтороводород получают действием концентрированной серной кислоты на плавиковый шпат:
CaF2+H2SO4=CaSO4+2HF
Хлороводород получают непосредственным взаимодействием водорода с хлором:
Н2+Сl2=2НСl
Это синтетический способ получения.
Сульфатный способ основан на реакции концентрированной серной кислоты с NaCl.
При небольшом нагревании реакция протекает с образованием НСl и NaHSO4.
NaCl+H2SO4=NaHSO4+HCl
При более высокой температуре протекает вторая стадия реакции:
NaCl+NaHSO4=Na2SO4+HCl
Но аналогичным способом нельзя получить HBr и HI, т.к. их соединения с металлами при взаимодействии с концентрировавной серной кислотой окисляются, т.к. I- и Br- являются сильными восстановителями.
2NaBr-1+2H2S+6O4(к)=Br02+S+4O2+Na2SO4+2Н2O
Бромоводород и иодоводород получают гидролизом PBr3 и PI3: PBr3+3Н2O=3HBr+Н3PO3 PI3+3Н2О=3HI+Н3РO3
