
- •Конспект лекцій з курсу
- •Лекція № 1. Значення курсу та його роль у становленні інженера хіміка-технолога.
- •Лекція № 2. Енергетико-магістральний напрямок соціально-економічного розвитку суспільства.
- •Лекція № 3
- •Лекція № 4
- •Лекція 11 ступінь термодинамічної досконалості технічних процесів
- •Лекція № 12. Розрахунок ексергії
- •Лекція № 13. Методика розрахунку ексергії
- •Лекція № 14. Основні положення термодинамічного аналізу хімічних процесів
- •Лекція № 15 процеси горіння рідкого і газоподібного палива. Ексергетичний і термічний ккд.
- •Лекція № 6. Другий закон термодинаміки
- •Лекція 8 процеси зміни стану газа
- •Лекція 9 поняття максимального коефіцієнта корисної дії
- •Лекція 10 ексергетичний метод термодинамічного аналізу
- •Лекція № 12. Розрахунок ексергії
- •Лекція № 13. Методика розрахунку ексергії
- •Лекція № 14. Основні положення термодинамічного аналізу хімічних процесів
- •Лекція № 15 процеси горіння рідкого і газоподібного палива. Ексергетичний і термічний ккд.
- •Термодинамічний аналіз теплообмінних процесів
- •Лекція № 18 вторинні енергетичні ресурси (вер) і способи утилізації теплоти технологічних виробництв.
Термодинамічний аналіз теплообмінних процесів
Процеси теплообміну є неминучою стадією будь-якого хімічного процесу, зв'язаного з нагріванням або охолодженням продуктів реакції. Від правильної організації цих процесів сильно залежать видаткові коефіцієнти, тому аналізові теплообміну присвячене велике число робіт /23, с.209-221; 24, с.31-48; 25, с.122-151/.
При розгляді процесів теплообміну з позицій першого закону термодинаміки до втрат тепла відносять в основному тепло, що відводиться в навколишнє середовище через неповну його рекуперацію. Однак, якщо теплообмінник розміщається усередині технологічного ланцюжка, те нецілком рекупероване тепло (або холод) приділяється не в навколишнє середовище, а корисно використовується. Тоді енергетичні втрати зводяться в основному до втрат у навколишнє середовище, що залежить від якості теплової ізоляції, і до втрат, що залежать від гідравлічного опору теплообмінника. Якщо цими втратами можна зневажити, то тепловий ККД процесу дорівнює 1. Однак, як відомо, втрати ексергії навіть в ідеально ізольованому теплообміннику з нульовим гідравлічним опором не дорівнюють нулеві. Необхідною, але, як буде показано, далеко не достатньою умовою ревності нулеві втрат ексергії є нескінченно велика поверхня теплообміну.
Як найпростіший приклад можна привести процес теплообміну (мал. 1а) двох потоків, рідини або газу, що мають однакову середню теплоємність Ср, один із яких нагрівається від температури Т1 до температури Т3 потоком рідини або газу, охолоджуваного при цьому від температури Т2 до температури Т4. Теплові втрати прийняті рівними нулеві. Кількість потоків G однакові. Отже, кількість переданого тепла дорівнює
H=GCp(T3-T1)= GCp(T2-T4)=kT zTTT (1)
де kT - відповідно коефіцієнти і поверхня теплопередачі.
Отже, рушійна сила теплообміну TT у будь-якій точці теплообмінника постійна
TT = Tгор=T2-T3=Тхол=T4-T1 (2)
Термічна ексергія кожного потоку дорівнює
Еi=GCp[(Ti-T0)- T0ln(Ti/T0)] (3)
У загальному випадку досить, щоб G1Cp1= G2Cp2= GCp де індекс = 1, 2, 3, 4 відноситься до крапок на мал.1а
T
2 4
3
1
4
2
1
3
2
4
3 1
2
4
3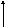
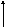
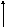
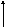 T
T T
T
T T
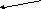

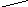
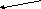


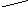


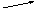




O H 1 O H 1 O H 1 O H 1
Мал.1. Температури потоків при нагріванні й охолодженні робочих тіл (а, в, г) і випарі чистої рідини за рахунок тепла чистої пари, що конденсується, (б):
а - при G1Cp1= G2Cp2;
у - при G1Cp1< G2Cp2;
м - при G1Cp1> G2Cp2
(Н - частка тепла, передана холодному потокові)
Отже, у ході теплообміну ексергія змінюється на величин
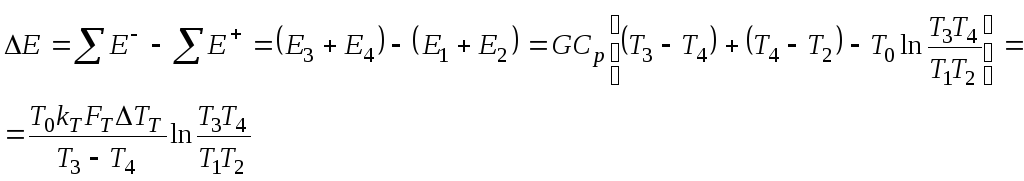 (4)
(4)
При Т3=Т2 (і, отже, Т4=Т1), тобто при нескінченній поверхні теплообміну, величина E=0. Якщо ж TT0 і оскільки завжди T3>T1. T2/T4=(T3+TT)/(T1++TT)<T3/T1 то 1< T2/T4 < T3/T1. Отже, (T3T4)/(T1T2)>1 і E<0 (ексергія губиться). Це справедливо у всіх випадках і при T>T0 і при T<T0 .
Іншим простим і розповсюдженим випадком теплообміну (мал.1б) є випар чистої рідини при Т1 за рахунок тепла конденсації пари при температурі Т2. Це можуть бути пари або тієї ж речовини при більш високому тиску, або іншої речовини. У цьому випадку, якщо G1= G2, то H1=H2.
Далі
E=-T0S=-T0G[ (S3+S4)- (S1-S2)] -T0[ (S3-S1)- (S2-S4)]=
=-T0G[(H3-H1)/T1-(H2-H4)/T2] =-T0GH(1/T1-1/T2) (5)
Оскільки T2<T1, то E<0. Чим більше різниця Т2-Т1, тим вище втрати ексергії.
Однак часто приходиться рекуперувати тепло газів і рідин, що мають неоднакову теплоємність або при неоднакових кількостях охолоджуваного потоку і потоку, що нагрівається, (мал.1в) і (мал.1г). У цих випадках кількість переданого тепла буде складати
H=G1C1(T3-T1)= G2C2(T2-T4) (6)
У практиці хімічної технології поширені й інші випадки теплообміну. Так, часто при рекуперації тепла хімічних реакцій гарячий газ використовується для виробництва водяної пари (мал.2). У цьому випадку неминуча висока різниця температур Tгор.= T2-T3 на гарячому кінці теплообмінника. При цьому, чим повніше використовується потенціал теплоносія, тим більше втрати потенціалу на гарячому кінці. Так, з мал.2а видно,
2
7
4
3
1
2
7
3
1
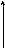
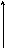









 T
T
T
T
O H4 H6 1 O H4 H6 1
Мал.2. Зміна температури при одержанні пари за рахунок тепла гарячого газу або рідини при найпростішій схемі (а) і при ступінчастому награванні.
що якщо збільшити температуру пари, отримуваної в котлі-утилізаторі з Т3 до Т7, то при нескінченно великій поверхні теплообміну, тобто при Tхол.0, кількість тепла, корисно використовуваного в котлі-утилізаторі, зменшиться на величинуH=H6-H4.Звідси випливає природний висновок, що більш раціональним є ступінчасте нагрівання з одержанням пари різних параметрів: спочатку низьких, тобто при температурі Т3 (див.мал.2б), а потім при температурі Т7. Така схема дозволяє більш повно використовувати тепло й ексергію теплоносія. При цьому втрати ексергії зменшуються на величину
E = -T0H(1/T7-1/T3) = -T0GC(T2-T7) (1/T7-1/T3) (6)
На мал.3 показаний ще один розповсюджений випадок неминучої необоротності при теплообміні: нагрівання газу або рідини парою, що конденсується. У цьому випадку при Tгор.=T2-T30 завжди Tхол.=T4-T1>0. У цёй ситуації для зменшення втрат ексергії використовується ступінчасте нагрівання різними теплоносіями.
У подібних випадках можливі й інші технічні рішення. Так, у промисловості реалізований спосіб (а.с. СРСР № 345716), по якому рекуперацію тепла гарячого регенерованого абсорбенту при очищенні газів від CO2 за схемою, показаною раніше, ведуть шляхом нагрівання меншої кількості насиченого абсорбенту (див.мал.2в) з одночасною десорбцією з нього CO2. Це дозволяє зменшити розходження мёж ∆Тгар. і ∆Тхол. ("перекіс" температур), наблизивши процес до режиму, показаного раніше.
2
3
1
T
4


O H 1
Мал.3. Зміна температури при нагріванні газу або рідини парами, що конденсуються
Часто теплообмін здійснюється при прямому контакті, тобто при змішанні потоків, що нагрівається й охолоджуваного (мал.4). До таких процесів можна віднести процеси сатурації газу парами рідин, сушіння речовин
G ,Cp,T1,E1
,Cp,T1,E1

2G,Cp,T3,E3

G ,Cp,T2,E2
,Cp,T2,E2
Мал.4. Схема теплообміну при змішанні потоків
шляхом нагрівання гарячими топковими газами, абсорбцією гарячих газів холодними рідинами (і навпаки), коли поряд з абсорбцією протікають процеси теплопередачі й ін. Тоді також губиться ексергія (при незмінній ентальпії). Неважко переконатися, що в розглянутому випадку втрати рівні
E=E3-(E1+E3)=-GCpT0[2ln(T1+T2)/2T0-ln(T1/T0)-ln(T2/T0)]=
![]() (7)
(7)
Величина Т![]() (Т1Т2)
завжди >1,
тому
∆E<0.
Дійсно, прийнявши ∆T=(T1T2)>0,
одержимо
(Т1Т2)
завжди >1,
тому
∆E<0.
Дійсно, прийнявши ∆T=(T1T2)>0,
одержимо
Т![]() (Т1Т2)
= (Т1+
Т2)2/(4
Т1
Т2)=1/4(Т1
/ Т1+
Т2
/ Т1)+
½ =
(Т1Т2)
= (Т1+
Т2)2/(4
Т1
Т2)=1/4(Т1
/ Т1+
Т2
/ Т1)+
½ =
=¼ [(Т2 - DТ1)/ Т2+( Т1+DТ)/ Т1]+1/2 = 1 =DТ/4(1/Т1 1/Т2-)0
Критерієм ступеня досконалості процесу може бути зниження питомих втрат ексергії, хоча більш загальним параметром є ексергетичний ККД. Для процесів теплообміну величину ККД можна визначати з рівняння
![]() (8)
(8)
У чисельнику
рівняння стоїть величина
![]() ,
що дорівнює приростові термічної
ексергії потоку, що нагрівається, (якщо
T>T0).
Крім того, у чисельник може входити
величина
,
що дорівнює приростові термічної
ексергії потоку, що нагрівається, (якщо
T>T0).
Крім того, у чисельник може входити
величина
![]() - збільшення хімічної ексергії за умови,
що нагрів супроводжується хімічним
перетворенням. У знаменнику крім
основного параметра -
- збільшення хімічної ексергії за умови,
що нагрів супроводжується хімічним
перетворенням. У знаменнику крім
основного параметра -![]() -
втрати термічної ексергії охолоджуваного
потоку при T>T0
або потоку, що нагрівається, при T>T0
входять
значення
-
втрати термічної ексергії охолоджуваного
потоку при T>T0
або потоку, що нагрівається, при T>T0
входять
значення
![]() і
і
![]() - втрати ексергії тиску потоків, що
залежать вёд гідравлічного опору
апарата.
- втрати ексергії тиску потоків, що
залежать вёд гідравлічного опору
апарата.
ККД процесів теплообміну сильно залежить від зовнішніх втрат ексергії, тобто від того, чи використовується чи ні низькопотенційне тепло (або холод) потоків, виведених з теплообмінника (у розглянутих прикладах тепло при температурі Т4). У сучасних енерготехнологічних схемах це тепло часто використовується. Так, наприклад, тепло, що відводиться в холодильнику і конденсаторі в процесі очищення газу, може використовуватися для підігріву води, що направляється для одержання пари. У такій схемі може існувати термодинамічно оптимальний режим рекуперації тепла.
Відомий класичний приклад оптимізації заснований на зіставленні енергетичних витрат, що знижуються зі зменшенням недорекуперації при холодному (у даному випадку) кінці теплообмінника і зростаючих при цьому капітальних витратах на теплообмінник.
