
- •Конспект лекцій з курсу
- •Лекція № 1. Значення курсу та його роль у становленні інженера хіміка-технолога.
- •Лекція № 2. Енергетико-магістральний напрямок соціально-економічного розвитку суспільства.
- •Лекція № 3
- •Лекція № 4
- •Лекція 11 ступінь термодинамічної досконалості технічних процесів
- •Лекція № 12. Розрахунок ексергії
- •Лекція № 13. Методика розрахунку ексергії
- •Лекція № 14. Основні положення термодинамічного аналізу хімічних процесів
- •Лекція № 15 процеси горіння рідкого і газоподібного палива. Ексергетичний і термічний ккд.
- •Лекція № 6. Другий закон термодинаміки
- •Лекція 8 процеси зміни стану газа
- •Лекція 9 поняття максимального коефіцієнта корисної дії
- •Лекція 10 ексергетичний метод термодинамічного аналізу
- •Лекція № 12. Розрахунок ексергії
- •Лекція № 13. Методика розрахунку ексергії
- •Лекція № 14. Основні положення термодинамічного аналізу хімічних процесів
- •Лекція № 15 процеси горіння рідкого і газоподібного палива. Ексергетичний і термічний ккд.
- •Термодинамічний аналіз теплообмінних процесів
- •Лекція № 18 вторинні енергетичні ресурси (вер) і способи утилізації теплоти технологічних виробництв.
Лекція № 4
ЕНЕРГЕТИКА І НАВКОЛИШНЄ
СЕРЕДОВИЩЕ
|
4.1 |
Поняття енергії й енергетики |
|
|
4.2 |
Форми енергії і їхня загальна характеристика |
|
|
4.3 |
Поняття теплоти. Характеристика процесу горіння органічного палива. Ядерна енергетика. |
|
|
4.4 |
Вплив продуктів горіння на навколишнє середовище, методи боротьби з ними. |
|
4.1. Енергія - загальна міра різних форм руху матерії. У тепловій енергії виявляється швидкий неупорядкований рух атомів і молекул: у формі електричної енергії - рух електронів або розподіл електричного заряду в просторі: механічна енергія являє собою енергію заряду тіла, що рухається; хімічна енергія зв'язана з хімічною структурою речовини; ядерна (атомна) енергія - з визначеною будівлею і складом атомного ядра і т.д. Якісно різні форми енергії можуть взаємно перетворюватися одна в іншу в строго визначених співвідношеннях, причому щораз строго дотримується закон збереження енергії. Відповідно до цього закону, повна енергія ізольованої системи постійна і не залежить від змін, що відбуваються в ній.
Оскільки частина енергії може бути перетворена в роботу, енергію можна розглядати як здатність зробити роботу. Тоді енергія визначає кількість "схованої роботи" і служить мірою усіляких фізичних змін. Абсолютну величину енергії не можна установити зовсім точно, і найчастіше говорять про збільшення енергії або збиток енергії системи відповідно до величини прикладеної до системи і зробленої нею роботи.
Під енергетикою в широкому змісті слова ми розуміємо галузь народного господарства, що займається одержанням, перетворенням, доставкою і використанням усіх видів енергії. У більш вузькому змісті, в енергетику не включають видобуток, доставку і переробку органічних палив. У такому розумінні вона розділяється по видах енергії: на електроенергетику, теплоенергетику, газову енергетику, гідроенергетику, атомну енергетику і т.д.
Енергетика складає одну з фундаментальних основ розвитку економіки сучасного людського суспільства. Її станом значною мірою визначаються темпи наукового і технічного прогресу, інтенсифікація суспільного виробництва, підвищення його технічного рівня і поліпшення умов праці.
4.2. Існує кілька форм енергії ( теплова, електрична, водна, сонячна, приливна, геотермальна, атомна, термоядерна, вітрова, хімічна ).
Усі ці форми енергії можна звести до двох видів: до енергії положення (потенційна) і енергії руху (кінетична). Механічна потенційна енергія зв'язана з положенням матеріальної точки (або тіла) у гравітаційному полі. Її мірою служить робота, що тіло може зробити при переході з даного положення в положення, прийняте за нульове. Кінетична енергія зв'язана зі станом руху тіла і виміряється максимальною величиною роботи, що тіло, що рухається, може зробити до своєї повної зупинки.
Якщо система переходить зі стану спокою в рух або навпаки, причому вона не робить ніякої роботи, то сума обох видів енергії (потенційній і кінетичної) у системі залишається постійною. Будь-які енергетичні процеси, що можуть викликати інтерес, зводяться до перетворення однієї форми енергії в іншу, котре протікає в строгому підпорядкуванні законові збереження енергії. Найчастіше ми використовуємо енергію в електричній, тепловій, хімічній і механічній формах. В даний час до цих форм додається атомна, а в перспективі - і термоядерна енергія. У кожнім процесі одержання енергії беруть участь паливо (її первинний носій), процес перетворення й енергетичний продукт: наприклад, у двигуні внутрішнього згоряння це бензин (разом з повітрям), спалювання і рух поршня.
Теплова енергія зв'язана з горінням органічного палива. Горіння є хімічний процес, при якому частини палаючої речовини з'єднуються з киснем.
Енергія води, що рухається. Ріки і хвилі океану, припливи, відливи.
Вітрова енергія - рух потоків повітряних мас. Середня потужність вітру на Землі - понад 44 трлн. кВт, тобто, у 500 разів більше, ніж споживання енергії.
Геотермальна енергія - магма Землі. Приблизно 50 м глибини дають ріст температури на 1о. Це значить, що на глибині близько 3 км кипить вода, на 11 км - плавиться свинець (327оС), на двадцятому - алюміній (659оС), а на глибині 60 км температура досягає 1800о С і плавиться навіть платина (1773оС).
Існують дві гіпотези походження тепла Землі. Одна стоїть на тім, що це тепло отримане в момент її зародження. Інша вважає, що ймовірними джерелами тепла є: падаюче на поверхню сонячне випромінювання, енергія розпаду деяких радіоактивних елементів, енергія сейсмічних хвиль, що поглинаються, енергія обертання Землі, тепло, що виділяється при стиску нижче лежачих шарів під тиском вище лежачих, що перетворюється в тепло, енергія падаючих на Землю метеоритів. Питомий тепловий потік з середини Землі до її поверхні складає близько 5*10-2 ТДж/м2с. Полный тепловой поток с учётом общей поверхности Земли составит 26 ТДж/с. Повний тепловий потік з урахуванням загальної поверхні Землі складе 26 ТДж/с. Це означає, що планета з початку нашого літочислення повинна була втратити близько 1,6*1012 ТДж тепла. Ця цифра в 10 разів перевищує енергію, яку можна було б залучити з усіх пропонованих запасів викопного палива.
Сонячна енергія - випромінювання планети Сонце, енергія, що приходиться на поверхню Землі.
Сонце за 3 дні посилає стільки енергії на Землю, скільки її знаходиться в розвіданих запасах органічного палива
За 1 с. - 170 млрд. Дж.
Ядерна енергія - розпад атомних ядер. Збиток 1 г маси ядра еквівалентний спалюванню 300 вагонів кам'яного вугілля.
Термоядерна енергія - виходить при термоядерній реакції. Злиття ядер легких елементів. 4 водневі ядра поєднуються в одне ядро атома гелію, що на 0,7% легше всіх чотирьох вихідних ядер водню. Плазма.
С + 02 = 12 кг + 32 кг = 44 кг. Масі речовини в 1 г відповідає енергія 0,000004 г. Теорія відносності Ейнштейна.
21,5 млрд. ккал. ( А.Проценко. Энергия будущего. М.: Молодая гвардия, 1985, 222с., ил.).
4.3. Теплота являє собою визначений вид енергії і тому можливий перехід між двома дотичними системами з різною температурою. Те, що ми називаємо теплотою, є кінетична енергія молекул. Енергія руху.
Оскільки теплота є вид енергії, її виражають в одиницях роботи. У системі СІ основною одиницею теплоти служить джоуль (Дж). При теплових вимірах як зразкову речовину часто використовують воду, і тому ще вживають третю одиницю кількості тепла - кілокалорію (ккал).
1 ккал = 4186,8 Дж
Повільне і швидке горіння. Вибух. Схема розподілу температур полум'я.
2С + О2 → 2СО
2СО + О2 → 2СО2
Самозаймистість палива.
Гіпотеза Лавуазьє швидко одержала загальне визнання: "горіння є хімічний процес, при якому частини палаючої речовини з'єднуються з киснем".
Незабаром виявилося, що процеси з'єднання з хлором, сіркою, бромом і іншими, так називаними, кислотоутворюючими елементами в багатьох відносинах дуже схожі на процес з'єднання з киснем. Сучасна атомна теорія пояснила і головні принципи, що лежать в основі хімічних процесів. Так установлено, що з окислюванням подібні всі реакції, у яких атоми або молекули втрачають негативний заряд. Тому сьогодні окислюванням прийнято називати будь-як процес з'єднання з киснем або іншим елементом, що приєднує електрони. Коли якась речовина в системі окисляється, то інша речовина в тій же системі відновлюється. Окислювання і відновлення - взаємозалежні хімічні перетворення. Речовина, здатна приєднати електрони, називається окисним реагентом, а речовина, здатна віддавати електрони, - відбудовним реагентом.
Основним джерелом енергії донині служать хімічні реакції горіння палива і при звичайних вибухах. У хімічних реакціях змінюються тільки зовнішні оболонки атомів, а ядра залишаються незмінними. Щоб вивільнилася хімічна енергія деревини, вугілля, нафти або іншого палива, це паливо необхідно запалити, іншими словами, викликати в ньому хімічні реакції, при яких змінюються електронні оболонки атомів.
Горіння вугілля С + О2 → СО2. При утворенні молекули СО2 електрони в оболонці атома вуглецю й обох атомах кисню зміщаються трохи ближче до ядер. Оболонки атомів перебудовуються так, що обсяг молекул виявляється менше, ніж сумарний обсяг трьох окремих, що ввійшли в неї атомів. "Стиснуті" електронні оболонки втрачають свою стійкість і здобувають її знову тільки тоді, коли випромінюють у навколишній простір фотони - кванти тепла і світла: вогонь світить і гріє. Фотони несуть з атомів частину маси разом з енергією, що атоми втратили при "перегрупуванні" електронів в оболонках. Подібно вуглецеві деревини або вугілля в печі, але трохи швидше, згоряє бензин або дизельне паливо в циліндрах двигунів внутрішнього згоряння. Від згоряння речовини залишається вже один крок до вибуху. По суті, вибух не що інше, як дуже швидке горіння.
Енергія, що виділяється у виді тепла і світла, утримується у вихідних речовинах у формі хімічної енергії, тобто енергії хімічних зв'язків.
Теоретично можна було б у відповідному пристрої перетворювати в корисну роботу велику частину хімічної енергії, якщо виключити проміжне перетворення її в теплоту. На сучасному етапі ми вміємо у великих масштабах одержувати корисну роботу при хімічних процесах тільки непрямим шляхом: через перетворення в теплоту.
4.4. У реальних умовах вплив теплових викидів в окремі водойми, озера, ділянки рік може виявлятися різним образом у залежності від біологічної, гідрологічної і фізико-хімічної обстановки в даній водоймі, від діапазону, швидкості і частоти зміни температури і їхніх зв'язків із природними циклами.
Теплові викиди в атмосферу.
Будь-яке місцеве джерело теплоти достатньої інтенсивності сприяє утворенню термічної циркуляції, що чітко виявляється при безвітрі. Цей ефект спостерігається на висотах до декількох сотень метрів. У круглого "острова теплоти" діаметром 10 км при швидкості вітру близько 1 м/с вертикальна швидкість виникаючих рухів у шарі товщиною до 500 м досягає 10 м/с. Спостереження з літака за градирнями трьох вугільних ТЕС великої потужності привели до висновку про слабкий вплив теплових викидів на утворення хмарності і туманів.
Кількісні оцінки ролі енергетики серед інших видів антропогенних впливів, наприклад, домішкових викидів, неоднозначні. За деякими оцінками вчених, частка ТЕС у всіх сумарних домішкових викидах в атмосферу складає 27%. Викиди інших галузей н/г складають у %:
чорна металургія - 24,3
кольорова металургія - 10,5
нафтовидобуток і нафтохімія - 15,5
автотранспорт - 13,3
вир-во будівельних матеріалів - 8,1
хімічна промисловість - 1,3
Склад сумарних антропогенних викидів істотно відрізняється від складу викидів ТЕС і характеризується наступними цифрами, у %:
окис вуглецю - 31,9
тв. частки (пил) - 28,3
окис сірки - 27,0
окис азоту - 1,1
вуглеводні - 10,7
ін. речовини - 1,0
Зниження викидів з'єднань сірки.
1) Очищення від з'єднань сірки продуктів згоряння (димових газів).
2) Видалення сірки з палива до його спалювання.
Зниження викидів з'єднань азоту.
Серйозну увагу до цієї проблеми було звернено енергетиками практично лише наприкінці 60-х років ХХ століття.
Застосовують ряд режимних і конструктивних заходів:
- організація двоступінчастого процесу горіння (удається знизити рівень NOx у димових газах з 1,42 * 10-3% до 0,27 * 10-3% ( в І ступіні процес йде з браком О2 =0,81, а в ІІ - при невеликому надлишку).
- зниження коефіцієнта надлишку повітря (зменшення до 1,03 концентрація NOx може бути знижена на 25 - 30%.
- зниження температури газів у зоні горіння.
- уловлювання окислів азоту з наступною переробкою їх у товарні продукти (HNO3). Як поглиначі використовують: Na2CO3, Ca(OH)2, розчини NH3, силікагелі Sі2 * nН2O, торфолужні сорбенти.
- зниження викидів твердих часток
інерційні золоуловлювачі, мокрого типу, тканинні фільтри, електрофільтри, комбіновані золоуловлювачі.
- зниження забруднюючих викидів АЕС
склад радіоактивних відходів і їхню активність залежать від типу і конструкції реактора, від виду ядерного пального.
- очищення стічних вод електростанцій
відповідно до норм ГДК.
- удосконалювання теплових схем установок.
- зниження втрат при виробництві і транспортуванні енергії.
- удосконалювання процесів споживання енергії.
ЛЕКЦІЯ 5
ОСНОВНІ ПОНЯТТЯ ТЕРМОДИНАМІКИ
|
5.1. |
І закон термодинаміки |
|
|
5.2. |
Енергетичний баланс і його використання при розрахунках теплових процесів |
|
І закон термодинаміки є окремим випадком закону збереження і перетворення енергії.
Сума усіх видів енергії ізольованої системи є величина постійна, тобто dE = 0 або Ei = const, Ei - види енергії.
Енергія передається від навколишнього середовища до робочого тіла
E = Q + L (І)
Роботу навколишнього середовища над робочим тілом можна замінити роботою подолання робочим тілом сил навколишнього середовища, що буде чисельно дорівнювати L, але протилежні по напрямку, тобто зі знаком мінус (позначимо L* ). Тоді рівняння (І) перепишеться
Q = E + L*
Це рівняння і є математичне вираження І закону термодинаміки. Кількість енергії, підведеної до тіла в даній термодинамічній системі у формі теплоти, йде на зміну його енергії і на здійснення цим тілом зовнішньої роботи.
Енергія тіла складається з зовнішньої Ез и внутрішньої енергії.
Е = Ез + U
Зовнішня енергія тіла Ез являє собою суму кінетичної і потенційної енергій цього тіла. Перша з них, якщо зневажити кінетичною енергією обертання тіла навколо центра інерції, дорівнює mc2 , де с - швидкість центра інерції тіла, м/с; m - маса тіла, кг.
Друга складова зовнішньої енергії тіла - зовнішня потенційна енергія дорівнює mgН, де g - прискорення вільного падіння, м/с2; H - висота, м. Отже, зміна зовнішньої енергії тіла
![]()
Внутрішня енергія тіла являє собою енергію, обумовлену рухом і силами взаємодії часток робочого тіла (молекул, атомів, електронів, атомних ядер) і, отже, дорівнює сумі кінетичної і потенційної енергій цих часток. Внутрішня енергія є функцією основних термодинамічних параметрів стану. Для ідеальних газів потенційна енергія дрібних часток робочого тіла дорівнює нулеві, і, отже, їхня внутрішня енергія дорівнює кінетичній енергії, що, у свою чергу, є функцією тільки температури.
5.2. Деякі основні поняття термодинаміки можна проілюструвати на прикладі розповсюдженого технологічного процесу - випарки (мал.1). До апарата підводиться тепло в кількості Q1 при температурі Т1, і відводиться тепло з парами речовини, що випарюється, (наприклад, з парами води) у кількості Q2 при температурі Т2. Крім того, деяка кількість тепла губиться в навколишнє середовище (теплові втрати Qn). З першого закону термодинаміки випливає, що
Q1 = Q2 + Qn
Рівняння (І) - це рівняння енергетичного балансу випарки. Якщо тепловими втратами можна зневажити, тобто при Qn Q1, то Q1 = Q2. Величину Q1 часто називають витратами енергії. Цей термін не строгий. Відповідно до першого закону термодинаміки, енергія не затрачається, а лише переходить з однієї форми в іншу. У даному випадку енергія у формі тепла, підведена теплоносієм Q1, перейшла в енергію водяної пари, тобто з'явилося вторинне тепло Q2, яке можна використовувати для якої-небудь корисної мети. Тому правильно називати величину Q1 "підведена енергія", а Q2 - "відведена енергія". Нерідко застосовують також поняття втрати енергії, що, однак, у відповідності зі сказаним вище, неточно. У деякій мірі їм можна скористатися для позначення тих відведених від системи потоків енергії, що свідомо не можуть бути корисно використані. До таких втрат у даному випадку відносяться втрати тепла Qn через ізоляцію в навколишнє середовище, а також утрати, зв'язані з перекачуванням газів і рідин. У цьому випадку енергія, підведена до насоса, витрачається на нагрівання трубопроводів і потім розсіюється в навколишнє середовище. Якщо тепло Q2 не використовується, його часто відносять до "утрат тепла". Таким чином, під "втратами енергії" варто розуміти енергію, що не використовується в технічній системі (наприклад тому, що переходить у форму, непридатну для застосування). З приведеного вище приклада видно, що загальноприйнятий енергетичний баланс дає досить важливу інформацію про процес.
Однак ця інформація неповна і може привести до перекрученого уявлення про процес. Насамперед з енергетичного балансу неясно, що варто віднести до енергетичних витрат на процес. У розповсюдженому випадку, коли Qn = 0, ця задача при використанні тільки першого закону термодинаміки формально нерозв'язна. Якщо прийняти, що тепло Q2 не використовується, тоді ці витрати рівні Q1. Якщо ж тепло Q2 цілком використовується, то енергетичні витрати формально дорівнюють нулеві, що суперечить так званому "здоровому глуздові". Дійсно, з одного боку, витрати існують, з іншого боку - їх неможливо кількісно оцінити. Неясно також, як у цьому випадку оцінити ефективність процесу, ступінь його досконалості. Часто для оцінки ефективності процесу застосовують коефіцієнт корисної дії, дорівнюючий відношенню корисного ефекту до витрат. У даному випадку "тепловий", або термічний ККД дорівнює
Q = Q2/Q1 = 1 (2)
Отже, розрахунок "теплового" ККД не дає корисної інформації, тому що будь-який процес, незалежно від його технологічного оформлення, при повному обліку всіх потоків має ККД, рівний або близький до одиниці. Тоді, якщо довіряти отриманому результатові, удосконалювати процеси немає необхідності.
Приклади, аналогічні розглянутому, можна продовжити. У будь-якому хімічному виробництві значна кількість тепла приділяється від системи у виді так званих вторинних енергетичних ресурсів (ВЕР). Якщо в схемі, показаній на мал.1, протікає не випарка, а ендотермічна хімічна реакція, то частина підведеного тепла Qx витрачається на проведення хімічної реакції, а інше тепло Q2 відводиться у вигляді ВЕР з нагрітими продуктами реакції. Тоді кількість вторинного тепла буде дорівнювати
Q2 = Q1 - Qx (3)
При аналізі рівняння (3) може створитися враження, що при повному використанні ВЕР енергетичні витрати можна знизити з Q1 до Q1 - Q2 і відповідно зменшити витрату палива для підведення тепла. Цей висновок, як буде показано нижче, у загальному випадку невірний, тому що кількість і якість цих потоків неоднакові. Економія буде менше, ніж випливає з енергетичного балансу. Тому навіть у найпростішому випадку енергетичний баланс повинний бути доповнений іншою інформацією, що характеризує "якість", "цінність" енергії. Таку інформацію можна одержати з другого закону термодинаміки.
Мал.1
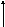
Qn

Q1(T1) Q2(T2)


Потоки енергії при випарці
Q1(T1) - підведене тепло; Q2(T2) - тепло, відведене з парами; Qn - теплові втрати в навколишнє середовище.
