
- •Н.В. Стулин, м.Н. Земцова, и.К. Моисеев
- •Углеводороды
- •Текст лекций по органической химии
- •Самара 2004
- •Гомологический ряд
- •Изомерия
- •Номенклатура
- •Рациональная номенклатура
- •Систематическая номенклатура (iupac)
- •Способы получения алканов
- •Промышленные методы
- •1. Метод Бергиуса (гидрогенизация бурых углей):
- •2. Метод Фишера-Тропша:
- •Лабораторные методы
- •3. Декарбоксилирование солей карбоновых кислот:
- •4. Гидрирование алкенов:
- •5. Восстановление галоидных алкилов:
- •Физические свойства алканов
- •Строение алканов
- •Химические свойства алканов
- •Реакции замещения
- •Общие проблемы галогенирования алканов
- •Реакции окисления
- •Мягкое окисление
- •Реакция расщепления (крекинг и пиролиз)
- •Отдельные представители
- •Лекция №3. Алкены
- •Гомологический ряд. Изомерия
- •Номенклатура
- •Промышленные источники алкенов
- •Методы синтеза алкенов
- •3. Дегалогенирование вицинальных дигалогенидов:
- •Физические свойства алкенов
- •Физические свойства некоторых этиленовых углеводородов приведены в табл.3.2
- •Строение алкенов
- •Химические свойства Гетерогенное каталитическое гидрирование
- •Реакции электрофильного присоединения
- •2. Присоединение галогеноводородных кислот (гидрогалогенирование):
- •Реакции радикального присоединения
- •Реакции окисления
- •1. Эпоксидирование (реакция Прилежаева):
- •2. Гидроксилирование (образование гликолей, реакция Вагнера):
- •Реакции по -углеродному атому
- •Полимеризация
- •Отдельные представители
- •Гомологический ряд диенов
- •Синтез изопрена
- •Синтез хлоропрена:
- •Лекция №6. Строение и химические свойства диенов
- •Строение и свойства алленов
- •1. Галогенирование:
- •2. Гидрогалогенирование:
- •3. Гидратация:
- •Строение сопряженных диенов
- •Химические свойства сопряженных диенов
- •5. Окисление:
- •Димеризация
- •Полимеризация
- •Гомологический ряд
- •Изомерия
- •Промышленные способы получения ацетилена
- •Из карбида кальция
- •Пиролиз метана.
- •Лабораторные способы получения ацетилена и его гомологов
- •1. Реакция дегидрогалогенирования:
- •Физические свойства
- •Строение алкинов
- •Химические свойства
- •Реакции присоединения
- •Присоединение воды к алкинам.
- •Отдельные представители
- •Строение бензола
- •Изомерия
- •Номенклатура
- •Методы получения
- •Промышленные источники
- •2. Нефть.
- •3. Из алкинов (Реппе, Зелинский):
- •Лабораторные способы
- •Лекция №10. Химические свойства арОматических углеводородов
- •Механизм реакций электрофильного замещения
- •Реакции электрофильного замещения
- •1. Нитрование:
- •2. Галогенирование:
- •3. Сульфирование. Для сульфирования часто применяется серная кислота, содержащая избыток so3 (олеум). Кислотно-основное равновесие между двумя молекулами серной кислоты:
- •Реакции окисления
- •3. Озонолиз:
- •4. Каталитическое окисление о2 в присутствии медного катализатора.
- •Влияние заместителей в бензольном ядре на электрофильное замещение
- •Распределение изомеров при нитровании производных бензола
- •Электрофильное замещение в дизамещенных бензолах
- •Отдельные представители
- •Нафталин
- •Изомерия, номенклатура
- •Способы получения
- •Структура нафталина
- •Химические свойства
- •Осторожное окисление нафталина и его гомологов приводит к потере ароматичности с образованием хинонов (в отличие от гомологов бензола):
- •Ориентация электрофильного замещения в нафталине
- •Антрацен и фенантрен
- •Гексафенилэтан
- •Библиографический список Основной
- •Дополнительный
- •Содержание
Отдельные представители
Из ацетиленовых углеводородов важное промышленное значение имеет только ацетилен.
Сжиженный ацетилен представляет большую опасность, так как он склонен к взрывному разложению. Теплота распада ацетилена на элементы составляет 226,9 кДж/моль, тогда как для этилена она равна 52,4 кДж/моль, а для этана 84,6кДж/моль. Поэтому сжатый ацетилен хранят в баллонах, наполненных адсорбентом, пропитанным подходящим растворителем (обычно ацетоном) под давлением до 2,5106 Па (25 атм).
При горении ацетилена в кислороде развивается очень высокая температура (до 3000С), поэтому он широко применяется для так называемой ацетиленовой сварки и резки металлов.
Ацетилен нашел широкое применение в химической промышленности, преимущественно для получения пластмасс, каучука, растворителей.
Значительная часть ацетилена в технике перерабатывается в винилацетилен. Винилацетилен при обычных условиях – газ. Подобно дивинилу он присоединяет галогены в 3,4- (по ацетиленовой связи) и в 1,4-положения, аналогично присоединяются и галогеноводороды. В присутствии катализаторов Cu2Cl2 и других 1,4-аддукты легко изомеризуются в 3,4-аддукты. Эта реакция используется в синтезе хлоропренового каучука из винилацетилена.
Лекция №9. АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
Ароматические углеводороды. Понятие ароматичности. Современные электронные и квантово-химические представления о строении бензола. Гомологический ряд бензола. Общая формула. Изомерия. Номенклатура. Методы получения: из каменного угля, нефти, реакцией Вюрца-Фиттига, Фриделя-Крафтса.
Первый представитель ароматических углеводородов - бензол известен с 1825 года. Впервые его выделил Фарадей из китового жира - ворвань.
Строение бензола

Впервые Кеккуле предложил структурную формулу бензола в 1865 году Современная точка зрения на строение бензола: плоская молекула, атомы углерода которой находятся в состоянии sp2 -гибридизации и объединены в правильный шестиугольник.
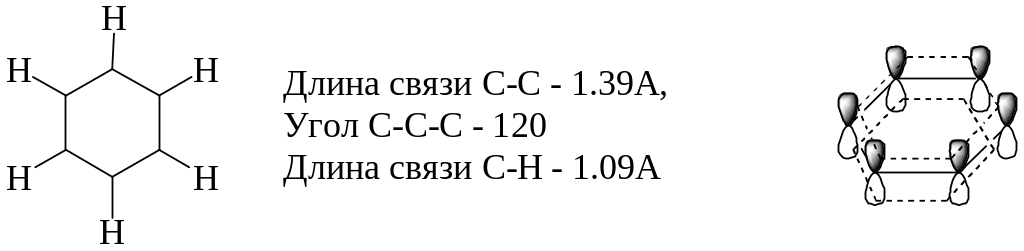
Негибридизованные р-орбитали располагаются перпендикулярно плоскости кольца и при боковом перекрывании образуют единую -молекулярную орбиталь, расположенную над и под плоскостью цикла (сопряжение р-орбиталей).
Изображение молекулы бензола:

Строение определяет устойчивость бензола. Он с трудом вступает в реакции присоединения, так как это связано с разрывом сопряженного электронного облака, что энергетически невыгодно. Также трудно протекают и реакции окисления бензольного кольца. Для бензола характерны реакции электрофильного замещения, так как существует π-молекулярная орбиталь и происходит замещение атома водорода электрофильным реагентом.
Энергия резонанса в молекуле бензола показана ниже.

Ароматичность - необычайно низкая энергия невозбужденного состояния, вызванная делокализацией π-электронов.
Изомерия
Для ди-, три- и тетразамещенных ароматических углеводородов характерна изомерия положения заместителя и изомерия боковой алкильной цепи.
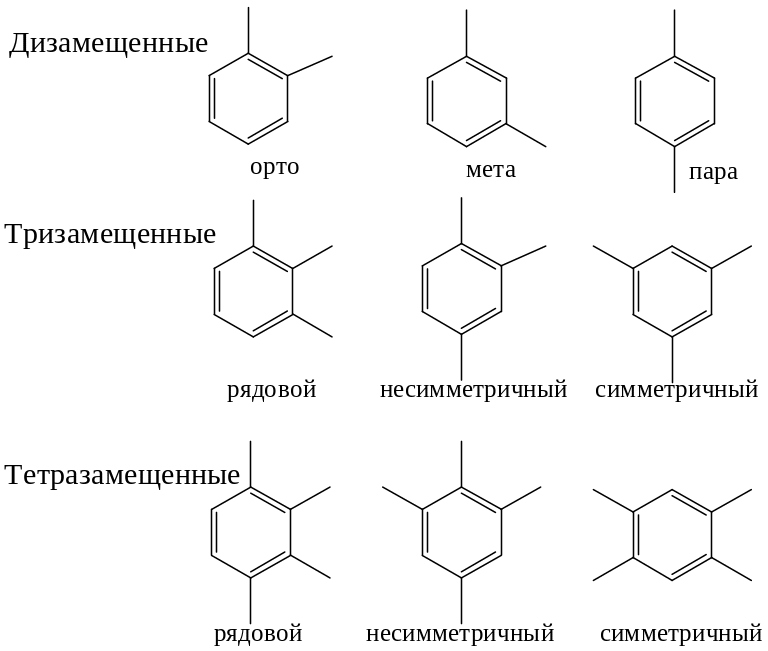
Моно-, пента- и гексазамещенные арены не имеют изомеров, связанных с положением заместителя в кольце.
Номенклатура
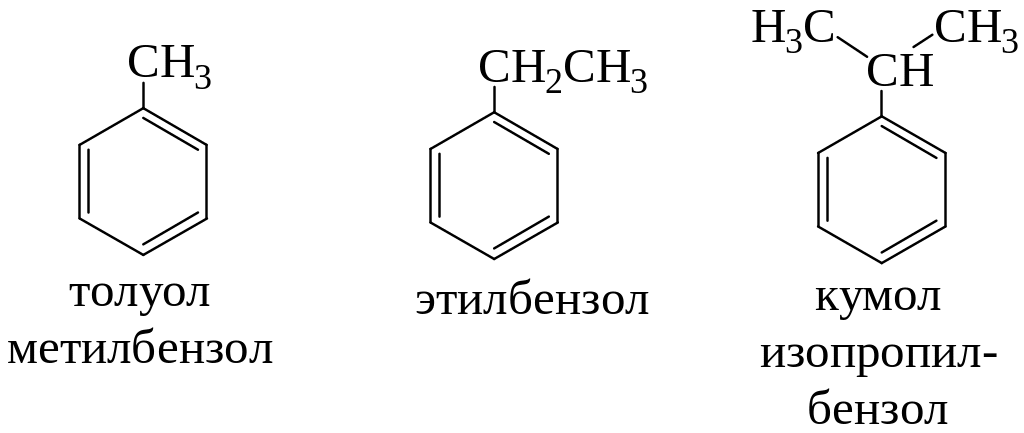
Производные бензола называют замещенными бензолами. Для многих из них либо используют тривиальные названия, либо заместитель обозначается приставкой перед словом «бензол». В случае монозамещенных бензолов в названия не входят цифры, так как все шесть атомов углерода молекулы бензола равноценны, для каждого заместителя возможен только один монозамещенный бензол.
Если в молекуле бензола присутствуют два заместителя, то могут существовать три различных дизамещенных бензола. Они называются соответственно орто-, мета- и пара-замещенными:
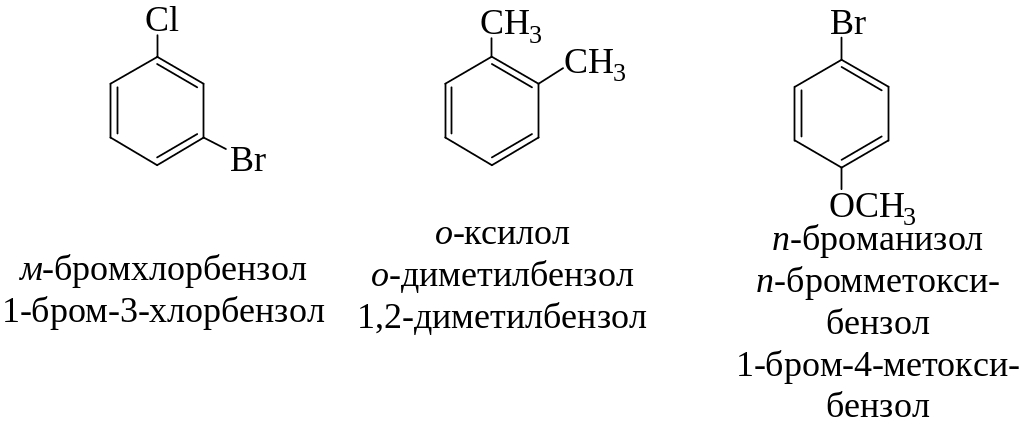
Если в бензоле имеется три и более заместителей, то их положение в кольце следует обозначать только цифрами. Во всех случаях названия заместителей перечисляют перед словом «бензол» в алфавитном порядке. Цифра 1 в названии может быть пропущена, заместитель, с которого начинается отсчет, в этом случае входит в основу названия:

Радикалы бензола и толуола соответственно называют фенил-, бензил- и о-, м- и п-толил:

