
- •Н.В. Стулин, м.Н. Земцова, и.К. Моисеев
- •Углеводороды
- •Текст лекций по органической химии
- •Самара 2004
- •Гомологический ряд
- •Изомерия
- •Номенклатура
- •Рациональная номенклатура
- •Систематическая номенклатура (iupac)
- •Способы получения алканов
- •Промышленные методы
- •1. Метод Бергиуса (гидрогенизация бурых углей):
- •2. Метод Фишера-Тропша:
- •Лабораторные методы
- •3. Декарбоксилирование солей карбоновых кислот:
- •4. Гидрирование алкенов:
- •5. Восстановление галоидных алкилов:
- •Физические свойства алканов
- •Строение алканов
- •Химические свойства алканов
- •Реакции замещения
- •Общие проблемы галогенирования алканов
- •Реакции окисления
- •Мягкое окисление
- •Реакция расщепления (крекинг и пиролиз)
- •Отдельные представители
- •Лекция №3. Алкены
- •Гомологический ряд. Изомерия
- •Номенклатура
- •Промышленные источники алкенов
- •Методы синтеза алкенов
- •3. Дегалогенирование вицинальных дигалогенидов:
- •Физические свойства алкенов
- •Физические свойства некоторых этиленовых углеводородов приведены в табл.3.2
- •Строение алкенов
- •Химические свойства Гетерогенное каталитическое гидрирование
- •Реакции электрофильного присоединения
- •2. Присоединение галогеноводородных кислот (гидрогалогенирование):
- •Реакции радикального присоединения
- •Реакции окисления
- •1. Эпоксидирование (реакция Прилежаева):
- •2. Гидроксилирование (образование гликолей, реакция Вагнера):
- •Реакции по -углеродному атому
- •Полимеризация
- •Отдельные представители
- •Гомологический ряд диенов
- •Синтез изопрена
- •Синтез хлоропрена:
- •Лекция №6. Строение и химические свойства диенов
- •Строение и свойства алленов
- •1. Галогенирование:
- •2. Гидрогалогенирование:
- •3. Гидратация:
- •Строение сопряженных диенов
- •Химические свойства сопряженных диенов
- •5. Окисление:
- •Димеризация
- •Полимеризация
- •Гомологический ряд
- •Изомерия
- •Промышленные способы получения ацетилена
- •Из карбида кальция
- •Пиролиз метана.
- •Лабораторные способы получения ацетилена и его гомологов
- •1. Реакция дегидрогалогенирования:
- •Физические свойства
- •Строение алкинов
- •Химические свойства
- •Реакции присоединения
- •Присоединение воды к алкинам.
- •Отдельные представители
- •Строение бензола
- •Изомерия
- •Номенклатура
- •Методы получения
- •Промышленные источники
- •2. Нефть.
- •3. Из алкинов (Реппе, Зелинский):
- •Лабораторные способы
- •Лекция №10. Химические свойства арОматических углеводородов
- •Механизм реакций электрофильного замещения
- •Реакции электрофильного замещения
- •1. Нитрование:
- •2. Галогенирование:
- •3. Сульфирование. Для сульфирования часто применяется серная кислота, содержащая избыток so3 (олеум). Кислотно-основное равновесие между двумя молекулами серной кислоты:
- •Реакции окисления
- •3. Озонолиз:
- •4. Каталитическое окисление о2 в присутствии медного катализатора.
- •Влияние заместителей в бензольном ядре на электрофильное замещение
- •Распределение изомеров при нитровании производных бензола
- •Электрофильное замещение в дизамещенных бензолах
- •Отдельные представители
- •Нафталин
- •Изомерия, номенклатура
- •Способы получения
- •Структура нафталина
- •Химические свойства
- •Осторожное окисление нафталина и его гомологов приводит к потере ароматичности с образованием хинонов (в отличие от гомологов бензола):
- •Ориентация электрофильного замещения в нафталине
- •Антрацен и фенантрен
- •Гексафенилэтан
- •Библиографический список Основной
- •Дополнительный
- •Содержание
3. Озонолиз:
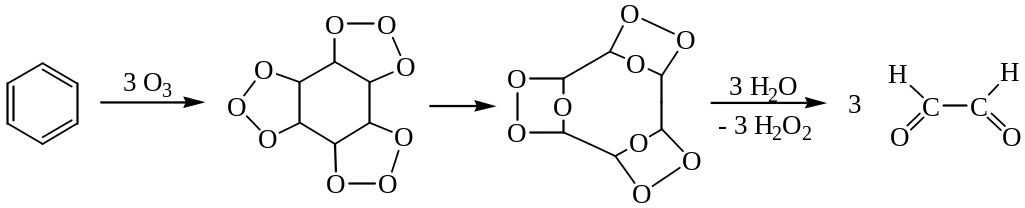
4. Каталитическое окисление о2 в присутствии медного катализатора.

Правила ориентации в бензольном ядре
Наличие заместителя в молекуле бензола требует ответа на два вопроса:
1. Какое влияние оказывает заместитель на скорость реакции – замедляет или ускоряет ее по сравнению со скоростью реакции незамещенного бензола?
2. В какое положение бензольного кольца он направляет электрофильную частицу Е+?
Эти вопросы связаны с перераспределением электронной плотности в бензольном кольце.
Рассмотрим два типа заместителей:

Метильная группа проявляет донорные свойства по отношению к бензольному кольцу за счет +I эффекта и эффекта гиперконъюгации (сверхсопряжения), что приводит к повышению электронной плотности в о- и п-положениях и, следовательно, к активации молекулы толуола в реакциях с электрофильными агентами и вступлению нового заместителя именно в о- и п-положения. Нитрогруппа обладает электроноакцепторными свойствами по отношению к бензольному кольцу из-за сильных –М и –I эффектов. Это приводит к уменьшению электронной плотности в о- и п-положениях бензольного кольца и дезактивации нитробензола по сравнению с незамещенным бензолом. м-Положения молекулы нитробензола менее чувствительны к влиянию нитрогруппы, частичный положительный заряд на этих атомах углерода меньше, чем в о- и п-положениях, поэтому в этом случае атака электрофила происходит в м-положение бензольного кольца.
Таким образом, электронодонорные заместители увеличивают электронную плотность в бензольном кольце и облегчают атаку электрофилом, замещение происходит в о- и п-положения. Реакции проходят быстрее, чем в случае незамещенного бензола. Электронодонорными свойствами обладают следующие заместители:
-NH2, -NHR, -NR2, -OH, -OR, -R (алкил)
Ряд по увеличению активности электронодонорных заместителей (увеличение скорости реакции):
NH2 OH OR Cl I CH3
Электроноакцепторные заместители, напротив, понижают электронную плотность в бензольном кольце, что затрудняет взаимодействие с электрофилом и приводит к снижению скорости реакции замещения по сравнению незамещенным бензолом, атака электрофилом осуществляется в м-положения бензольного кольца. Акцепторными свойствами обладают следующие функциональные группы:

Ряд по увеличению активности электроноакцепторных заместителей (уменьшение скорости реакции):
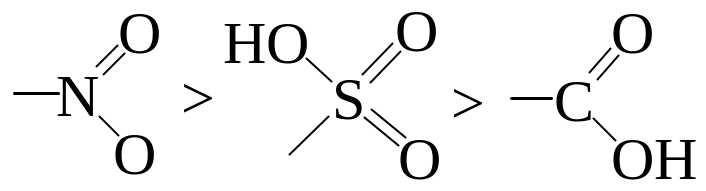
Особенности влияния галогенов. Галогены дезактивируют молекулу бензола в реакциях электрофильного замещения, но направляют электрофильный агент в о- и п-положения бензольного кольца. Это связано с тем, что –I – эффект атомов галогенов сравним с +М – эффектом.

Таблица 10.1
Влияние заместителей в бензольном ядре на электрофильное замещение
-
Орто-, пара - ориентанты
Мета-ориентанты
Активизируют ароматическое кольцо
-OH, -OR
-NH2, -NHR, -NR2
-NHCOR
Алкил
Арил
Дезактивируют
F, Cl, Br, I
Дезактивируют ароматическое кольцо
-CN
-COOH
-COOR
-CHO
-NO2
-+NR3
-SO3H, -SO2OR
Хотя заместители и подразделяются для удобства на два класса - о, п и м-ориентанты (табл. 10.1), однако, практически существует очень мало реакций, в которых образовались бы только о-, п- или м-замещенные. Большинство реакций приводит к получению всех трех изомеров, а ориентирующее влияние сказывается на том, какой из них образуется в избытке.
В табл. 10.2 показано, что большинство о-, п-ориентирующих заместителей дают больше продуктов пара-замещения, чем орто, несмотря на то, что орто-положений два. Причиной тому служат стерические факторы. В качестве примера приведем данные по изомерному составу смеси продуктов реакции нитрования различных производных бензола:

Таблица 10. 2
