- •Н.В. Стулин, м.Н. Земцова, и.К. Моисеев
- •Углеводороды
- •Текст лекций по органической химии
- •Самара 2004
- •Гомологический ряд
- •Изомерия
- •Номенклатура
- •Рациональная номенклатура
- •Систематическая номенклатура (iupac)
- •Способы получения алканов
- •Промышленные методы
- •1. Метод Бергиуса (гидрогенизация бурых углей):
- •2. Метод Фишера-Тропша:
- •Лабораторные методы
- •3. Декарбоксилирование солей карбоновых кислот:
- •4. Гидрирование алкенов:
- •5. Восстановление галоидных алкилов:
- •Физические свойства алканов
- •Строение алканов
- •Химические свойства алканов
- •Реакции замещения
- •Общие проблемы галогенирования алканов
- •Реакции окисления
- •Мягкое окисление
- •Реакция расщепления (крекинг и пиролиз)
- •Отдельные представители
- •Лекция №3. Алкены
- •Гомологический ряд. Изомерия
- •Номенклатура
- •Промышленные источники алкенов
- •Методы синтеза алкенов
- •3. Дегалогенирование вицинальных дигалогенидов:
- •Физические свойства алкенов
- •Физические свойства некоторых этиленовых углеводородов приведены в табл.3.2
- •Строение алкенов
- •Химические свойства Гетерогенное каталитическое гидрирование
- •Реакции электрофильного присоединения
- •2. Присоединение галогеноводородных кислот (гидрогалогенирование):
- •Реакции радикального присоединения
- •Реакции окисления
- •1. Эпоксидирование (реакция Прилежаева):
- •2. Гидроксилирование (образование гликолей, реакция Вагнера):
- •Реакции по -углеродному атому
- •Полимеризация
- •Отдельные представители
- •Гомологический ряд диенов
- •Синтез изопрена
- •Синтез хлоропрена:
- •Лекция №6. Строение и химические свойства диенов
- •Строение и свойства алленов
- •1. Галогенирование:
- •2. Гидрогалогенирование:
- •3. Гидратация:
- •Строение сопряженных диенов
- •Химические свойства сопряженных диенов
- •5. Окисление:
- •Димеризация
- •Полимеризация
- •Гомологический ряд
- •Изомерия
- •Промышленные способы получения ацетилена
- •Из карбида кальция
- •Пиролиз метана.
- •Лабораторные способы получения ацетилена и его гомологов
- •1. Реакция дегидрогалогенирования:
- •Физические свойства
- •Строение алкинов
- •Химические свойства
- •Реакции присоединения
- •Присоединение воды к алкинам.
- •Отдельные представители
- •Строение бензола
- •Изомерия
- •Номенклатура
- •Методы получения
- •Промышленные источники
- •2. Нефть.
- •3. Из алкинов (Реппе, Зелинский):
- •Лабораторные способы
- •Лекция №10. Химические свойства арОматических углеводородов
- •Механизм реакций электрофильного замещения
- •Реакции электрофильного замещения
- •1. Нитрование:
- •2. Галогенирование:
- •3. Сульфирование. Для сульфирования часто применяется серная кислота, содержащая избыток so3 (олеум). Кислотно-основное равновесие между двумя молекулами серной кислоты:
- •Реакции окисления
- •3. Озонолиз:
- •4. Каталитическое окисление о2 в присутствии медного катализатора.
- •Влияние заместителей в бензольном ядре на электрофильное замещение
- •Распределение изомеров при нитровании производных бензола
- •Электрофильное замещение в дизамещенных бензолах
- •Отдельные представители
- •Нафталин
- •Изомерия, номенклатура
- •Способы получения
- •Структура нафталина
- •Химические свойства
- •Осторожное окисление нафталина и его гомологов приводит к потере ароматичности с образованием хинонов (в отличие от гомологов бензола):
- •Ориентация электрофильного замещения в нафталине
- •Антрацен и фенантрен
- •Гексафенилэтан
- •Библиографический список Основной
- •Дополнительный
- •Содержание
Реакция расщепления (крекинг и пиролиз)
Крекинг - процесс деструктивной переработки нефти или ее фракций, проводимый для увеличения выхода легких продуктов и повышения их качества, главным образом для получения легких моторных топлив.
Крекинг бывает термический, каталитический, крекинг с водяным паром, гидрокрекинг (температура 250 - 450С, Н2, давление).
Пример:
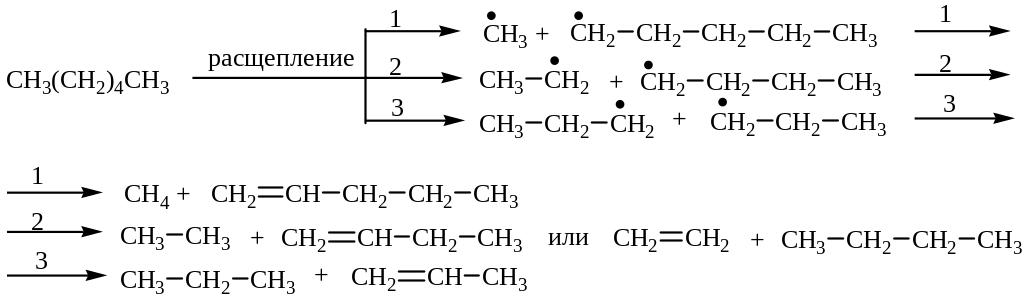
Пиролиз алканов также носит радикальный характер и протекает с образованием различных продуктов:

Применение пиролиза идет по двум основным направлениям - топливному и «химическому». В первом случае основной целью является получение высококачественных (газообразных, жидких и твердых) топлив и масел. Во втором случае целевым назначением пиролиза является получение химического сырья, в первую очередь олефинов и ароматических углеводородов, для промышленного органического синтеза.
Отдельные представители
Первый в ряду предельных углеводородов – метан – является основной частью природных и попутных газов и широко используется в качестве промышленного и бытового газа. Химически перерабатывается главным образом в ацетилен, газовую сажу, фторо- и хлоропроизводные.
Этан, пропан, бутан и пентаны используются в технике для получения соответственно этилена, пропилена, дивинила и изопрена (дегидрирование, в последнем случае с изомеризацией). Смесь пропана и бутана используется в качестве топлива (бытовой сжиженный газ). Значительные количества бутана используются в технике для получения уксусной кислоты (окисление).
Высшие жидкие и твердые парафины используются как дизельное топливо, смазочный материал, в виде твердого парафина, озокерита и т.д.
Лекция №3. Алкены
Гомологический ряд. Общая формула. Изомерия. Номенклатура. Способы получения: из алканов, галогеналканов, алкинов и спиртов. Физические свойства.
Гомологический ряд. Изомерия
Двойная углерод - углеродная связь является отличительным признаком алкенов. Алкены образуют гомологический ряд с общей формулой CnH2n: С2Н4 (этилен), С3Н6 (пропилен), С4Н8 (бутилены) и т.д.
Для алкенов характерна структурная и геометрическая изомерия. Структурная изомерия связана с изомерией углеродного скелета и положением двойной связи. Так, углеводород С4Н8 существует в виде трех структурных изомеров:
![]()
Геометрическая изомерия алкенов связана с расположением заместителей относительно двойной углерод - углеродной связи: по одну сторону связи (цис-изомеры) либо по разные стороны связи (транс изомеры):

Существование геометрической изомерии связано с затрудненным вращением вокруг двойной связи, которое невозможно без разрыва -связи, а это требует значительной затраты энергии.
Геометрические изомеры имеют различные физические свойства (температуру плавления, температуру кипения, показатель преломления, растворимость, плотность). Это позволяет разделить их перегонкой, кристаллизацией.
Геометрические изомеры имеют аналогичные химические свойства, но скорости реакций различны.
Номенклатура
Существует несколько способов названия алкенов (тривиальная, рациональная и систематическая номенклатуры). Простейшие алкены имеют тривиальные названия - этилен, пропилен, бутилены.
По рациональной номенклатуре углеводороды с двойной связью называют как производные этилена, положение заместителей обозначается буквами - и :
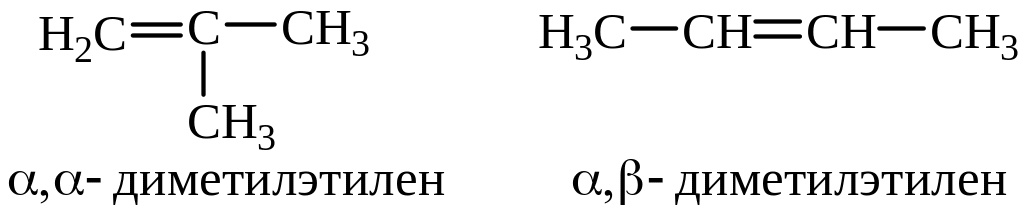
По систематической номенклатуре IUPAC за основу названия принимают самую длинную углеродную цепь, содержащую двойную связь, нумерация начинается с углеродного атома, расположенного ближе к двойной связи. Положение двойной связи обозначается цифрой. Цифрами обозначают и положения алкильных групп, связанных с основной цепью. В названии основной углеводородной цепи окончание –ан названия соответствующего алкана заменяют на -ен:

Для названия цис-, транс изомеров была создана E,Z-номенклатура. Используя систему Кана - Ингольда – Прелога (заместитель тем старше, чем больше порядковый номер в периодической системе атома, связанного с атомом углерода кратной связи, либо, если это атом углерода, то чем более он окислен), определяют сначала относительное старшинство заместителей, связанных с двойной связью, и дают им номера по старшинству 1 или 2. Если две наиболее старшие группы расположены по одну сторону от плоскости -связи, то конфигурация обозначается Z, если же по разные стороны, то E: